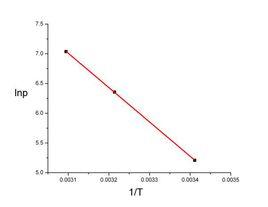
公式
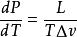 克拉伯龍方程
克拉伯龍方程其中L是相變潛熱,Δv是比體積的變化。
推導
 典型的相圖,途中的界限即為相平衡線
典型的相圖,途中的界限即為相平衡線通過吉布斯自由能導出克拉伯龍方程:
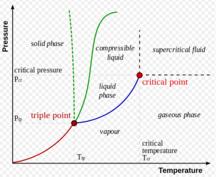
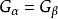 克拉伯龍方程
克拉伯龍方程在α和β兩相平衡的時候應該有
而dG=-sdT+Vdp,其中s為比熵 因此有
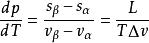 克拉伯龍方程
克拉伯龍方程另外
值得注意的是,把理想氣體方程和克拉伯農方程等效是不正確的。一般克拉伯龍方程是指描述相平衡的方程dp/dT=L/(TΔv)。儘管理想氣體定律是由克拉伯龍發現,但是國際上不把理想氣體狀態方程叫克拉伯龍方程。
理想氣體狀態方程,描述理想氣體狀態變化規律的方程。由克拉伯龍於將玻意耳定律和蓋-呂薩克定律合併起來。特此澄清一點,部分國內教材將理想氣體狀態方程和克拉伯龍方程畫等號,這是不正確的。儘管理想氣體狀態方程是由克拉伯龍提出的,但是克拉伯龍方程所描述的是相平衡的物理量。國際慣例,將理想氣體狀態方程稱為State Equation of Ideal Gas 或者 Ideal Gas law, 而克拉伯龍方程 Clapeyron Equation的同義詞是 Clausius-Clapeyron Relation 或者 Clapeyron Equation.大量百度知道和之前的百度百科混淆了這一點。