反應機理
Sn1反應機理是分步進行的,反應物首先解離為碳正離子與帶負電荷的離去基團,這個過程需要能量,是控制反應速率的一步,即慢的一步。當分子解離後,碳正離子馬上與親核試劑結合,速率極快,是快的一步。
Sn1反應速率只與一種反應物有關,是動力學一級反應。
在Sn1反應中,試劑的親核性並不重要,因為親核試劑與底物的反應不是決定速率的一步,對反應速率的影響不大,同時碳正離子的反應性很高,不管試劑的親核能力是大還是小,均能發生反應。比較起來,在Sn2反應中,親核試劑提供一對電子,與底物的碳原子成鍵,試劑的親核性越強,成鍵越快。因此在Sn2反應中試劑親核性的強弱,對反應的影響很大。
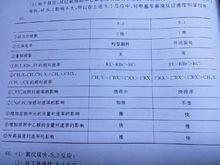 SN1與SN2的對比
SN1與SN2的對比性質
1、Sn1導致產物 外消旋化;這是因為OHˉ可以從碳正離子的兩面進攻,而生成兩個構型相反的化合物。但其外消旋化產物大多數並非1:1生成,這可以從反應機理進行解釋。有科學家認為,其機理應介於Sn1與Sn2之間。
2、Sn1會導致產物的 重排。這是因為碳正離子發生了向更穩定的碳正離子重排。
實例
下面以叔丁基溴在鹼性水溶液中的水解為例子。
叔丁基溴的水解速率只與叔丁基溴的濃度都成正比(CH3)3C-Br+OH-→(CH3)3C-OH+Br-
v=k[(CH3)3CBr]
首先,叔丁基溴在溶劑中水解為叔丁基正離子、Brˉ。過程為C-Br鍵逐漸伸長,電子云偏向Brˉ,並使得中心碳原子上的正電荷逐漸增加,達到過渡態,再繼續解離為離子。解離所需的能量由生成的離子發生的溶劑化作用補償;接著,OHˉ進攻中心碳原子,並經過過渡態,最後生成產物。
總結
影響SN反應活性的因素有:烴基的結構、離去基的種類、親核試劑的親核性、溶劑的極性等。
(1)不同烴基反應活性:叔>仲>伯。其中烯丙型和苄基型的鹵代烴都有極高的活性。
(2)離去基團越易離去,反應的速度越高。其中I>Br>Cl。
(3)試劑親核性對SN1反應無太大影響,但影響SN2反應。
(4)極性試劑有利於SN1反應

