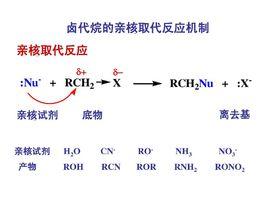
親核反應定義
由親核試劑進攻反應物而引起的反應稱為親核反應。親核反應又可以進一步分為親核加成反應,親核取代反應。親核取代反應又包括單分子親核取代和雙分子親核取代。
親核加成反應
定義
親核加成反應是由親核試劑與底物發生的加成反應。反應發生在碳氧雙鍵、碳氮叄鍵、碳碳叄鍵等等不飽和的化學鍵上。反應過程中,一般是親核試劑中帶負電荷的部分(即親核部分)先進攻底物中不飽和化學鍵帶部分正電荷一端原子,並與之成鍵,π鍵斷開形成另一端原子的負離子中間體,然後試劑中的親電部分與負離子中間體結合,形成親核加成產物。
代表反應
最有代表性的反應是醛或酮的羰基與格氏試劑加成的反應。
RC=O + R'MgCl → RR'C-OMgCl
再水解得醇,這是合成醇的良好辦法。在羰基中,O稍顯電負性;在格氏試劑中,C-Mg相連,Mg稍顯電正性,C是親核部位。於是格式試劑的親核碳進攻親電的羰基碳,雙鍵打開,新的C-C鍵形成。
水、醇、胺類以及含有氰離子的物質都可以與羰基加成。碳氮叄鍵(氰基)的親核加成主要表現為水解生成羧基。此外,端炔的碳碳叄鍵也可以與HCN等親核試劑發生親核加成,如乙炔和氫氰酸反應生成丙烯腈。
判斷標準
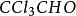 親核反應
親核反應羰基碳正電性強的活性強,空間阻礙小的活性強, 連有吸電子基可使正電性加強,推電子基減弱, 這部分不會考活性比較的, 重點是親核取代,即先加成再消除的機理 還要有負碳離子反應。親核加成反應活性最強的化合物是: 。
單分子親核取代
定義
單分子親核取代反應(unimolecular nucleophilic substitution,SN1)是只有一種分子參與了決定反應速率關鍵步驟的親核取代反應,簡寫為SN1,其中S表示取代反應,角標N表示親核,1表示只有一種分子參與速控步驟。
反應機理
SN1反應的反應機理可概述為:反應物首先解離為碳正離子與帶負電荷的離去基團,這個過程需要能量,是控制反應速率的一步。分子解離後,碳正離子立即與親核試劑結合,是快的一步。以叔丁基溴在鹼性溶液中的水解反應為例,其反應步驟如下:
反應的第一步是叔丁基溴緩慢解離形成叔丁基正碳離子和溴負離子,這一過程需要的能量大,是控制反應速率的一步,也是慢的一步。第一步生成的正碳離子性質活潑,稱為活性中間體。而正碳離子的穩定性是影響SN1速率的主要因素,越穩定的正碳離子越容易形成,形成的速度也越快,所以SN1反應中,鹵代烷的反應活性與正碳離子的穩定性次序相同。正碳離子一旦形成,立即與親核試劑OH-結合生成產物,並釋放能量,這就是反應的第二步,是快的一步。第二步反應較慢,是決定整個反應速率的步驟。由於整個反應僅與叔丁基溴的濃度有關,而且發生共價鍵變化的也只有叔丁基溴一種分子,而與親核試劑的濃度無關,所以稱為單分子親核取代反應(SN1)。
特點
①SN1反應為一級反應。
②反應分步進行,有碳正離子中間體生成,常發生重排。
③反應物中心碳原子是手性碳原子時,產物外消鏇化(鏇光性部分或全部消失)。
雙分子親電取代
定義
雙分子親核取代反應反應(SN2)是親核取代反應的一類,其中S代表取代(Substitution),N代表親核(Nucleophilic),2代表反應的決速步涉及兩種分子。與SN1反應相對應,SN2反應中,親核試劑帶著一對孤對電子進攻具親電性的缺電子中心原子,形成過渡態的同時,離去基團離去。反應中不生成碳正離子,速率控制步驟是上述的協同步驟,反應速率與兩種物質的濃度成正比,因此稱為雙分子親核取代反應。無機化學中,常稱雙分子親核取代反應類型的反應機理為“交換機理”。
機理
SN2反應最常發生在脂肪族sp3雜化的碳原子上,碳原子與一個電負性強、穩定的離去基團(-X)相連,一般為鹵素陰離子。親核試劑(Nu)從離去基團的正後方進攻碳原子,Nu-C-X角度為180°,以使其孤對電子與C-X鍵的σ反鍵軌道可以達到最大重疊。然後形成一個五配位的反應過渡態,碳約為sp2雜化,用兩個垂直於平面的 p軌道分別與離去基團和親核試劑成鍵。C-X的斷裂與新的C-Nu鍵的形成是同時的,-X很快離去,形成含C-Nu鍵的新化合物。
SN2反應也可以在分子內發生,合成的環系一般為五元環、六元環和三元環。分子內的Williamson合成得到環氧化合物,即是這類反應的一個例子。
相比下,四元環張力太大,空間上也不利,很難生成;七元、八元之類的大環可以生成,但分子間反應處於優勢,需要將反應物以高稀溶液的形式反應,以增大分子內產物的比例。
SN2反應一般發生在伯碳原子上,很難成為有位阻分子的反應機理,並且取代基越多,按SN2機理反應的可能性越小。基團在空間上比較擁擠的分子一般採用SN1機理,可以緩解一部分的位阻,也可生成較穩定的碳正離子(通常為三級碳正離子)。
由於親核試劑是從離去基團的背面進攻,故如果受進攻的原子具有手性,則反應後手性原子的立體化學發生構型翻轉,也稱“瓦爾登翻轉”。這也是SN2反應在立體化學上的重要特徵。反應過程類似於大風將雨傘由里向外翻轉。
影響因素
1)離去基團的鹼性越強,其離去能力越弱,反之亦然。離子的鹼性隨著所在周期的增加而降低。對於鹵素離子而言,碘離子的鹼性最弱,因此碘離子是一個很好的離去基團;氟離子則相反,氟代烴也因此很難發生SN2反應。鹼性 F-> Cl-> Br-> I-,離去能力與上述順序相反。
2)親核性需要與上面的鹼性相區別。鹼性是試劑對質子的親和能力,而親核性是試劑形成過渡態時,對碳原子的親和能力。一般來講,試劑的負電性、鹼性和可極化性越強,其親核性也越強。實際上通常需要綜合考慮這幾個因素以及溶劑的影響。
3)SN2反應在質子溶劑中進行時,一方面,溶劑化作用有利於離去集團的離去;另一方面,溶劑也會與親核試劑發生作用,使親核試劑與底物的接觸變得困難。最後的影響是這兩種因素的綜合結果。相對而言,非極性溶劑分子很少包圍負離子,因此對SN2反應是有利的。
4)位阻(含體積大的取代基)會使親核試劑的親核性下降。雖然乙醇的酸性比叔丁醇強,但叔丁氧基負離子的親核性弱於乙氧基負離子,就是因為這個緣故。