簡介
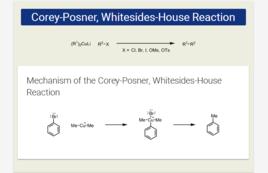
二烴基銅鋰(吉爾曼試劑)與鹵代烴反應,偶聯為烷烴。
反應機理
反應一般分為三步進行。首先是用金屬鋰在醚中處理鹵代烴(R-X),將其轉變為烴基鋰化合物(R-Li)。此處的鹵代烴可以是一級、二級或三級鹵代烴。
第二步是用碘化亞銅(CuI)處理上述烴基鋰化合物,得到反應中用到的試劑二烷基銅鋰(R2CuLi)。二烷基銅鋰試劑最早是由美國化學家亨利·吉爾曼(Henry Gilman)製得的,故通常稱為吉爾曼試劑。
最後用二烷基銅鋰與另一分子鹵代烴(R'-X)進行反應,偶聯生成含新生成的碳-碳鍵的產物(R-R')。
若第二分子鹵代烴與第一分子鹵代烴不同(R ≠ R'),那么該反應可以視為一種交叉偶聯反應。
第二分子鹵代烴為甲基鹵、苄鹵、伯鹵代烴和環狀仲鹵代烴時反應進行得較為順利。
 反應機理
反應機理反應示例
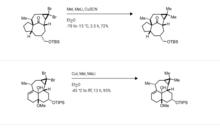 反應示例
反應示例吉爾曼試劑
簡述
一類有機金屬化合物,是親核取代反應很好的反應物,主要作用是在溶解有機生物上有良好效果。不過由於烴基鋰比烴基鎂價錢較高,只需要親核加成反應時多用格林尼亞試劑。
製備
吉爾曼試劑一般分兩步製備:第一步用烴基鹵(R-X)與鋰在液態烷反應,形成烴基鋰。原子即插在烴基和鹵素原子之間。由於烴基鋰化合物比格林尼亞試劑更活潑,遇水即水解,遇羰基即加成,因此在第二步反應時用鹵化銅製成有烴基鋰的較不活潑的烴基銅。反應器皿中不能有水,也不能有二氧化碳。
R-X+2Li → RLi+LiX(液態烷溶劑)(X=氯、溴或碘)
2RLi+CuX → RCuLi+LiX(醚溶劑)
性質
由於銅和鋰原子直接和碳鏈相連,鄰近鎂原子的那個碳原子就積聚了很多負電荷,這根C-Cu和C-Li鍵極具反應活性。為了保證吉爾曼試劑不發生其他反應,反應一般在乙醚中進行。吉爾曼試劑和同類的格林尼亞試劑都是一種烷基載體,但由於格林尼亞試劑有二價鎂,格林尼亞試劑會與其他烴基鹵形成二烷基鎂化合物,破壞其功用。吉爾曼試劑則可以直接與其他烴基滷製成烷;由於這是親核取代反應,理論上烴基碘的效果較好。
R'-X+RCuLi→R-R'+R-Cu+LiX(醚溶劑)。