成份
鹽酸托莫西汀
化學名:(-) -N-甲基 -3-苯基 -3-(O-甲苯氧基)-丙胺鹽酸鹽。
結構式:
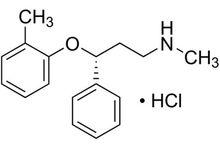 鹽酸托莫西汀膠囊
鹽酸托莫西汀膠囊分子式:CHNO.HCl
分子量:291.82
性狀:
本品為膠囊劑,內容物為白色至類白色粉末。
適應症
用於治療兒童和青少年(6歲-18歲)的注意缺陷/多動障礙(ADHD)。
規格
10mg、18mg、25mg、40mg
用法用量:
初始治療 :
體重不足70公斤的兒童和青少年用量 - 開始時,鹽酸托莫西汀的每日總劑量應約為0.5 mg/kg,並且在3天的最低用量之後增加給藥量,至每日總目標劑量,約為1.2 mg/kg,可每日早晨單次服藥或早晨和傍晚平均分為2次服用。劑量超過1.2 mg/kg/日未顯示額外的益處。對兒童和青少年,每日最大劑量不應超過1.4 mg/kg或100 mg,選其中較小的一個劑量。
體重超過70公斤的兒童、青少年和成人用量 - 開始時,鹽酸托莫西汀每日總劑量應為40 mg,並且在3天的最低用量之後增加給藥量,至每日總目標劑量,約為80 mg,每日早晨單次服藥或早晨和傍晚平均分為2次服用。在繼續使用2-4周后,如仍未達到最佳療效,每日總劑量最大可以增加到100 mg,沒有數據支持在更高劑量下會增加療效。對體重超過70 kg的兒童和青少年以及成人,每日最大推薦總劑量為100 mg。
維持/長期治療 :還沒有對照試驗的資料提示ADHD患者應使用多長時間的鹽酸托莫西汀。不過通常認為,ADHD可能需要長期的藥物治療。如果醫生選擇長期使用鹽酸托莫西汀,應定期再評價長期治療對患者的有效性。鹽酸托莫西汀可與食物同服或分開服。尚未系統評價單次服藥劑量超過120 mg或每日總劑量超過150 mg的安全性。
肝功能損傷患者的劑量調節 - 伴肝功能不全(HI)的ADHD患者的劑量調節建議如下 :中度HI患者(Child-Pugh Class B),初始和目標劑量應降至常規用量(對不伴HI的患者)的50%。重度HI患者(Child-Pugh Class C),初始和目標劑量應降至常規用量的25%(見藥代動力學項下特殊人群)。
與強CYP 2D6抑制劑聯合使用的劑量調節 -服用強CYP 2D6抑制劑如帕羅西汀、氟西汀、奎尼丁,且體重不足70公斤的兒童和青少年,鹽酸托莫西汀的初始劑量應為0.5 mg/kg/日;只有當4周后症狀未見改善並且初始劑量有很好的耐受性時,才增加至通常的目標劑量1.2 mg/kg/日。服用強CYP 2D6抑制劑如帕羅西汀、氟西汀、奎尼丁,且體重超過70公斤的兒童、青少年和成年人,鹽酸托莫西汀的初始劑量應為40 mg/日,如果4周后症狀未見改善並且初始劑量有很好的耐受性,僅可增加至通常的目標劑量80 mg/日。停止治療時,不需逐漸減量。
不良反應:
鹽酸托莫西汀已經在2067名ADHD的兒童或青少年和270名ADHD的成人中進行了臨床研究。在ADHD臨床試驗中,169名患者的治療時間超過1年,526名患者的治療時間超過6個月。下表的數據和內容不適於在一般的醫療實踐中預測不良反應的發生率,因為患者的特點和其它因素與臨床試驗中的不同。同樣,所引用的不良反應的發生率也不能與使用其他治療方法、手段或眼瞼的臨床研究的數據相比較。所引用的數據為處方醫生估計藥物和非藥物因素對研究人群中不良事件發生率的相對影響提供一些基礎。兒童和青少年臨床試驗 :在兒童和青少年研究中,因不良時間中止治療的原因 - 在短期兒童和青少年安慰劑對照研究中,有3.5%(15/427)在托莫西汀治療組和1.4%(4/294)在安慰劑組患者因不良事件中止了治療。在所有的研究中(包括開放和長期研究),5%的強代謝(EM)患者和7%的弱代謝(PM)患者因為不良事件中止了研究。在接受鹽酸托莫西汀治療的患者中,造成1個以上的患者中止治療的原因為攻擊行為(0.5%,N=2),易激惹(0.5%,N=2),嗜睡(0.5%,N=2)和嘔吐(0.5%,N=2)。在兒童和青少年短期安慰劑對照試驗中常見的不良事件 - 下表中列出了在每日2次治療研究中,鹽酸托莫西汀組最常見(發生率2%或以上)但在安慰劑組不常見(在鹽酸托莫西汀治療組中的發生率高於安慰劑組)的不良事件,與每日1次治療的結果相近。除下表中列出的在每日2次和每日1次中均可見的不良事件,在接受鹽酸托莫西汀治療中,最常見的不良事件(發生率在5%或以上和至少為在安慰劑患者中發生率的2倍,在每日2次或每日1次劑量組) :消化不良、噁心、嘔吐、疲勞、食欲不振、眩暈和情緒波動。在兒童和青少年短期(9周以內,每日2次給藥)研究中,與接受鹽酸托莫西汀治療相關的常見不良事件 :鹽酸托莫西汀組N=340,安慰劑組N=207。胃腸道症狀 :上腹痛20%(安慰劑組為16%) ;便秘3%(安慰劑組為1%) ;消化不良4%(安慰劑組為2%) ; 嘔吐11%(安慰劑組為9%)。感染 :耳部感染3%(安慰劑組為1%) ;流感3%(安慰劑組為1%)。體檢 :體重減輕2%(安慰劑組為0%)。代謝和營養症狀 :食慾減退14%(安慰劑組為6%)。神經系統症狀 :頭暈(特別是眩暈)6%(安慰劑組為3%) ;頭痛27%(安慰劑組為25%) ;嗜睡7%(安慰劑組為5%)。精神症狀 :哭2%(安慰劑組為1%) ;煩躁8%(安慰劑組為5%) ;情緒波動2%(安慰劑組為0%)。呼吸、胸和縱隔症狀 :咳嗽11%(安慰劑組為7%) ;鼻液溢4%(安慰劑組為3%)。皮膚和皮下組織症狀 :皮炎4%(安慰劑組為1%)。這些事件至少由2%以上使用托莫西汀治療的患者報告,並且比用安慰劑者多。下列不良事件不符合這一標準,但與安慰劑組相比,托莫西汀組有更多患者報告這些不良事件,而且可能與托莫西汀治療有關 :厭食、血壓升高、早醒、興奮、瞳孔擴大、竇性心動過速、多淚。下列不良事在使用托莫西汀的患者中至少有2%的報告,並且相等於或少於安慰劑組 :關節痛、病毒所致的胃腸炎、失眠、咽喉痛、鼻充血、鼻咽炎、瘙癢、竇充血、上呼吸道感染。下列不良事件在PM患者的發生率至少2%,而且或是等於或是發生頻率相對於EM患者有統計學意義 :食慾下降(23%PM、16%EM) ;失眠(13%PM、7%EM) ;鎮靜狀態(4%PM、2%EM) ;抑鬱(6%PM、2%EM) ;震顫(4%PM,1%EM) ;早醒(3%PM、1%EM) ;瘙癢(2%PM、1%EM) ;瞳孔擴大(2%PM,1%EM)。成人臨床試驗 :成人短期安慰劑對照研究中,因不良事件中止治療的原因 - 在短期的安慰劑對照研究中,因不良事件中止治療的,在接受鹽酸托莫西汀治療的患者中有8.5%(23/270),安慰劑組有3.4%(9/266)。接受鹽酸托莫西汀治療的患者,造成1個以上的患者中止治療的原因為失眠(1.1%,N=3) ;胸痛(0.7%,N=2) ;心悸 (0.7%,N=2) ;尿瀦留(0.7%,N=2)。在成人短期安慰劑研究中常見的不良事件 - 下表中列出了與鹽酸托莫西汀治療相關的常見不良事件(發生率2%或以上),但在安慰劑組不常見(在鹽酸托莫西汀治療組中的發生率高於安慰劑治療組)的不良事件。在接受鹽酸托莫西汀治療中最常見的不良事件(發生率在5%或以上或至少為安慰劑組患者發生率的2倍):便秘、口乾、噁心、食慾下降、頭暈、失眠、性慾降低、射精障礙、無力、排尿不暢、和/或尿瀦留和/或排尿困難和痛經。在成人短期(達10周)研究中,與接受鹽酸托莫西汀治療相關的常見不良事件(:鹽酸托莫西汀組N=269 ;安慰劑組N=263) :心臟症狀 :心悸4%(安慰劑組為1%)。胃腸道症狀 :便秘10%(安慰劑組為4%) ;口乾21%(安慰劑組為6%) ;消化不良6%(安慰劑組為4%) ;腹脹2%(安慰劑組為1%) ;噁心12%(安慰劑組為5%)。全身症狀和給藥部位症狀 :疲勞和/或嗜睡7%(安慰劑組為4%) ;發熱3%(安慰劑組為2%) ;寒戰3%(安慰劑組為1%)。感染 :鼻竇炎6%(安慰劑組為4%)。體檢 :體重下降2%(安慰劑組為1%)。代謝和營養症狀 :食慾減退10%(安慰劑組為3%)。肌肉骨骼、結締組織和骨症狀 :肌痛3%(安慰劑組為2%)。神經系統症狀 :頭暈6%(安慰劑組為2%) ;頭痛17%(安慰劑組為17%) ;失眠和/或中段失眠16%(安慰劑組為8%) ;感覺異常4%(安慰劑組為2%) ;竇性頭痛3%(安慰劑組為1%) 。精神症狀 :多夢4%(安慰劑組為3%) ;性慾減退6%(安慰劑組為2%) ;睡眠障礙4%(安慰劑組為2%)。腎臟和泌尿系統症狀 :排尿不暢和/或尿瀦留和/或排尿困難8%(安慰劑組為0%)。生殖系統和乳房症狀 :痛經7%(安慰劑組為3%) ;射精失敗和/或射精障礙5%(安慰劑組為2%);勃起障礙7%(安慰劑組為1%);陽萎3%(安慰劑組為0%);月經延遲2%(安慰劑組為1%);月經紊亂3%(安慰劑組為2%);月經不規律2%(安慰劑組為0%);性高潮異常2%(安慰劑組為1%);前列腺炎3%(安慰劑組為0%)。皮膚和皮下組織症狀 :皮炎2%(安慰劑組為1%);多汗4%(安慰劑組為1%)。血管症狀 :潮熱3%(安慰劑組為1%)。以上事件至少由2%以上使用托莫西汀治療的患者報告,並且多於安慰劑組。以下不良事件不符合這一標準,但與安慰劑組相比,托莫西汀組有更多患者報告這些不良事件,且可能與托莫西汀治療有關 :早醒、末梢冷、心動過速。以下的不良事至少2%接受託莫西汀治療的患者有報告,並且相等於或少於安慰劑組 :上腹痛、關節痛、背痛、咳嗽、失眠、腹瀉、流感、興奮、鼻咽炎、咽喉痛、上呼吸道感染、嘔吐。有關生殖系統和乳房症狀,分別基於所有男性(鹽酸托莫西汀組,N=174 ;安慰劑組,N=172),或基於所有女性(鹽酸托莫西汀組,N=95;安慰劑組,N=91)。男性和女性的性功能障礙 - 托莫西汀在一些患者中引起性功能受損。性慾和性行為的改變、性滿意度在大多數研究中沒能夠得到很好的評價,因為患者和醫生不願意就以上問題進行討論。因此,引證在說明書中的對不愉快的性體驗和性行為發生率的評價可能會低於實際的發生率。以下列出的是在安慰劑對照研究中,接受鹽酸托莫西汀治療的至少有2%的成人患者報告的性方面不良事件發生率 :勃起障礙(僅男性)7%(安慰劑組為1%) ;陽萎(僅男性)3%(安慰劑組為0%) ;性高潮異常2%(安慰劑組為1%)。沒有對接受鹽酸托莫西汀治療出現性障礙進行充分的和規範的對照調查研究。儘管很難知道鹽酸托莫西汀用藥導致性功能障礙的明確的危險性,醫生應常規地調查這方面的可能的不良反應。以下列出上市後自發報告的不良事件/反應和其相應的報告率。心血管系統 - 極少(發生率<0.01%) :QT間期延長,暈厥。血管異常 - 很少見(<0.01%) :周圍血管不穩定性和/或雷諾氏現象(已有疾病新的發作或加劇)。
禁忌:
過敏 :鹽酸托莫西汀禁用於已知對托莫西汀或對該產品的其它成分過敏的患者 (見警告)。單胺氧化酶抑制劑(MAOI):鹽酸托莫西汀不應與MAOI合用,或在停用MAOI 兩周內使用。同樣,MAOI治療不應在停用鹽酸托莫西汀2周內開始。已有報導稱,其它影響腦內單胺濃度的藥物與MAOI合用可引起嚴重的、有時會致命的反應(包括高熱、強直、肌陣攣、自主神經系統功能不穩定,可能出現生命體徵的快速波動,以及精神狀態改變,包括可發展為譫妄和昏迷的極度激越)。有些病例表現出類似神經阻滯劑所致的惡性綜合徵的特點。這類反應可能在這些藥物同時使用或清洗期過短時發生。狹角性青光眼 :在臨床研究中,使用鹽酸托莫西汀與增加瞳孔擴大的危險有關,因此,本品不推薦在患有狹角性青光眼的患者中使用。
注意事項:
對血壓和心率的影響 - 因為鹽酸托莫西汀可使血壓和心率增高,因此,患高血壓、心動過速或心血管或腦血管的疾病患者應注意。在治療前、鹽酸托莫西汀劑量增加時和治療中應定期測量脈搏和血壓。在兒科安慰劑對照研究中,相對於安慰劑組,接受鹽酸托莫西汀治療的患者出現平均心率加快6次/分鐘。在停藥之前的最終研究觀察中,相對於安慰劑組0.5%(?04),3.6%(12/335)接受鹽酸托莫西汀治療的患者心率增快25次/分鐘,心率至少為110次/分鐘。沒有兒科病例超過1次出現心率增快至少25次/分鐘和心率至少在110次/分鐘。相對於安慰劑組的0.5%(?07),心動過速被認為是這些兒科患者的1.5%(5/340)的不良事件。平均的心率增快在強代謝(EM)患者為6.7次/分種,在弱代謝(PM)患者中為10.4次/分鐘。與安慰劑組相比,接受鹽酸托莫西汀治療的兒科患者的收縮壓和舒張壓平均增高1.5 mmHg。在停藥之前的最終研究觀察中,相對於安慰劑組的3.0%(6/197),6.8%(22/324)接受鹽酸托莫西汀的兒科患者具有高收縮壓。相對於安慰劑組的3.6%(7/197),高收縮壓在接受鹽酸托莫西汀治療的患者中有8.6%(28/324)為2次或更多。在停藥之前的最終研究觀察中,相對於安慰劑組0.5%(?00),接受鹽酸托莫西汀治療的兒科患者有2.8%(9/326)出現高舒張壓。出現2次或以上高舒張壓的,在安慰劑組為1.5%(3/200),接受鹽酸托莫西汀治療的患者為5.2%(17/326)。(高收縮壓和舒張壓值是依據超過95th美國國家高血壓評價工作組關於在兒童和青少年中高血壓控制中定義的按年齡、性別和身高百分率分層的百分率而定。)在成人的對照研究中,相對於安慰劑組,接受鹽酸托莫西汀治療的患者心率平均增快5次/分鐘。心動過速被認為是一種不良事件,在安慰劑組為0.8%(2/263),在托莫西汀治療組為3%(8/269)。相對於安慰劑組,接受鹽酸托莫西汀治療的成人患者收縮壓平均增高約3 mmHg,舒張壓平均增高約1 mmHg。在停藥之前的最終研究觀察中,安慰劑組有1.2%(3/256),接受鹽酸托莫西汀治療的患者中有1.9%(5/258)收縮壓≥150 mmHg ;安慰劑組有0.4%(?57),接受鹽酸托莫西汀治療的患者中有0.8%(2/257)舒張壓≥100 mmHg。沒有發現成人患者有高收縮壓或舒張壓超過1次。在使用鹽酸托莫西汀的患者中有出現直立性低血壓的報導。在短期兒童和青少年對照研究中,相對於安慰劑組有0.5%(?07),接受鹽酸托莫西汀治療的患者中有1.8%(6/340)出現體位性低血壓症狀。使用鹽酸托莫西汀應注意可能使患者出現低血壓。對排尿的影響 - 在成人ADHD對照研究中,相對於安慰劑組的0%(0/263),接受託莫西汀治療的患者中有3%(7/269)出現尿瀦留,3%(7/269)出現排尿不暢。因為尿瀦留有2名成人患者退出托莫西汀對照研究,而安慰劑組沒有。出現尿瀦留和排尿不暢認為與托莫西汀有潛在的關聯。對生長發育的影響 - 在幾個開放試驗中將受試者體重和身高的變化與標準值進行比較,從而總結出鹽酸托莫西汀膠囊對生長發育的長期影響。一般來說,在經過最初的9-12個月的治療之後,患者的體重和身高的增長落後於根據標準人群預計的值。當治療達3年時,體重的增長開始回彈,平均增長17.9公斤,比根據基線數據的預計值高0.5公斤。身高方面,在經過12個月的治療之後,身高的增長趨於穩定,治療達3年時,患者身高平均增長19.4厘米,比根據基線數據預計值低0.4厘米。(見下圖1)這種生長模式大致相同,與患者接受治療時的發育程度無關。尚未進入青春期的兒童患者(女孩8歲以下,男孩9歲以下)接受治療3年後體重平均增長2.1公斤,身高平均增長1.2厘米,低於預計值 ;已經處於青春期(女孩8-13歲,男孩9-14歲)或青春期後期(女孩13歲以上,男孩14歲以上)的兒童患者接受治療3年後體重和身高的平均增長值接近或超過預計值。對於快代謝和慢代謝的患者(EMs,PMs),生長發育的模式相似。接受治療2年後,慢代謝患者的體重和身高分別比預計值少2.4公斤和1.1厘米,快代謝患者的體重和身高分別比預計值少0.2公斤和0.4厘米。在短期對照試驗中(9周以內),接受鹽酸托莫西汀膠囊治療的患者體重平均減少0.4公斤,身高平均增長0.9厘米,而接受安慰劑的患者體重平均增長1.5公斤,身高平均增長1.1厘米。在1項固定劑量對照試驗中,對於對照組,0.5毫克/公斤/日劑量組,1.2毫克/公斤/日劑量組和1.8毫克/公斤/日劑量組,分別各有1.3%,7.1%,19.3%和29.1%的患者體重減少3.5%。在鹽酸托莫西汀膠囊的治療過程中必須對患者的生長發育進行監測。攻擊行為或敵意 - 在兒童和青少年的ADHD患者中容易觀察到攻擊行為或敵意,並且已經在臨床試驗和上市後旨在治療ADHD的一些用藥經歷中有所報導。儘管尚沒有明確的證據顯示鹽酸托莫西汀會導致攻擊行為或敵意,但在兒童和青少年的臨床試驗中,與安慰劑相比,用鹽酸托莫西汀後產生攻擊行為或敵意的發生率較大(總的風險比是1.33 - 沒有統計學差異)。應注意監察ADHD患者接受治療後其攻擊行為或敵意是否惡化。實驗室檢查 :不需要常規實驗室檢查。 CYP 2D6代謝 - 服用鹽酸托莫西汀後,相對於CYP 2D6強代謝(EM)者,弱代謝(PM)者的AUC會高10倍,最大血漿濃度會高5倍。大約7%的高加索人為PM。實驗室檢查能夠鑑定CYP 2D6PM。在PM的血漿水平與給予CYP 2D6強抑制劑後相近。在PM中高的血漿水平會導致服用鹽酸托莫西汀後的不良反應率較高(見不良反應)。
孕婦及哺乳期婦女用藥:
妊娠 :沒有充分的和規範的對照研究在孕婦中進行。鹽酸托莫西汀不應在妊娠期使用,除非潛在的對於胎兒的利益大於潛在的危險性。大鼠的分娩不受託莫西汀影響。目前尚不清楚鹽酸托莫西汀對人類分娩的影響。托莫西汀和/或其代謝產物在大鼠的乳汁中排泌。目前尚不清楚托莫西汀是否在人類的乳汁中排泌。哺乳期母親應慎用鹽酸托莫西汀。
兒童用藥:
任何人考慮在兒童或青少年中使用鹽酸托莫西汀膠囊,必須對其使用的風險和臨床的需要進行權衡(參見關於自殺觀念的警告項以及各種警告)。鹽酸托莫西汀對年齡小於6歲的兒科患者的安全性和療效尚未確定。尚未對鹽酸托莫西汀治療9周以上的療效和1年以上的安全性進行系統評價。在年輕大鼠中進行了托莫西汀對成長、神經行為和性發育影響的評價研究。管飼法,從大鼠出生後早期(10天大)貫穿至成年,給予托莫西汀1、10和50 mg/kg/日(以 mg/m 為單位計算,分別約為人最高劑量的0.2、2和8倍)。觀察到,陰道不閉合(所有劑量)和包皮分離(10和50 mg/kg)的輕度延遲,附睪重量和精子數輕度減少(10和50 mg/kg)和黃體的輕度減少(50 mg/kg),但不影響生育力和生殖行為。在50 mg/kg組出現切牙長出的輕度延遲。在15天大(雄性10和50 mg/kg,雌性50 mg/kg)和30天大(雌性50 mg/kg)出現運動活力的輕度增強,但在60天大沒有觀察到。對學習和記憶試驗沒有影響。這些發現對人類的意義還不知道。
老年用藥:
鹽酸托莫西汀在老年患者中的安全性和療效尚未確定。
藥物相互作用:
舒喘靈 - 給予正在系統給藥(口服或靜脈注射)舒喘靈(或其他β2 受體激動劑)的患者鹽酸托莫西汀需要注意,因為舒喘靈可能導致心率加快和血壓升高。舒喘靈(600 ug靜脈注射2小時以上)降低心率的增快和血壓。托莫西汀(60 mg每日2次服用5天)可加強這些作用,在聯合使用舒喘靈和托莫西汀的初期最明顯。 CYP 2D6活性和托莫西汀血漿濃度 - 托莫西汀主要通過CYP2D6途徑代謝為4-羥基托莫西汀。在EM中,CYP2D6抑制劑增高托莫西汀穩態濃度,使與在PM的表現相近。在EM中,當聯合使用CYP2D6抑制劑,如帕羅西汀、氟西汀和奎尼丁時,有必要調節鹽酸托莫西汀的劑量(見[注意事項]下藥物相互作用)。在體外研究中顯示,在PM中聯合使用細胞色素P450抑制劑不會提高托莫西汀的血漿濃度。 托莫西汀對P450酶的影響 - 托莫西汀不會產生具有臨床意義的對P450酶的抑制或削弱,包括CYP 1A2、CYP 3A、CYP 2D6和CYP 2C9。 CYP 2D6抑制劑 - 在EM中,選擇性的CYP 2D6抑制劑使穩態血漿濃度與PM相近。在個別聯合使用帕羅西汀或氟西汀的EM中。
藥物過量:
臨床試驗中鹽酸托莫西汀過量的例子有限,沒有因此造成死亡的病例報導。上市後有報導短期和長期過量服用鹽酸托莫西汀,沒有報導僅因為過量服用鹽酸托莫西汀導致死亡的病例。短期或長期過量服用鹽酸托莫西汀的症狀是嗜睡,激越,活動過度,行為異常和胃腸道系統症狀。與交感神經系統相關的症狀和體症(如:散瞳,心動過速,口乾)也有報導。藥物過量的處理 :保證周圍通風 ;用適當的指征顯示及其他支持措施監測心臟和生命體徵。服藥過量後短時間內建議洗胃。使用活性碳可以限制藥物吸收。由於托莫西汀蛋白結合率高,所以如用透析來處理藥物過量沒有很大用處。
臨床試驗:
在一項前瞻性、隨機的臨床試驗中,將228例注意缺陷障礙患兒隨機分為兩組,即鹽酸托莫西汀組184例和哌甲酯組44例,10周為1個療程,採用注意缺陷障礙4度評分法評價兩種藥物的療效。結果,鹽酸托莫西汀組治療前評分為(39.4±8.5)分,用藥後為(20.0±13.9)分;而哌甲酯組用藥前評分為(37.6±9.7)分,用藥後為(19.8±16.6)分,兩組的療效差異無顯著性(P>0.05)。因不良反應而中斷用藥的患者鹽酸托莫西汀組為5.4%,而哌甲酯組為11.4%。提示本品對小兒多動症的療效與哌甲酯相當,但具有較高的安全性和耐受性。
藥理毒理:
現代研究認為,小兒多動症發病機制是因中樞兒茶酚胺類神經遞質多巴胺(DA)和去甲腎上腺素(NA)代謝障礙造成的輕度腦功能缺陷。鹽酸托莫西汀治療小兒多動症的準確機制尚不清楚,目前認為本品的治療作用與其他選擇性抑制突觸前胺泵對NA的再攝取效應有關,能增強NA的翻轉效應,從而改善小兒多動症的症狀,間接促進認識的完成及注意力的集中。
藥代動力學:
本品口服吸收迅速,血藥濃度達峰時間為1~2小時。成人高脂飲食試驗表明,食物不會影響本品的絕對生物利用度,但可以降低吸收速度,使峰濃度(C)下降約37%,達峰時間(t)延遲約3小時。本品在治療劑量時,血漿蛋白結合率約為98%,主要與血漿蛋白結合;表觀分布容積(Vc)為0.85升/千克,表明其主要分布於體液中。體內藥物經過肝微粒體細胞色素酶P4502D6(CYP2D6)代謝生成4-羥基托莫西汀,血藥濃度約為原藥的1%。代謝產物4-羥基托莫西汀的藥理活性與原藥相似。本品在飯前或飯後服用,平均血漿清除率(K)為5.83毫升/分,半衰期(t)為5.2小時。口服給藥後僅3%以原形藥物排除體外,大於80%的藥物以葡萄糖苷的形式經腎隨尿液排泄,約17%的藥物經消化道隨糞便排泄。
貯藏:
室溫保存,可在15至30℃範圍內變化。
包裝:
鋁塑泡罩包裝,7粒/盒
有效期:
24個月
妊娠分級
FDA妊娠分級:C