簡介
金屬EDTA螯合物螯合物通常比一般配合物要穩定,其結構中經常具有的五或六元環結構更增強了穩定性。正因為這樣,螯合物的穩定常數都非常高,許多螯合反應都是定量進行的,可以用來滴定。使用螯合物還可以掩蔽金屬離子。可形成螯合物的配體叫螯合劑。常見的螯合劑如下:乙二胺(en),二齒 2,2'-聯吡啶(bipy),二齒 1,10-鄰二氮雜菲(phen),二齒 草酸根(ox),二齒 乙二胺四乙酸(EDTA),六齒 值得一提的是EDTA。它能提供2個氮原子和4個羧基氧原子與金屬配合,可以用1個分子把需要6配位的鈣離子緊緊包裹起來,生成極穩定的產物。其化學結構表示如下:(HOOCCH2)2NCH2CH2N(CH2COOH)2 螯合物在工業中用來除去金屬雜質,如水的軟化、去除有毒的重金屬離子等。一些生命必須的物質是螯合物,如血紅蛋白和葉綠素中卟啉環上的4個氮原子把金屬原子(血紅蛋白含Fe2+,葉綠素含Mg2+)固定在環中心。
其他信息
螯合劑是多齒的配位劑,多齒的意思就是一個配位劑可以與中心離子形成兩個及以上的配位鍵。常見的螯原子主要是N,O和S。具體的例子附在圖片裡面了。例子是一個NN型螯合物。
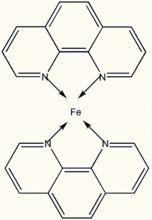 螯合反應圖示
螯合反應圖示