前言
本標準代替GB/T5009.15-2003《食品中鎘的測定》。
本標準與GB/T5009.15-2003相比,主要變化如下:
———標準名稱修改為“食品安全國家標準 食品中鎘的測定”;
———刪除第二法原子吸收光譜法、第三法比色法、第四法原子螢光法。
正文
範圍
本標準規定了各類食品中鎘的石墨爐原子吸收光譜測定方法。
本標準適用於各類食品中鎘的測定。
原理
試樣經灰化或酸消解後,注入一定量樣品消化液於原子吸收分光光度計石墨爐中,電熱原子化後吸收228.8 nm共振線,在一定濃度範圍內,其吸光度值與鎘含量成正比,採用標準曲線法定量。
試劑和材料
注1:除非另有說明,本方法所用試劑均為分析純,水為GB/T6682規定的二級水。
注2:所用玻璃儀器均需以硝酸溶液(1+4)浸泡24 h以上,用水反覆沖洗,最後用去離子水沖洗乾淨。
試劑
硝酸(HNO):優級純。
鹽酸(HCl):優級純。
高氯酸(HClO):優級純。
過氧化氫(HO, 30%)。
磷酸二氫銨(NHHPO)。
試劑配製
硝酸溶液(1%):取10.0 mL硝酸加入100 mL水中,稀釋至1000 mL。
鹽酸溶液(1+1):取50 mL鹽酸慢慢加入50 mL水中。
硝酸-高氯酸混合溶液(9+1),取9份硝酸與1份高氯酸混合。
磷酸二氫銨溶液(10 g/L):稱取10.0 g磷酸二氫銨,用100 mL硝酸溶液(1%)溶解後定量移入1000 mL容量瓶,用硝酸溶液(1%)定容至刻度。
標準品
金屬鎘(Cd)標準品,純度為99.99%或經國家認證並授予標準物質證書的標準物質。
標準溶液配製
鎘標準儲備液(1000 mg/L):準確稱取1 g金屬鎘標準品(精確至0.0001 g)於小燒杯中,分次加20 mL鹽酸溶液(1+1)溶解,加2滴硝酸,移入1000 mL容量瓶中,用水定容至刻度,混勻;或購買經國家認證並授予標準物質證書的標準物質。
鎘標準使用液(100 ng/mL):吸取鎘標準儲備液10.0 mL於100 mL容量瓶中,用硝酸溶液(1%)定容至刻度,如此經多次稀釋成每毫升含100.0 ng鎘的標準使用液。
鎘標準曲線工作液:準確吸取鎘標準使用液0 mL、0.50 mL、1.0 mL、1.5 mL、2.0 mL、3.0 mL於100 mL容量瓶中,用硝酸溶液(1%)定容至刻度,即得到含鎘量分別為0 ng/mL、0.50 ng/mL、1.0 ng/mL、1.5 ng/mL、2.0 ng/mL、3.0 ng/mL的標準系列溶液。
儀器和設備
原子吸收分光光度計,附石墨爐。
鎘空心陰極燈。
電子天平:感量為0.1 mg和1 mg。
可調溫式電熱板、可調溫式電爐。
馬弗爐。
恆溫乾燥箱。
壓力消解器、壓力消解罐。
微波消解系統:配聚四氟乙烯或其他合適的壓力罐。
分析步驟
試樣製備
乾試樣:糧食、豆類,去除雜質;堅果類去雜質、去殼;磨碎成均勻的樣品,顆粒度不大於0.425 mm。儲於潔淨的塑膠瓶中,並標明標記,於室溫下或按樣品保存條件下保存備用。
鮮(濕)試樣:蔬菜、水果、肉類、魚類及蛋類等,用食品加工機打成勻漿或碾磨成勻漿,儲於潔淨的塑膠瓶中,並標明標記,於-16℃~-18℃冰櫃中保存備用。
液態試樣:按樣品保存條件保存備用。含氣樣品使用前應除氣。
試樣消解
可根據實驗室條件選用以下任何一種方法消解,稱量時應保證樣品的均勻性:
a)壓力消解罐消解法:稱取乾試樣0.3 g~0.5 g(精確至0.0001 g)、鮮(濕)試樣1 g~2 g(精確到0.001 g)於聚四氟乙烯內罐,加硝酸5 mL浸泡過夜。再加過氧化氫溶液(30%)2 mL~3 mL(總量不能超過罐容積的1/3)。蓋好內蓋,旋緊不鏽鋼外套,放入恆溫乾燥箱,120℃~160℃保持4 h~6 h,在箱內自然冷卻至室溫,打開後加熱趕酸至近乾,將消化液洗入10 mL或25 mL容量瓶中,用少量硝酸溶液(1%)洗滌內罐和內蓋2次,洗液合併於容量瓶中並用硝酸溶液(1%)定容至刻度,混勻備用;同時做試劑空白試驗。
b)微波消解:稱取乾試樣0.3 g~0.5 g(精確至0.0001 g)、鮮(濕)試樣1 g~2 g(精確到0.001 g)置於微波消解罐中,加5 mL硝酸和2 mL過氧化氫。微波消化程式可以根據儀器型號調至最佳條件。消解完畢,待消解罐冷卻後打開,消化液呈無色或淡黃色,加熱趕酸至近乾,用少量硝酸溶液(1%)沖洗消解罐3次,將溶液轉移至10 mL或25 mL容量瓶中,並用硝酸溶液(1%)定容至刻度,混勻備用;同時做試劑空白試驗。
c) 濕式消解法:稱取乾試樣0.3 g~0.5 g(精確至0.0001 g)、鮮(濕)試樣1 g~2 g(精確到0.001 g)於錐形瓶中,放數粒玻璃珠,加10 mL硝酸高氯酸混合溶液(9+1),加蓋浸泡過夜,加一小漏斗在電熱板上消化,若變棕黑色,再加硝酸,直至冒白煙,消化液呈無色透明或略帶微黃色,放冷後將消化液洗入10 mL~25 mL容量瓶中,用少量硝酸溶液(1%)洗滌錐形瓶3次,洗液合併於容量瓶中並用硝酸溶液(1%)定容至刻度,混勻備用;同時做試劑空白試驗。
d)乾法灰化:稱取0.3 g~0.5 g(精確至0.0001 g)、鮮(濕)試樣1 g~2 g(精確到0.001 g)、液態試樣1 g~2 g(精確到0.001 g)於瓷坩堝中,先小火在可調式電爐上炭化至無煙,移入馬弗爐500℃灰化6 h~8 h,冷卻。若個別試樣灰化不徹底,加1 mL混合酸在可調式電爐上小火加熱,將混合酸蒸乾後,再轉入馬弗爐中500℃繼續灰化1 h~2 h,直至試樣消化完全,呈灰白色或淺灰色。放冷,用硝酸溶液(1%)將灰分溶解,將試樣消化液移入10 mL或25 mL容量瓶中,用少量硝酸溶液(1%)洗滌瓷坩堝3次,洗液合併於容量瓶中並用硝酸溶液(1%)定容至刻度,混勻備用;同時做試劑空白試驗。
註:實驗要在通風良好的通風櫥內進行。對含油脂的樣品,儘量避免用濕式消解法消化,最好採用乾法消化,如果必須採用濕式消解法消化,樣品的取樣量最大不能超過1 g。
儀器參考條件
根據所用儀器型號將儀器調至最佳狀態。原子吸收分光光度計(附石墨爐及鎘空心陰極燈)測定參考條件如下:
———波長228.8 nm,狹縫0.2 nm~1.0 nm,燈電流2 mA~10 mA,乾燥溫度105℃,乾燥時間20 s;
———灰化溫度400℃~700℃,灰化時間20 s~40 s;
———原子化溫度1300℃~2300℃,原子化時間3 s~5 s;
———背景校正為氘燈或塞曼效應。
標準曲線的製作
將標準曲線工作液按濃度由低到高的順序各取20 μL注入石墨爐,測其吸光度值,以標準曲線工作液的濃度為橫坐標,相應的吸光度值為縱坐標,繪製標準曲線並求出吸光度值與濃度關係的一元線性回歸方程。
標準系列溶液應不少於5個點的不同濃度的鎘標準溶液,相關係數不應小於0.995。如果有自動進樣裝置,也可用程式稀釋來配製標準系列。
試樣溶液的測定
於測定標準曲線工作液相同的實驗條件下,吸取樣品消化液20 μL(可根據使用儀器選擇最佳進樣量),注入石墨爐,測其吸光度值。代入標準系列的一元線性回歸方程中求樣品消化液中鎘的含量,平行測定次數不少於兩次。若測定結果超出標準曲線範圍,用硝酸溶液(1%)稀釋後再行測定。
基體改進劑的使用
對有干擾的試樣,和樣品消化液一起注入石墨爐5 μL基體改進劑磷酸二氫銨溶液(10 g/L),繪製標準曲線時也要加入與試樣測定時等量的基體改進劑。
分析結果的表述
試樣中鎘含量按式(1)進行計算:
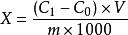 食品安全國家標準食品中鎘的測定
食品安全國家標準食品中鎘的測定式中:
X ———試樣中鎘含量,單位為毫克每千克或毫克每升(mg/kg或mg/L);
C ———試樣消化液中鎘含量,單位為納克每毫升(ng/mL);
C ———空白液中鎘含量,單位為納克每毫升(ng/mL);
V ———試樣消化液定容總體積,單位為毫升(mL);
m ———試樣質量或體積,單位為克或毫升(g或mL);
1000———換算係數。
以重複性條件下獲得的兩次獨立測定結果的算術平均值表示,結果保留兩位有效數字。
精密度
在重複性條件下獲得的兩次獨立測定結果的絕對差值不得超過算術平均值的20%。
其他
方法檢出限為0.001mg/kg,定量限為0.003mg/kg。

