套用領域
在動物界,除了一些特殊的魚類,一般沒有專門感受外界電刺激或電場改變的器官或感受細胞,但在體內有很多細胞,如神經細胞和各種肌細胞,在它們的細胞膜中卻具有多種電壓門控通道蛋白質,它們可由於同一細胞相鄰的膜兩側出現的電位改變而再現通道的開放,並由於隨之出現的跨膜離子流而出現這些通道所在膜的特有的跨膜電位改變。例如,前述的終板膜由Ach門控通道開放而出現終板電位時,這個電位改變可使相鄰的肌細胞膜中存在的電壓門控式Na+通道和K+通道相繼激活(即通道開放),出現肌細胞的所謂動作電位;當動作電位在神經纖維膜和肌細胞膜上傳導時,也是由於一些電壓門控通道被鄰近已興奮的膜的電變化所激活,結果使這些通道所在的膜也相繼出現特有的電變化。由此可見,電壓門控通道所起的功能,也是一種跨膜信號轉換,只不過它們接受的外來刺激信號是電位變化,經過電壓門控通道的開閉,再引起細胞膜出現新的電變化或其他細胞內功能變化,後者在Ca2+通道打開引起膜外Ca2+內流時甚為多見。
科研成果
 電壓門控通道
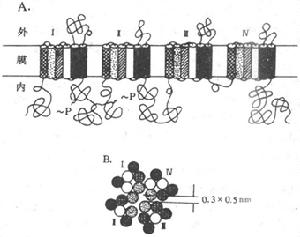
電壓門控通道根據對Na+、K+、Ca2+三種離子的電壓門控通道蛋白質進行的分子結構分析,發現它們一級結構中的胺基酸排列有相當大的同源性,說明它們屬於同一蛋白質家族,與之有關的mRNA在進化上由同一個遠祖基因演化而來。圖2-8是與體內動作電位(見後)產生至關重要的Na+通道在膜內結構的模式圖,它主要由一個較大的α-亞單位組成,分子量約260kd;有時還另有一個或兩個小分子量的亞單位,分別稱為β1和β2。但Na+通道的主要功能看來只靠α-亞單位即可完成。這個較長的α-單位肽鏈中包含了4個結構類似的結構域(domain,每個結構域大致相當於上述Ach門控通道中的一個亞單位,但結構域之間由肽鏈相連,是一個完整的肽鏈,應由一個mRNA編碼和合成),而每個結構域中又各有6個由疏水性胺基酸組成的跨膜α-螺旋段(圖示2-8,A);這4 個結構域及其所包含的疏水α-螺旋,在膜中包繞成一個通道樣結構(圖2-8,B)。現已證明,每個結構域中的第4個跨膜α-螺旋在胺基酸序列上有特點,即每隔兩個疏水性胺基酸,就再現一個帶正電荷的精氨酸或賴氨酸;這些α-螺旋由於自身的帶電性質,在它們所在膜的跨膜電位有改變時會產生位移,因而被認為是該通道結構中感受外來信號的特異結構,由此再誘發通道“閘門”的開放;還有實驗提示,每個結構域中的第2、第3個α-螺旋構成了該通道水相孔道的“內壁”;據測算,水相孔道內徑最窄處橫斷面積約為0.3×0.5nm差不多剛能通過一個水化的Na+