定義
膠團結構式是用來表示膠團結構的化學式寫法,一個膠團由內到外分為三層:膠粒、吸附層和擴散層,核和吸附層組成膠粒,膠粒和擴散層組成膠團。
例如經過FeCl水解出的Fe(OH)形成過飽和狀態,在另一過量反應物作為穩定劑,形成溶膠。
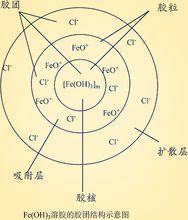
例如Fe(OH)溶膠的膠團結構和膠團結構式,分別如下圖所示:
 膠團結構式
膠團結構式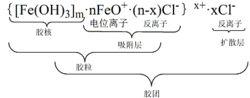 膠團結構式
膠團結構式其中m為Fe(OH)3的分子數,約10 ;n為電位離子數目,m>n;x為擴散層反離子數目;n-x為吸附層中反離子數目。
與之類似,推廣到一般的膠團結構式,約定俗成膠粒的分子數為m,而n作為電位離子(反離子)的數目,而且吸附的離子較少,所以m>n,而擴散層的反離子的數目為x,吸附層中反離子數目為n-x,整個膠團呈現電中性。
但電位離子的數目可為n的倍數(反離子的價數),吸附層中反離子數目為n-x的倍數(電位離子的價數)。例如SiO溶膠在水中生成HSiO。
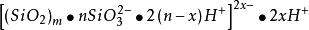 膠團結構式
膠團結構式性質
根據離子選擇吸附的原理,吸附劑會從電解質溶液中選擇性吸附與其組成有關的離子,溶膠具有很大表面能的膠核充當吸附劑,Fe(OH)膠核會從溶液里吸附與其組成相關FeO 離子作為電位離子,而與其組成不相關的Cl 則作為反離子。
 膠團結構式
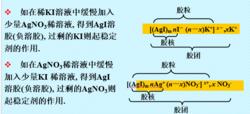
膠團結構式有時溶液中可能存在兩種或以上的離子與膠核結構的組成相關,例如
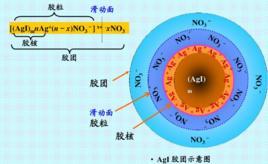
在AgNO3溶液和KI溶液製備AgI溶膠時,需要注意過量的問題,哪一個過量即作為電位離子,而與膠核結構無關的離子作為反離子。
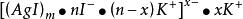 膠團結構式
膠團結構式過量的KI溶液:
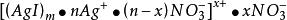 膠團結構式
膠團結構式過量的AgNO3溶液:
可以注意到電位離子的符號始終是和膠粒的符號一致的,這也符合膠團結構的性質。