概述
 細胞修復療法
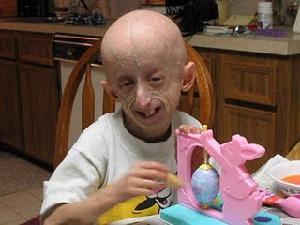
細胞修復療法這項為期18個月,由英國杜倫大學領導的研究的首批結果已經在《人類分子遺傳》雜誌發表。研究者對一組患有核纖層蛋白病的病人進行了觀察,這是一種遺傳性退行性疾病,一般認為是由LMNA基因異常引起的一組人類遺傳病。其中最嚴重的情況包括發生早年衰老綜合症(HGPS),這是一種非常嚴重的疾病,可以導致兒童早衰。
試驗
來自杜倫大學和博洛尼亞大學的研究者套用試管模型以及分子成像技術對細胞內氧化應激水平和DNA損傷進行觀察。氧化應激和人體的解毒和自我修復機制直接相關。當細胞處於氧化應激狀態時,一種被稱為活性氧自由基(ROS)的高活性分子的水平將急劇上升。這將導致對細胞結構和DNA的重大損害,而這正是人體衰老和早衰的發生機理。
研究小組對數千例病患進行了觀察,並了解他們在服用一種被廣泛使用的藥物N-乙醯-半胱氨酸(NAC)之後的細胞損傷情況。他們發現這種藥物儘管不能影響細胞應激水平,但是卻能相當有效地控制自由基水平以及由此產生的DNA損傷。而對於細胞應激水平,現有的很多藥物就能進行很好的控制。因此研究人員發現如果綜合NAC和其他傳統藥物一併給藥,將有可能改善患有早衰症兒童的狀況。
克里斯·哈特利森(Chris Hutchison)是杜漢大學生物物理學院教授,他說:“在患有早衰症的兒童身上我們能觀察到由於DNA雙鏈結構損傷導致的細胞發育異常。我們使用NAC和其他藥物聯合治療可以對抗這種損傷。”
他說:“LMNA基因的變異還可以導致更多其它病症,包括肌肉萎縮症。我們已經發現這種DNA損傷是可以被控制的,我們的發現將是重要的一步,將幫助那些不幸患有早衰症的兒童以及器官衰老的老年人改善健康狀況。”
不過研究者也承認他們目前的發現仍處在早期階段,仍需要更多的測試和臨床試驗才能真正開發出一種行之有效的藥物療法。哈特利森教授說:“我們正採取審慎的步驟去觀察患有早衰症的病人,並嘗試了解是否有某種可以適用於更廣泛範圍的模型。能夠幫助這些孩子提高健康水平並延長他們的生命真是一件讓人高興的事,並且除此之外我們還能通過這一發現幫助改善世界各地許多老年人的健康水平。”
他說:“這一研究目前還處於非常早期的階段,不過它已經顯示出其巨大的潛力,有望幫助人們過上更加舒適的生活,減少人們的痛苦,讓老人們再年過70或80之後能安享晚年。”
早年衰老綜合症
早年衰老綜合症是一種非常罕見的致命基因疾病,其症狀是兒童表現出加速衰老。根據文獻報導,全世界這一疾病的發病率約為每4~800萬名嬰兒中會出現1例。其發病率在不同性別,不同民族人群中幾乎相同。儘管嬰兒在出生時看不出任何異樣,但是在18~24個月左右,嬰兒便開始表現出明顯的一系列加速衰老跡象。
症狀
早衰症的具體表現包括生長停滯,身體脂肪流失,掉發,皮膚老化,關節硬化,髖關節脫位,動脈硬化,心血管疾病和中風等等。並且來自不同種族的兒童都表現出極其相似的症狀。一般患者最終會因心臟病去世,患者死亡的平均年齡約為13歲,最早8歲,晚的21歲。
進展
萊斯利·戈登(Leslie Gordon)博士是早衰症研究基金會藥物主管,他說:“哈特利森教授教授的研究不僅確認了早衰症的細胞損傷機理,還未可能的治療方案指明了道路。這些進展將最終幫助醫學界開發出治療的方法並幫助那些患有早衰症的患兒。”
展望
這一研究也將為未來的研究提供一個基準模型,幫助醫師們找到針對個體的藥物劑量和療法,從而改善用藥者的健康水平。
2014年小兒腦癱治療最新進展
小兒腦癱從古至今是可對患者造成終生影響的中樞系統損傷類疾病,而隨著近年來醫學水平的提高,腦癱治療也有了新的進展,從最初的藥物治療、手術治療、康復訓練,到如今的生物細胞免疫技術,對於腦癱患者都可起到治療的作用。
在各國學者的努力下,半個多世紀以來腦性癱瘓的治療有了大的發展,基本走上了以功能訓練治療為主導的全面綜合治療的軌道。以軀體療法為基礎,進行作業,語言,教育,心理,視、聽覺,交流,日常生活活動能力,社會活動能力,矯形器及支具,以及外科手術等綜合治療,顯著改善了腦性癱瘓的病情和預後,甚至在某些輕症患者可達到正常化。
近年來,隨著生物治療和再生醫學技術的進步,細胞治療可顯著修復腦性癱瘓小兒中樞神經系統損傷的方法則為本病的根本性治療康復提供了新的治療思路和途徑。
