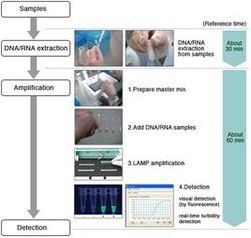
辨析
注意等溫過程和絕熱過程的區別,即等溫過程是過程中溫度保持不變,可能有吸熱或放熱,絕熱過程是過程中沒有吸放熱,但溫度可能變化,所以系統溫度的改變並不標誌系統有無熱的得失,有熱量得失的過程可以是恆溫過程,也可以是非恆溫過程。
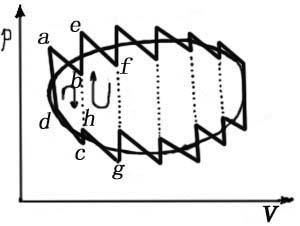 等溫過程
等溫過程例證
等溫過程例如,與恆溫箱接觸的一個氣筒,可用一活塞對它緩慢地壓縮,所做的功表現為流進容器內使氣體的溫度保持不變的能量。蓄電池在室溫下緩慢充電和放電,都是近似的等溫過程。又如,在101.325kpa,273.15K下凍的熔化成水是等溫,恆壓的可逆相變過程。對一定質量理想氣體等溫可逆過程的特徵是氣體壓強P和體積V的乘積不變,PV=恆量。理想氣體的內能僅僅是溫度的函式,所以過程中內能不變。
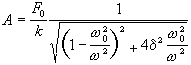 等溫過程
等溫過程理想氣體經等溫過程由狀態I(p1,V1)到狀態 Ⅱ(p2,V2)時系統所做的功
v為氣體的摩爾數,T為氣體的熱力學溫度(見熱力學溫標),R為摩爾氣體常數。理想氣體的內能僅僅是溫度的函式,所以等溫過程中內能的變化為零。由熱力學第一定律得出,理想氣體在等溫過程中能量轉換的特點是Q=A,即系統吸收的熱量等於系統對外界所做的功。
等溫過程是熱力學中一種重要過程。卡諾循環就是由兩個等溫過程和兩個絕熱過程組成的。物質三態的可逆轉變也是在等溫條件下進行的。