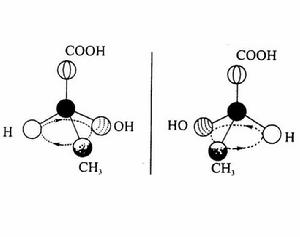
定義
分子構造式相同但分子中原子或基團在空間的排布不同而產生的同分異構體。產生立體異構的原因是由於分子中原子或原子團在空間的排列方式不同。
分類
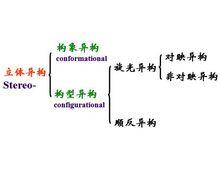 立體異構的分類
立體異構的分類立體異構可分為構型異構和構象異構,其中構型異構又可分為旋光異構(包括對映異構和非對映異構)和順反異構(或稱幾何異構)。
構型異構
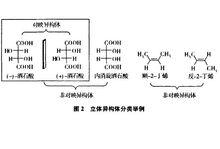 立體異構分類舉例
立體異構分類舉例構型異構是原子在大分子中不同空間排列所產生的異構現象,可分為旋光異構(包括對映異構和非對映異構)和順反異構(或稱幾何異構)。
(1)順反異構
兩者的分子式相同,原子或原子團的排列順序也相同,但分子中原子或原子團在空間的排布不同,即構型不同。這樣的立體異構稱為順反異構(或幾何異構)。通常將相同或相似的基團處於雙鍵同側的稱為順式(cis)構型;處於異側的則稱為反式(trans)構型。
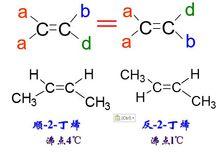 順反異構及舉例
順反異構及舉例順反異構產生的條件:具有雙鍵的化合物——由於雙鍵不能自由旋轉,當雙鍵連有不同的原子或基團時,就會出現兩種不同的空間排布方式,從而產生順反異構體。環狀化合物——把碳環近似的看成一個平面,連在環碳上的原子或基團就有在環平面的上下之分,從而產生順反異構現象。另外,每個不能自由旋轉的碳原子均連有2個不相同的原子或原子團。
順反異構體在物理性質、化學性質、生理活性上均存在一定差異。
(2)旋光異構
不對稱分子中原子或原子團在空間的不同排布,對平面偏振光的偏振面發生不同影響的異構現象,稱為旋光異構現象(optical isomerism),它所產生的異構體,稱為旋光異構體(optical antipodes)。
產生旋光異構現象的原因:任何一個不能和它的鏡像完全重疊的分子稱為手性分子。所謂手性,就是指實物與鏡像對映而不能完全重疊的特性,就如同左手與右手的關係一樣。
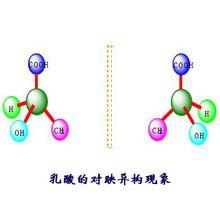 乳酸的對映異構現象
乳酸的對映異構現象①對映異構現象:互為實物與鏡像關係,但又不能完全重合的異構體,簡稱對映體;產生對映體的現象稱為對映異構現象。
對映異構體都有旋光性,其中一個是左旋的,一個是右旋的。兩個異構體之間的關係就如同一個物體的立體結構在照鏡子,這個立體結構和它在鏡子中的像互為對映異構體。物質產生旋光性的根本原因是分子的手性,即任何一個具有旋光性的分子必定是手性分子。手性分子通常必定產生旋光性,但也有極少數手性分子沒有或旋光活性很小,或者在某些波長的光段不表現出旋光性。
②非對映異構:兩個結構相同的分子,由於具有構型不同的不對稱原子,彼此不呈實物與鏡像的關係。非對映異構體的旋光性不同,熔點、沸點、溶解度、密度、折射率等物理性質也很不同。其化學性質雖然相似,但也不完全相同。
非對映異構體是由已含有一個手性中心的分子產生第二個手性中心時的必然產物。與對映體的生成不同,由於第一個手性中心的影響,所得到的兩個非對映異構體的數量並不相同。這就是不對稱合成的基礎。
構象異構
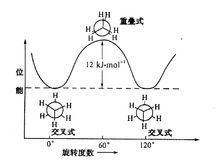 乙烷的幾種構象異構的能量曲線
乙烷的幾種構象異構的能量曲線構象是指由於碳碳單鍵的旋轉或扭曲(鍵不斷開)而引起分子中原子或原子團在空間的不同排列形式;因單鍵的旋轉或扭曲而產生的異構現象稱為構象異構現象,其對應的異構體稱為構象異構體。以乙烷為例,乙烷分子的兩個甲基以單鍵相連,如使一個甲基不動,另一個甲基圍繞碳碳單鍵而轉動,則兩個甲基上連線的氫原子在空間排列的方式將不斷改變,得到無數不同的空間的排列方式,這就是構象。
構型異構和構象異構的區別
(1)構型異構體可以互相分離,而構象異構體暫時還不能用化學方法把它們分離開來;
(2)構型異構體的互相轉變要經過化學反應,涉及化學鍵的斷裂和形成,而構象異構體的互相轉變不涉及化學鍵的斷裂和形成,僅僅通過鍵的旋轉,一般在室溫下就可以完成。