簡介
分子的正負電荷中心在無電場時是重合的,沒有固定的電偶極矩, 如氫氣(H)、高氯酸(HCl),二氧化碳(CO),氮氣(N),氧氣(O)、甲烷(CH)、聚丙乙烯、石蠟等。
 無極分子
無極分子電介質
定義
所謂電介質,就是通常所說的由大量電中性的分子組成的絕緣體。
在靜電場中平衡時:
1.內部電場強度不為零;
2.電介質表面出現極化電荷。
電介質出現極化電荷的現象,稱為電介質極化。
若把電介質放入靜電場中,電介質原子中的電子和原子核在電場力的作用下,在原子範圍內作微觀的相對位移。在外電場中電介質要受到電場的影響,同時也影響外電場。
分類
電介質可分為無極分子和有極分子。
無極分子和有極分子的區別
有極分子:分子的正負電荷中心在無電場時不重合的,有固定的電偶極矩, 如HO、HCl、 CO、SO、環氧樹脂、陶瓷等。
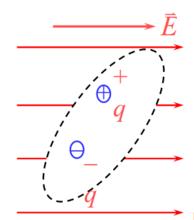 無極分子
無極分子有極分子的等效電偶極矩:
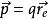 無極分子
無極分子整個電介質可以看成是無數的點偶極子的聚集體。雖然每個分子的等效點偶極矩不為零,但不管從電介質整體來看,還是從電解質的某一小體積來看,電解質是呈中性的。
 無極分子
無極分子無極分子:分子的正電荷中心與負電荷中心重合。
 無極分子
無極分子無極分子的等效電偶極矩:
 無極分子
無極分子無極分子電介質整體也是呈中性的。
電介質的極化
無極分子的位移極化
加上外電場後,在電場力作用下電介質分子的正負電荷中心不再重合,形成一個電偶極子,它們的等效電偶極矩P的方向都沿著電場的方向。
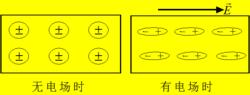 無極分子
無極分子電介質的兩個和外電場強度 相垂直的表面層里,將分別出現正電荷和負電荷。這些電荷不能離開介質,也不能在電介質中自有移動,我們稱之為極化電荷。這種在外電場作用下,在電介質中出現極化電荷的現象叫做電介質的極化。
由於無極分子的極化在於正、負電荷中心的相對位移,所以常叫做位移極化。
有極分子的取向極化
無外電場時,有極分子電偶極矩取向不同,整個介質不帶電。
在外電場中有極分子的固有電矩要受到一個力矩作用,電矩方向轉向和外電場方向趨於一致。
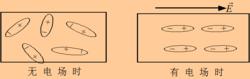 無極分子
無極分子有極分子的極化就是等效電偶極子轉向外電場的方向,所以叫做取向極化。
一般來說,分子在取向極化的同時還會產生位移極化,但是,對於有極分子電介質來說,在靜電場作用下,取向極化的效應比位移極化的效應強得多,所以有極分子的極化機理是取向極化。
上面從分子的結構出發,說明了兩類不同的電介質的極化過程,這兩類電介質極化的微觀過程雖然不同,但巨觀的效果卻是相同的,都是在電介質的兩個相對表面上出現了異號的極化電荷,在電介質內部有沿電場方向的電偶極矩。
無極分子之間的色散力
組成物質的分子可分為有極分子和無極分子。有極分子中,正負電荷的“中心”不集中在一點,因此形成一對距離很近的等值異號電荷所構成的等效電偶極子,其固有的電偶極矩為p=ql,電偶極子所產生的電場完全由它們的電偶極矩p決定。電偶極子在外電場中所受到的作用力也決定於它的電偶極矩。無極分子中,正負電荷的“中心”集中在一點,因此,分子的電偶極矩為零,對外也不產生電場。在有外電場的情況下,無論是有極分子或是無極分子,都會產生電極化現象,並存在電偶極矩之間的相互作用力。
對無極分子及惰性氣體而言,原子結晶體的結合力為共價鍵,共價鍵是決定物質分子化學性質的主要因素。分子晶體的結合力是范德瓦耳斯力,對無極分子來說就是色散力,按照倫敦提出的范德瓦耳斯力的量子理論,無極分子的電子云分布是球形對稱的,固有電矩為零。因此,它們之間的相互作用能亦為零。這徉無極分子之間似乎就不存在什麼作用,但實際不然,例如室溫下漠是液體,碘、蔡是固體,H、0、N等無極分子在低溫下也會被液化或固化,這些物質能維持某種聚集狀態,說明無極分子之間存在著一種相互作用力,這種力就是色散力。
雖然無極分子電子云是球形對稱分布,不顯示出固有電矩,這不過表示在原子核外的四周出現電子的機率相等,即在某段時間內,電偶極矩的統計平均值等於零。但由於每個分子中的電子不斷運動和原子核的不斷振動,經常發生電子云和原子核之間的瞬時相對位移,使分子的正、負電荷“中心”暫時不重合,產生瞬時偶極矩,而且兩個瞬時偶極矩必然是採取異極相鄰的狀態,這些瞬時偶極矩可以相互作用,相互極化而產生吸引力,這種吸引力如果用帶電粒子的線諧振子代表瞬時偶極矩,用量子力學可以證明:
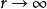 無極分子
無極分子1)兩振子無相互作用時,即當兩個諧振子平衡點(正電荷所處位置)之間的距離時,系統的能量為
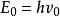 無極分子
無極分子2)兩振子有相互作用時,系統的能量為
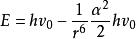 無極分子
無極分子比較1)、2)式可以看出,兩振子相互作用後,能量降低了,降低的數值為:
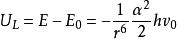 無極分子
無極分子其中a為極化係數,,h為普朗克常數,v為振子的振動頻率。兩振子才能相互作用,表現出它們之間的吸引力。因為它與v有關,故稱為色散力。無極性物質分子之間正是由於色散力的作用才能凝聚為液體,凝固為固體。因此,色散力是決定無極性分子物質物理性質的主要因素。
從上面分析中知道,無論在哪種情況下,由於無極分子瞬時偶極矩的產生,它所具有的電勢能、排斥能都大於吸引能按照能量最小原理,即原子中每一個電子都有一個趨勢,占據能量最低的能級,當原子中電子的能量最小時,整個原子的能量最低,原子即處於穩定狀態。因為能量最小原理具有普遍意義,當原子與原子、離子與離子、分子與分子結合時,同樣遵循這一原理,所以,分子具有的吸引能(W)的機率大於它所具有的排斥能的機率。正因為無極分子之間具有最小的吸引能,即最小結合能,所以無極分子可以結合成分子晶體。
