碳的循環
碳對生物和生態系統的重要性僅次於水,它構成生物體重量(乾重)的49%。有機化學就是專門研究碳化合物的一門科學,碳分子獨一無二的特性就是可以形成一個長長的碳鏈,這個碳鏈為各種複雜的有機分子(蛋白質、磷脂、碳水化合物和核酸等)提供骨架。同構成生物的其他元素一樣,碳不僅構成生命物質,而且也構成各種非生命化合物。在碳的循環中我們更加強調非生命化合物的重要性,因為最大量的碳被固結在岩石圈中,其次是在化石燃料(石油和煤等)中,這是地球上兩個最大的碳儲存庫,約占碳總量的99.9%,僅煤和石油中的含碳量就相當於全球生物體含碳量的50倍!在生物學上有積極作用的兩個碳庫是水圈和大氣圈(主要以CO2的形式)(圖5-37)
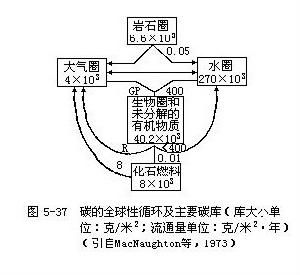
植物通過光合作用從大氣中攝取碳的速率和通過呼吸和分解作用而把碳釋放給大氣的速率大體相等。大氣中二氧化碳是含碳的主要氣體,也是碳參與循環的主要形式。碳循環的基本路線是從大氣儲存庫到植物和動物,再從動植物通向分解者,最後又回到大氣中去。在這個循環路線中,大氣圈是碳(以CO2的形式)的儲存庫,二氧化碳在大氣中的平均濃度是0.032%(或320/100萬,即320ppm)(圖5-38)
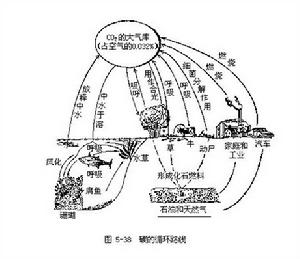
除了大氣以外,碳的另一個儲存庫是海洋。實際上海洋是一個更重要的儲存庫,它的含碳量是大氣含碳量的50倍。更重要的是,海洋對於調節大氣中的含碳量起著非常重要的作用。在植物光合作用中被固定的碳,主要是通過生物的呼吸(包括植物、動物和微生物)以二氧化碳的形式又回到了大氣。除此之外,非生物的燃燒過程也使大氣中二氧化碳的含量增加,如人類燃燒木材、煤炭以及森林和建築物的偶然失火等。正如前面已提到過的,地球上最大的碳儲存庫是岩石圈,其中包括由生物遺體所形成的泥炭、煤和石油以及由軟體動物的貝殼和原生動物的骨骼所形成的石灰岩(主要成分是碳酸鈣)。此外,有很多生長在鹼性水域中的水生植物,在進行光合作用時會釋放出碳酸鈣(光合作用的副產品)。例如,伊樂藻(Elodea canadensis)在自然光照條件下每10小時就可釋放出相當自身重量2%的碳酸鈣。這種純碳酸鈣和粘土混合就可形成泥灰岩,泥灰岩長期受壓就可轉變為石灰岩。廣泛分布於世界各地的石灰岩大都是這樣生成的。岩石圈中的碳也可以重返大氣圈和水圈,主要是藉助於岩石的風化和溶解、化石燃料的燃燒和火山爆發等。
二氧化碳在大氣圈和水圈之間的界面上通過擴散作用而互相交換著,而二氧化碳的移動方向決定於它在界面兩側的相對濃度,它總是從濃度高的一側向濃度低的一側擴散。藉助於降水過程,二氧化碳也能進入水圈。例如,一升雨水中大約含有0.3毫升的二氧化碳。在土壤和水域生態系統中,溶解的二氧化碳可以和水結合形成碳酸(H2CO3),而且這個反應是可逆的。碳酸在這個可逆反應中可以生成氫離子和碳酸氫根離子。
由於所有這些反應都是可逆的,所以反應進行的方向就取決於參加反應的各成分的濃度。由此可以想到,如果大氣中的二氧化碳發生局部短缺,就會引起一系列的補償反應,水圈裡的溶解態二氧化碳就會更多地進入大氣圈。同樣,如果水圈裡的碳酸氫根離子徑或從大氣中得到補充。總之,碳在生態系統中的含量過高或過低,都能通過碳循環的自我調節機制而得到調整,並恢復到原有的平衡狀態。放射性碳(14C)可用來估計空氣和水之間二氧化碳的交換速度。由於核武器試驗使大氣中含有很多的碳同位素。觀察空氣中14C的減少情況就能計算出二氧化碳在溶于海水以前在大氣中滯留了多少時間(大約是5~10年)。大氣中每年約有1000億噸的二氧化碳進入水中,同時水中每年也有相等數量的二氧化碳進入大氣。在陸地和大氣之間,碳的交換大體上也是平衡的。陸地植物的光合作用每年約從大氣中吸收1.5×1010噸碳,植物死後腐敗約可釋放1.7×1010噸碳。森林是碳的主要吸收者,每年約可吸收3.6×109噸碳,相當其他類型植被吸收碳量的兩倍。森林也是生物碳庫的主要儲存庫,約儲存著482×109噸碳,這相當於目前地球大氣含碳量的2/3。
但是,碳循環的調節機制能在多大程度上忍受人類的干擾,目前還不十分清楚。由於人類每年約向大氣中釋放2×1010噸的二氧化碳,使陸地、海洋和大氣之間二氧化碳交換的平衡受到干擾,結果使大氣中二氧化碳的含量每年增加7.5×109噸,這僅是人類釋放到大氣中二氧化碳的1/3,其餘的2/3則被海洋和增加了的陸地植物所吸收。大氣中二氧化碳含量的變化引起了人們的關注,大氣二氧化碳的含量在人類干擾以前是相當穩定的,但人類生產力的發展水平已達到了可以有意識地影響氣候的程度。從長遠來看,大氣中二氧化碳含量的持續增長將會給地球的生態環境帶來什麼後果,是當前科學家最關心的問題之一。
氮的循環
氮是構成生物蛋白質和核酸的主要元素,因此它與碳、氫、氧一樣在生物學上具有重要的意義。氮的生物地化循環過程非常複雜,循環性能極為完善(圖5-39)
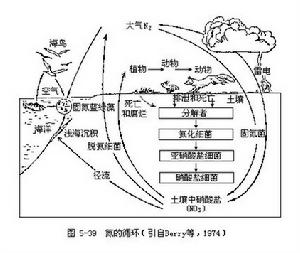
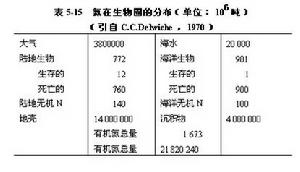
由於大氣成分的79%是氮氣,所以氮最重要的儲存庫就是大氣圈,但是大多數生物又不能直接利用氮氣,所以以無機氮形式(氨、亞硝酸鹽和硝酸鹽)和有機氮形式(尿素、蛋白質和核酸等)存在的氮庫對生物最為重要。大氣中的氮只有被固定為無機氮化合物(主要是硝酸鹽和氨)以後,才能被生物所利用。雖然固氮的方法有物理化學法和生物法兩種,但其中以生物固氮法最為重要。據估計,靠電化學和光化學固氮,每年平均可固氮7.6×106噸,而生物固氮平均每年的固氮量為54×106噸,人類每年合成氮肥約30×106噸,這也是一個不小的數字。根據人類合成氮肥的增產速度,預計到本世紀末,每年約可生產氮肥100×106噸。C.C.Delwiche認為:現在的工業固氮量約等於現代農業到來之前的生物固氮量。
固氮過程首先需要分子氮激活,使其分裂為兩個自由氮原子(N2→2N),這個過程需要消耗能量,在生物固氮時,1摩爾的N2約耗能669×103焦。在自由氮與氫結合形成氨氣時(N→NH3),1摩爾的氮氣(28克)可釋放54×103焦能量,因此,固定1摩爾的氮氣,只需輸入615×103焦能量就夠了(即669-54=615)。除了光化學固氮法外,所有固氮生物都需要從外部提供碳化合物作為一種能源,以便影響這一吸熱反應。生物固氮需要兩種酶(固氮酶和氫化酶)進行調節,生物固氮的意義在於低能消耗,而工業固氮需要極高的溫度和極大的壓力(即400℃高溫和200個大氣壓)。
已知有固氮能力的細菌和藻類很多,但為了方便可把它們分為兩個類群:一類是共生的固氮生物(主要是細菌,但也有真菌和藻類),另一類是自由生活的固氮生物(包括細菌、藻類和其他一些微生物)。共生的固氮生物主要生活在陸地,而營自由生活的固氮生物在陸地和水域都有。但共生固氮生物在數量上至少要比營自由生活的固氮生物多幾百倍。
在共生固氮生物中,根瘤菌(Rhizobium)是最重要的,也是人類了解最清楚的。根瘤菌對宿主植物(如豌豆、三葉草和菜豆等豆科植物)有高度的特異性,一定種類的根瘤菌只同一定種類的豆科植物發生共生關係,這些根瘤菌可潛入豆科植物的根毛,然後進行繁殖。已知有10多種高等植物(如鼠李、楊梅和榿木等)也有共生生物固氮作用。由於豆科植物與根瘤菌之間已經形成了密切的共生關係,所以豆科植物離開了根瘤菌就不能固氮,而把根瘤菌接種在其他植物上也不能固氮。
正如前面已說過的,在水生生態系統中,固氮生物大都是非共生生物,但有一個重要例外,這就是滿江紅(Azolla)及其共生物藍綠藻[魚腥藻(Anabaena)],它們廣泛分布於我國溫帶和亞熱帶的水稻田中,被農民作為肥料加以利用,因此對農業生產有重要意義。在非共生固氮生物中既有需氧細菌也有厭氧細菌,還包括藍綠藻。需氧固氮菌[如固氮菌屬(Azotobacter)]廣泛分布在土壤中以及淡水和海水中;厭氧菌[如梭菌屬(Clostridium)]的分布也同樣廣泛。事實證明:土壤和水體中的很多細菌都有固氮能力,又由於它們數量極多,所以它們固定的氮量也相當可觀。例如在鹽沼的沉積層中,細菌固氮量相當於藻類固氮量的10倍。這裡值得強調的一點是:所有的共生和非共生固氮菌都需要從外部供應糖類,以便作為一種能源去完成固氮過程的吸熱反應,因為沒有任何一種固氮菌能夠進行光合作用(固定1摩爾氮氣(N2)需吸熱615×103焦)。
為了研究水體中的固氮過程,需把溶於水中的大氣氮移出(通常是用氦清除),然後用一種穩定的氮同位素15N取而代之。並且質譜分析儀跟蹤觀察這種同位素的去向,這種方法與使用14C測定初級生產量的方法大體相同。P.Richard等人用這種方法研究過Sanctuary湖的固氮過程。研究表明:高固氮率與三種藍綠藻(魚腥藻屬)存在著正相關。對其他兩個湖(Mondota和Wingra湖)的研究也表明:高固氮率與其他藍綠藻(包括Gleotrichia echinulata)的大量存在密切相關。而在馬尾藻海,高固氮率則與束毛藻(Trichodesmium屬)的存在相關。固氮過程所需要的能量是靠這些藍綠藻的光合作用提供的,也就是說,藍綠藻所生產的有機物質提供了固氮所需要的能量(615×103焦/摩爾)。
當無機氮經由蛋白質和核酸合成過程而形成有機化合物(主要是胺類,即—NH2)以後,這些含氮的有機化合物通過生物的新陳代謝又會使氮以代謝產物(尿素和尿酸)的形式重返氮的循環圈。土壤和水中的很多異養細菌、放線菌和真菌都能利用這種富含氮的有機化合物。這些簡單的含氮有機化合物在上述生物的代謝活動中可轉變為無機化合物(氨)並把它釋放出來。這個過程就稱為氨化作用(ammonification)式礦化作用(mineralization)。實際上,這些微生物是在排泄它們體內過剩的氮。有些具有氨化作用的微生物只能利用腖而不能利用簡單的胺基酸,或者只能利用尿素而不能利用尿酸。相反,其他的微生物則能利用多種多樣的含氮有機化合物。氨化過程是一個釋放能量的過程,或者說是一种放熱反應(exothermic reaction)。例如,如果蛋白質的基本構成物是甘氨酸,那么1摩爾的這種蛋白質經過氨化就可釋放出736×103焦的熱能。這些能量將被細菌用來維持它們的生命過程。
硝化作用雖然有些自養細菌和海洋中的很多異養細菌可以利用氨或銨鹽來合成它們自己的原生質,但一般說來,這些含氮化合物難以被直接利用,而必須使它們在硝化作用(nitrifi-cation)中轉化為硝酸鹽。這個過程在
-nas屬)可使氨轉化為亞硝酸鹽,而其他細菌(如硝化細菌)則能把亞硝酸鹽轉化為硝酸鹽。這些細菌全都是具有化能合成作用的自養細菌,它們能從這一氧化過程中獲得自己所需要的能量。它們還能利用這些能量使二氧化物或重碳酸鹽還原而獲得自己所需要的碳,同時產生大量的亞硝酸鹽或硝酸鹽。據R.Jackson和F.Raw的研究,亞硝化胞菌(N.europaea)每同化一個單位的二氧化碳就可使35個單位的氨氧化為亞硝酸鹽;而硝化菌(Nitrobacter agilis)每同化一個單位的二氧化碳可使76~135個單位的亞硝酸鹽氧化為硝酸鹽。硝酸鹽和亞硝酸鹽很容易通過淋溶作用從土壤中流失,特別是在酸性條件下。
目前,對開闊海洋及其海底沉積物中的硝化作用還不十分了解。1962年,S.Watson首次報導了從開闊大洋海水中分離出來的海洋亞硝化菌(Nitrosocystis oceanus),他的研究表明,這是一種專性自養細菌,它只能從氨中獲得能量和從二氧化碳中獲得碳。不少科學家認為,氮素是海洋浮游植物生產量的主要限制因素。
(也稱脫氮作用)
反硝化作用是指把硝酸鹽等較複雜的含氮化合物轉化為N2、NO和N2O的過程,這個過程是由細菌[如假單孢菌屬(Pseudomonas)]和真菌參與的。這些細菌和真菌在有葡萄糖和磷酸鹽存在時可把硝酸鹽作為氧源加以利用。大多數有反硝化作用的微生物都只能把硝酸鹽還原為亞硝酸鹽,但是,另一些微生物卻可以把亞硝酸鹽還原為氨。在無氧條件下和有葡萄糖存在時,硝酸鹽還原為一氧化氮的反硝化過程是一种放熱反應,1摩爾的硝酸鹽約可放熱2.28×106焦。若將1摩爾的硝酸鹽還原為分子氮(N2),則可放熱2.38×106焦。
由於反硝化作用是在無氧或缺氧條件下進行的,所以這一過程通常是在透氣較差的土壤中進行的。依據同樣的道理,在氧氣含量很豐富的湖泊和海洋表層,反硝化作用便很難發生。但是在水生生態系統缺氧的時期,分子氮就可以通過反硝化過程而產生,這一現象已在Alaskan湖被觀察到了。J.Goering從湖底和冰層下1米深處採集水樣(冬季),注入標記氮的硝酸鹽(K15NO3),然後將水樣培養在與湖溫相同的溫度下。用質譜分析儀進行分析表明:湖底水樣中的反硝化過程約比湖面附近快6倍,反硝化作用最重要的終結產物是分子氮,但是沒有NO和N2O,分子氮如果未在固氮活動中被重新利用則會返回大氣圈庫。
據估計,全球每年的固氮量為92×106噸(其中生物固氮54,工業固氮30,光化學固氮7.6和火山活動固氮0.2)。但是,藉助於反硝化作用,全球的產氮量只有83×106噸(其中陸地43,海洋40和沉積層0.2)。兩個過程的差額為9×106噸,這種不平衡主要是由工業固氮量的日益增長所引起的,所固定的這些氮是造成水生生態系統污染的主要因素。最近對海洋環境的研究表明,硝化作用大約可使海洋氮庫補充20×106噸氮。從各種來源輸入海洋的氮,大體上能被反硝化作用所平衡,基本上能維持一種穩定狀態。
至今有一點是很清楚的,即氮的移動絕不是單方向、不可調節和與能量無關的。氮有很多循環路線,而每一條路線都受生物或非生物機制所調節,而且每一個過程都伴隨著能量的消耗或釋放。氮循環的這許多自我調節機制、反饋機制和對能量的依賴性曾導致提出了這樣一個假設,即全球的氮循環是平衡的,固氮過程將被反硝化過程所抵銷。目前這一假說還處在討論之中。如果工業固氮量速率加速增長,而反硝化作用的增加速度又跟不上的話,那么任何已經達到的平衡都可能受到越來越大的壓力。另外一個干擾因素是來自汽車和其他機動車所排放的NO2,排放到大氣中的含氮氣體是造成空氣污染的主要原因之一,而且這種污染物對於呼吸系統和大氣臭氧層非常有害。在某些生態系統內,硝化過程和反硝化過程能達到極好的協調,以有利於生態系統生產力的需要。這種協調過程在溫帶地區的冬季進行得最快,以致總是能保證在春季和夏初時使硝酸鹽的數量達到最大,而這時也正是植物生長和繁殖需要硝酸鹽最多的時候。
