與Lewis的結構
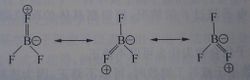 形式電荷
形式電荷形式電荷可以用來判斷所寫的Lewis結構是否合理。例
如:SCN1- 的 Lewis結構應該是將碳原子放在中間,氮原子和硫原子分別放在兩邊。此時,氮原子的形式電荷是-1,碳原子和硫原子的形式電荷是0;但如果將硫原子安排在中間,則氮原子的形式電荷是-1,碳原子的形式電荷是-2,硫原子的形式電荷是+2。可以看出,後者中,各原子形式電荷數相差很多,結構不穩定,顯然前者更合理。
根據判斷Lewis結構式的穩定性
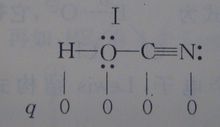 形式電荷
形式電荷⑴在Lewis結構式中,q應儘量小,若共價分子中所有原子的形式電荷都為零,則是最穩定的Lewis結構式;
⑵兩相鄰原子之間的形式電荷應避免同號。
