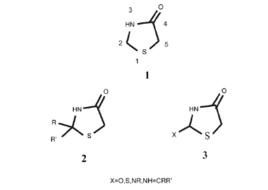
基本介紹
對於含有噻唑環的藥物來說,得到最廣反套用的就是噻唑酮類,如羅格列酮6。它屬於新一代的抗糖尿病藥物即噻唑烷二酮類藥品,於1999年在美國上市,在2002年就已經超越人工胰島素成為全球銷售第一的降糖產品。羅格列酮本身不會引起身體分泌更多的胰島素,它是通過幫助身體更有效地利用胰島素來達到治療目的。近年來,利用不對稱有機催化構建噻唑酮類衍生物的研究備受關注,其中對於噻唑酮類衍生物的不對稱構建己經取得了一些突破性的成果。噻唑酮分子上帶有很多反應位點,因此能夠進行一系列的修飾反應。它們的五元環上存在11個不同的親核位點和一個親電位點,這使得它們成為良好的反應底物套用於多種多樣的分子合成中。
藥理學活性
噻唑酮類化合物的藥理學活性
抗組胺活性(H1受體阻斷劑)
噻唑酮類化合物對組胺H1受體具有抑制作用。Singh等研究了2, 3-二取代-噻唑酮抗組胺H1受體活性,並得到以下結論:苯環4-位帶有疏水性取代基或苯環上取代基的電負性增強都能使抗組胺活性增強。Diurno等人設計了一系列2-取代苯基-噻唑酮類化合物,發現化合物1及其衍生物能夠抑制由組胺引起的豚鼠迴腸收縮。化合物構效關係的研究表明,當苯環上取代基的疏水性增強時,與化合物與組胺H1受體的結合能力增強。因此化合物疏水性在抗組胺活性中起著至關重要的作用。
抗結核活性
由於多藥耐藥性結核病的出現,愛滋病結核病雙重感染在世界範圍內廣泛流行,使得結核病成為世界最擔憂的健康問題。近年來,K. Babaoglu等以鼠李糖生物合成路徑中的關鍵酶作為靶點,建立了一個2,3,5-三取代的噻唑酮虛擬化合物庫,希望這些化合物可以作為氯喹的替代品。發現噻唑酮構架可以模擬氯喹,其與靶點的特異性結合因環周圍取代基團的不同而改變。這些化合物可以嵌入分支結核桿菌差向異構酶(Rml C)的活性空腔中。選擇合成其中結合能力最強的94個化合物進行活性測試,發現其中30個化合物(20 μmol·L−1)在鼠李糖合成實驗中對鼠李糖合成的抑制率大於50%。K. Babaoglu等還假設噻唑酮結構是通過模擬二磷酸而起抑制作用的。
心血管作用
噻唑酮化合物的抗心血管疾病作用早有報導,各種2-環戊基(環己基)亞胺-2-芳基-噻唑酮-5羧酸類化合物,對任意性別的成年貓均有不同程度的降血壓作用[6],但降壓持續時間都短於15 min。Suzuki等研究了化合物CP-060S對狗的心臟功能和心肌耗氧量(MVO2)的影響。結果表明,其作用類似於典型的鈣通道阻斷劑地爾硫 。
抗菌抗生物膜活性
關於噻唑酮類化合物潛在抗菌活性的研究有很多報導。一些類似於文拉法辛(抗抑鬱藥)結構的新型2,3-二取代-4噻唑酮對枯草芽孢桿菌和大腸桿菌有明顯的抑制作用。。其中化合物3具有優異的抗菌活性,初步的構效關係表明:苯環2-位和6-位氟原子的吸電子作用對抗菌活性有很大影響;噻唑酮和文拉法辛結構的拼接可能提高抗菌活性。Mohamed S. A等將磺胺類藥物的潛在活性基團與噻唑酮骨架進行有機結合,合成的化合物4及其類似物表現出與氨苄西林相似的抗菌活性。近年來,細菌生物被膜(bacterial biofilm,BBF)引起的感染日益嚴重。BBF是由於細菌相互黏連、聚集纏繞其中形成的膜樣物,可以抵擋宿主的免疫殺傷,而且具有極強的耐藥性。復旦大學醫學院和中國科學院上海藥物研究所合作,以表皮葡萄球菌Yyc G組氨酸激酶功能域作為候選抗菌藥物靶點,通過高通量虛擬篩選獲得小分子化合物,其中具有噻唑酮結構的化合物對表皮葡萄球菌形成生物膜的殺傷濃度達到6.25 μmol·L−1,遠高於萬古黴素88 μmol·L−1。
抗真菌活性
Katti等合成的化合物5及其衍生物對2種白色念珠菌菌株和一種新型隱球菌菌株具有抑制作用,通過連續雙倍稀釋法測得最小抑菌濃度(MIC)為50 μg·m L−1,並對其他3種真菌菌株具有較好的抑制活性。Dandia等將吲哚環和噻唑酮母環相結合,合成了化合物6和一系列衍生物。測試其抗真菌活性。結果表明對選擇的3種菌株具有很好的抗菌活性。在噻唑酮環上引入雜環明顯增強了化合物抗真菌活性 。
抗癌活性
一系列新型的噻唑酮的醯胺類化合物表現出抗前列腺癌細胞增殖作用。在實驗中,分別測試這些化合物對5種人類前列腺癌細胞系(DU-145,PC-3,LNCa P,PPC-1和TSU)和陰性對照組RH7777的抗增殖活性,結果表明有些化合物能夠有效殺傷前列腺癌細胞。
環氧合酶(COX)是催化花生四烯酸轉化為前列腺素(PGs)的重要酶。而PGs也是癌症發病機制中的重要物質。有報導利用COX-2抑制劑作為潛在藥物預防和治療癌症,特別是結腸直腸癌。化合物8衍生物能夠抑制人類結腸癌細胞株HT-29細胞的增殖,並能抑制其他細胞株如DLD-1的增殖。山東大學藥學院和美國馬里蘭大學等單位合作,運用計算機虛擬篩選和組合化學手段,設計合成了具有216個化合物的化合物庫。測定了這些化合物的抗癌活性並研究了其構效關係。結果表明:在C環上的R2基團可能更接近活性位點,而R1則與之遠離;化合物通過2個氫鍵和3個疏水鍵和受體相結合。
抗HIV活性
近年來,不斷有關於2, 3-二芳基-噻唑酮抗HIV活性的報導。部分化合物表現出很高的抗HIV-1受體活性並且具有較低的細胞毒性。它們的作用機制是通過抑制逆轉錄酶從而抑制人類免HIV的。Barreca設計合成了包括化合物9在內的一系列新型的非核苷逆轉錄酶抑制劑,與作為先導化合物的苯並咪唑類化合物相比抗HIV活性增強了10倍以上。而且表現出很高的選擇性。其中,化合物9的選擇性指數高達6470,而半數有效濃度(EC50)達到0.044 μmol·L−1。構效關係的研究表明:分子中的2個共軛系統以及芳環上的氮原子會增強對逆轉錄酶的抑制活性;增大芳環部分的空間體積也可以提高抗病毒活性。Katti等[20]也報導了新型的抗HIV受體活性的噻唑酮化合物10,EC50達到0.204 μmol·L−1。Ravichandran 等通 過 三 維 定 量 構 效 關 系(3D-QSAR)研究了一些噻唑酮類似物的抗HIV活性。
套用
噻唑酮在有機不對稱催化中的套用
到目前為止,噻唑酮在藥物中的套用已經得到了廣泛的研究,雖然有很多的含有噻唑酮單元的藥物已經得到合成套用,但是利用不對稱催化的方法對其的研究依然十分有限。在2010年,Ooi小組發表了第一例將噻唑酮套用於不對稱催化中的研究。在報導中,作者合成了一個新的Cl-軸對稱的手性Binol衍生內胺鹽L23,並將其成功的套用到了2-烷氧基噻唑酮的不對稱Mannich反應中。產物都以優秀的非對應以及對應選擇性獲得,並且通過簡單的衍生步驟即可得到。隨後在2011年,我們小組報導了一個使用奎寧衍生物的有機催化體系,通過該體系,我們成功的實現了2,4-二取代噻唑酮和N-苯磺醯亞胺的Mannich反應。反應取得了優秀的立體選擇性,並且得到了一系列的2,4-二取代噻唑酮衍生物 。通過細胞實驗檢測,這些化合物發現具有良好的抗癌活性。這些工作對於後期發展噻唑酮類的手性抗癌試劑具有重要意義。