道爾頓實心球
道爾頓模型(1803年) 原子是一個堅硬的實心小球
英國自然科學家約翰·道爾頓提出了世界上第一個原子。
理論
①原子都是不能再分的粒子;②同種元素的原子的各種性質和質量都相同;③原子是微小的實心球體。
 實心球體
實心球體雖然,經過後人證實,這是一個失敗的理論模型,但道爾頓第一次將原子從哲學帶入化學研究中,明確了今後化學家們努力的方向,化學真正從古老的鍊金術中擺脫出來,道爾頓也因此被後人譽為“近代化學之父”
葡萄乾蛋糕
1904年約瑟夫·約翰·湯姆遜(J.J.Thompson)模型 原子是一個帶正電荷的球,電子鑲嵌在裡面,原子好似一塊“葡萄乾布丁”(Plum pudding)故名“棗糕模型”或“葡萄乾蛋糕模型”;或是像西瓜子分部在西瓜瓤中,所以也叫“西瓜模型”。
約瑟夫·約翰·湯姆遜在1897年發現電子,否定了道爾頓的“實心球模型”。
葡萄乾蛋糕模型(棗糕模型/西瓜模型)由約瑟夫·約翰·湯姆遜提出,是第一個存在著亞原子結構的原子模型。
約瑟夫·約翰·湯姆遜生在發現電子的基礎上提出了原子的葡萄乾蛋糕模型(棗糕模型/西瓜模型)。
原理
 棗糕模型
棗糕模型①電子是平均的分布在整個原子上的,就如同散布在一個均勻的正電荷的海洋之中,它們的負電荷與那些正電荷相互抵消。②在受到激發時,電子會離開原子,產生陰極射線。
盧瑟福行星
湯姆生的學生盧瑟福完成的α粒子轟擊金箔實驗(散射實驗),否認了葡萄乾麵包式模型的正確性。
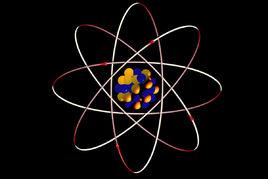
1911年盧瑟福提出行星模型:原子的大部分體積是空的,電子按照一定軌道圍繞著一個帶正電荷的很小的原子核運轉。
行星模型由盧瑟福在提出,以經典電磁學為理論基礎,主要內容有:
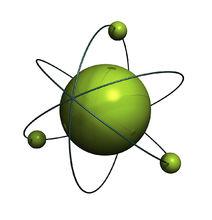 行星模型
行星模型①原子的大部分體積是空的 ②在原子的中心有一個很小的原子核 ③原子的全部正電荷在原子核內,且幾乎全部質量均集中在原子核內部。帶負電的電子在核空間進行繞核運動。
玻爾量子化
1913年玻爾模型電子不是隨意占據在原子核的周圍,而是在固定的層面上運動,當電子從一個層面躍遷到另一個層面時,原子便吸收或釋放能量。
為了解釋氫原子線狀光譜這一事實,玻爾在行星模型的基礎上提出了核外電子分層排布的原子結構模型。
玻爾原子結構模型的基本觀點是:
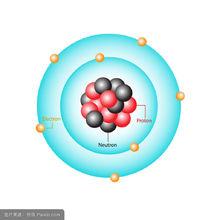 量子軌道模型
量子軌道模型①原子中的電子在具有確定半徑的圓周軌道(orbit)上繞原子核運動,不輻射能量。②在不同軌道上運動的電子具有不同的能量(E),且能量是量子化的,軌道能量值以n(1,2,3,...)的增大而升高,n稱為量子數。而不同的軌道則分別被命名為K(n=1)、L(n=2)、M(n=3)、N(n=4)、O(n=5)、P(n=6)。③若且唯若電子從一個軌道躍遷到另一個軌道時,才會輻射或吸收能量。如果輻射或吸收的能量以光的形式表現並被記錄下來,就形成了光譜。
現代電子云
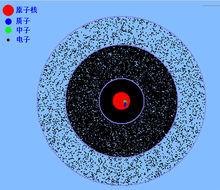 電子云模型
電子云模型20世紀20年代以來 現代模型(電子云模型) 電子繞核運動形成一個帶負電荷的雲團,對於具有波粒二象性的微觀粒子在一個確定時刻其空間坐標與動量不能同時測準,這是德國物理學家海森堡在1926年提出的著名的不確定性原理。