背景知識
有機反應類型分類
根據共價鍵斷裂的方式,有機化學反應可以分為協同反應,自由基反應,離子型反應。
協同反應:在反應過程中,舊鍵的斷裂和新鍵的形成都相互協調地在同一步驟中完成的反應稱為協同反應。協同反應往往有一個環狀過渡態。它事一種基元反應。
自由基型反應: 由於分子經過均裂產生自由基而引發的反應稱為自由基型反應。自由基型反應分鏈引發、鏈轉移和鏈終止三個階段。
離子型反應:出分子經過異裂生成離子而引發的反應稱為離子型反應 。 離子型反應有親核反應和親電反應。 由親核試劑進攻而發生的反應稱為親核反應,親核試劑是對正原子核有顯著親和力而起反應的試劑。由親電試劑進攻而發生的反應稱為親電反應。而親核以及親電反應又可以進一步分為加成反應和取代反應。
反應物與試劑
反應物和試劑之間沒有十分嚴格的界限,是個相對的概念、 慣用語。本來相互作用的兩種物質,即可互為反應物, 也可互為試劑。但為了討論和研究問題時方便,從經驗中人為的規定反應中的一種有機物為反應物,無機物或另一種有機物為試劑。
分子內親核取代反應歷程
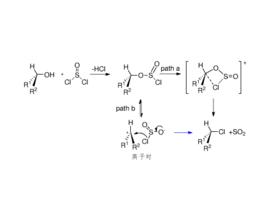
分子內親核取代反應(internalnucleophilicsubstitution)用SNi表示,其中S代表取代,N代表親核,i代表分子內。在上述醇與二氯亞碸作用生成氯代烷的反應中,若在無溶劑條件下進行,或在非親核性溶劑(如二氯甲烷)中進行,反應也得到構型保持的氯代產物。在此情況下,反應按照SNi機理進行,而不是兩次SN2過程。
 分子內親核取代
分子內親核取代反應首先形成氯亞磺酸酯,氯亞磺醯酯在加熱分解時通過一個協同的四元環過渡態,一步生成構型保持的氯代烷(patha),或先生成離子對,然後,離去基團作親核試劑,同面進攻碳正離子,生成構型保持的產物(pathb)。這兩個機理目前尚存爭論。
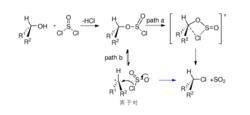 分子內親核取代
分子內親核取代前沿研究
最近報導,四氯化鈦可催化醇與二氯亞碸的反應。在二氯甲烷溶劑中,醇二氯亞碸先生成氯亞磺酸酯,後者在催化量的四氯化鈦存在下轉化為構型保持的氯化物,例如:
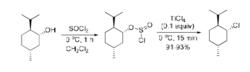 分子內親核取代
分子內親核取代相關知識-其他兩種親核取代反應
發生在鹵代烷、醇、磺酸酯等有機化合物的飽和碳原子上的親核取代主要有兩種機理,即單分子親核取代反應(用SN1表示)和雙分子親核取代反應(用SN2表示),其中S代表取代(substitution),N代表親核(nucleophilic),1代表單分子,2代表雙分子。
單分子親核取代反應
以叔丁基氯的水解為例:反應分步進行。首先C‐Cl鍵發生異裂生成碳正離子和氯負離子,碳正離子接受溶劑的親核進攻,生成質子化的醇,和水發生質子交換最後得到醇。反應發生在飽和碳原子,即sp3碳原子上,淨結果是氯被羥基所取代,水作為親核試劑進攻到碳原子上,因此,稱為飽和碳原子上的親核取代。反應的決速步驟是C‐Cl鍵的異裂,反應速度只和叔丁基氯的濃度有關,和親核試劑的濃度無關,因此,是單分子反應動力學。總體上講,該反應稱為飽和碳原子上單分子親核取代反應,即SN1反應。
反應的決速步驟是C‐X鍵的異裂,因此,離去基團對SN1反應速度的影響如下,氟代烴不能作為SN1反應的底物:R-I > R-Br > R-Cl。SN1反應為單分子反應動力學,反應速度只和底物的濃度有關,和親核試劑的濃度無關,因此,親核性的強弱對SN1反應無影響。碳正離子是一個平面結構,親核試劑從可以平面的兩側進攻碳正離子,理論上產物是一對對映體,沒有立體選擇性。多數情況下,SN1反應優先得到構型翻轉的產物。這可從離子對理論進行解釋。離子對理論認為,C-X鍵的異裂經過緊密離子對、溶劑間隔離子對,最後成為自由的碳正離子。只有自由的碳正離子才是以均等的幾率接受親核試劑的兩面進攻。親核試劑進攻底物、緊密離子對、溶劑間隔離子對時,都是從離去基團的反面進行進攻。因此,主要產物為構型翻轉的產物。
雙分子親核取代反應
與SN1反應相對應,SN2反應中,親核試劑帶著一對孤對電子進攻具親電性的缺電子中心原子,形成過渡態的同時,離去基團離去。反應中不生成碳正離子,速率控制步驟是上述的協同步驟,反應速率與兩種物質的濃度成正比,因此稱為雙分子親核取代反應。無機化學中,常稱雙分子親核取代反應類型的反應機理為“交換機理”。SN2反應最常發生在脂肪族sp3雜化的碳原子上,碳原子與一個電負性強、穩定的離去基團(-X)相連,一般為鹵素陰離子。親核試劑(Nu)從離去基團的正後方進攻碳原子,Nu-C-X角度為180°,以使其孤對電子與C-X鍵的σ反鍵軌道可以達到最大重疊。然後形成一個五配位的反應過渡態,碳約為sp2雜化,用兩個垂直於平面的 p軌道分別與離去基團和親核試劑成鍵。C-X的斷裂與新的C-Nu鍵的形成是同時的,-X很快離去,形成含C-Nu鍵的新化合物。
SN2反應一般發生在伯碳原子上,很難成為有位阻分子的反應機理,並且取代基越多,按SN2機理反應的可能性越小。基團在空間上比較擁擠的分子一般採用SN1機理,可以緩解一部分的位阻,也可生成較穩定的碳正離子(通常為三級碳正離子)。由於親核試劑是從離去基團的背面進攻,故如果受進攻的原子具有手性,則反應後手性原子的立體化學發生構型翻轉,也稱“瓦爾登翻轉”。這也是SN2反應在立體化學上的重要特徵。反應過程類似於大風將雨傘由里向外翻轉。