反應機理
鹵代芳烴與強鹼反應下機理舉例:
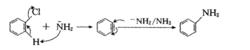 反應機理
反應機理苯炔
苯炔是從苯環去除兩個H原子得到的電中性的活性中間體。
苯炔主要含有以下三種位置異構體。在合成化學中,最重要也是最常見的是鄰位的兩個H被消除後得到的o-苯炔。它具有特彆強的親電子性,常被用於Diels-Alder反應中。而p-苯炔由於是環烯二炔環化(正宗-Bergman環化)的中間體而被大家所熟知。
開發歷史
1940年代Wittig (1940), Gilman (1945), Bergstrom (1946)等人用強鹼作用於鹵代苯環得到了意料之外的反應,但是那時候並不知道是生成了苯炔,所以一直也沒有苯炔結構的鑑定報導。在1953年Roberts等人詳細探索了這個反應,提出了苯炔反應中間體。
反應機理
苯炔的三鍵其實並不是穩定的直線型的,而是變形的比較斜的結構,正因為這種不穩定結構,經常被用於反應中間體進行各種化學反應。
苯炔的三鍵長度(1.24Å)介於雙鍵(乙烯1.34Å)與典型三鍵(乙炔1.20Å)之間。
苯炔在反應溶液中顯親電子性,在芳香族的親核置換反應中,如下圖所示,反應機理一般是親核試劑進攻苯炔完成取代反應。而這個反應機理也通過同位素碳標記(紅色單鍵)得到證實。
苯炔的親核反應的位置選擇性受到苯炔環上的取代基影響,最近研究也發現這種擁有扭曲環結構的位置選擇性與取代基之間關係是可以預測的。
反應實例
苯炔的環化三聚物。
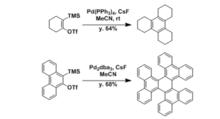 苯炔的環化三聚物
苯炔的環化三聚物分子內親核反應。
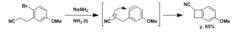 分子內親核反應
分子內親核反應