簡介
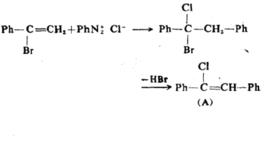
芳基自由基可與烯反應,將芳基引至烯鍵的碳原子上,稱為Meerwein芳基化反應。芳基自由基通常由芳基重氮鹽在銅催化下分解生成,如 :
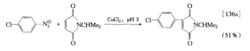 反應方程式
反應方程式在有些情況下,得到的產物是鹵代物。如:
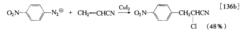 反應方程式
反應方程式反應機理
有認為此反應為自由基-親核芳香取代機理。首先重氮鹽斷裂放出氮氣,生成芳基自由基,接下來芳基自由基對雙鍵進行自由基加成,產生的烷基自由基中間體被重氮鹽中的反離子如鹵素或四氟硼酸根捕獲,生成取代芳香族化合物。此產物還可繼續經過消除放出鹵化氫,從而進一步得到苯乙烯衍生物。
Meerwein反應的機理可能是:重氮鹽生成芳基自由基(151),(151)進攻烯烴得自由基(152),後者被Cu(Ⅱ)氧化得碳正離子(153),接著轉變為烯(154)或鹵代物(155)。
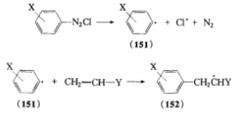 反應機理
反應機理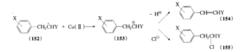 反應機理
反應機理反應特點
Meerwein反應通常以丙酮、水或吡啶等極性溶劑為反應介質。酸性有利於反應的進行,無氯化銅或氯化亞銅等催化劑存在時,雖能反應,但收率不高。乙烯、乙炔等不飽和烴連有吸電子基團而重氮鹽的芳環上連有釋電子基時,產率通常比較高。