成份
化學名稱:1-環丙基-7-{(S,S)-2,8-重氮-二環[4.3.0]壬-8-基}-6-氟-8-甲氧-1,4-二氫-4-氧-3-喹啉羧酸鹽酸鹽。
化學結構式:
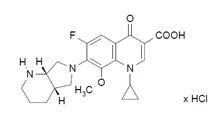 鹽酸莫西沙星氯化鈉注射液
鹽酸莫西沙星氯化鈉注射液分子式:CHFNO·HCl
分子量:437.9
輔料:氯化鈉、鹽酸、氫氧化鈉、注射用水。
性狀
本品為黃色的澄清液體。
適應症
成人(≥18歲)上呼吸道和下呼吸道感染,如:急性竇炎,慢性支氣管炎急性發作,社區獲得性肺炎;以及皮膚和軟組織感染。
複雜腹腔感染包括混合細菌感染,如膿腫。
規格
250ml : 莫西沙星0.4g與氯化鈉2.0g。
用法用量
給藥方法:根據中國健康受試者心臟所能耐受的輸液速率以及國內I、II、III期臨床研究的結果,推薦本品的輸液時間應為90分鐘。(國外推薦0.4g莫西沙星靜脈給藥的輸液時間應大於60分鐘。)
劑量範圍(成人):
推薦劑量為一次0.4g,一日一次(一次1瓶,一日一次)。
療程:
根據症狀的嚴重程度或臨床反應決定療程。治療上呼吸道和下呼吸道感染時通常可按照下列療程:
慢性支氣管炎急性發作:5天
社區獲得性肺炎:序貫給藥(靜脈給藥後繼續口服用藥)推薦的總療程為7~14天。
急性竇炎:7天
治療皮膚和軟組織感染的推薦療程為7天。
莫西沙星可以在開始治療時靜脈給藥,之後再根據患者情況口服片劑給藥。
0.4g莫西沙星注射液在臨床試驗中最多用過14天。
給藥方法:
靜脈給藥0.4g的時間應為90分鐘。
莫西沙星既可以單獨給藥也可以與一些相容的溶液一同滴注。
下列注射液與莫西沙星注射液的混合液在室溫條件下可保持穩定24小時以上,因此被認為可以合併給藥:
注射用水
0.9%氯化鈉注射液
1摩爾氯化鈉注射液
5%葡萄糖注射液
10%葡萄糖注射液
40%葡萄糖注射液
20%木糖醇注射液
林格氏液
乳酸林格氏液
Aminofusin10%(生產廠家: Pharmacia&Upjohn)
Jonosteril D5 (生產廠家: Fresenius Kabi)
若莫西沙星注射液需與其它藥物合用,每種藥物需單獨給藥(見不相容性)。
只有澄明的溶液才能使用。
老年人
老年人不必調整用藥劑量。
兒童
莫西沙星對兒童和青少年的療效和安全性尚未確定。(見特別提醒和注意事項)
肝損害
肝功能受損的病人(Child Pugh A to C)與健康志願者或肝功能正常的患者血漿藥物濃度在臨床上無明顯差別。
腎損害
腎功能受損的病人(包括肌酐清除率≤30ml/min/1.73m)和慢性透析,如血液透析和持續性不臥床腹膜透析的患者無需調整劑量。
種族差異
對高加索人、日本人、黑人及其他種族人群進行了可能的種族間差別試驗,未發現臨床相關的藥代動力學差別。因此,不同種族間不必調整藥物劑量。
不良反應
本品不良反應(ADRs)以0.4g莫西沙星(口服和序貫療法)的全部臨床研究為基礎,按照CIOMSIII頻率分類,(總計n=12984,包括序貫療法n=2535,時間:2005年12月)整理如下:
“常見”項下所列不良反應(ADRs)除噁心和腹瀉外發生率在3%以下。
源自上市後報告(時間:2008年6月)的不良反應(ADRs)為斜體印刷。
 鹽酸莫西沙星氯化鈉注射液
鹽酸莫西沙星氯化鈉注射液在接受口服或靜注貫序治療亞組患者中,下述不良反應發生頻率較高:
常見:γ谷氨醯氨轉肽酶增高
少見:室性心動過速,低血壓,水腫,抗生素所致結腸炎(極少病例伴有致命併發症),各種臨床表現的癲癇發作(包括癲癇大發作),幻覺,腎臟損傷和腎衰(脫水所致,尤其已患腎病老年患者)。
禁忌
已知對莫西沙星的任何成份,或其他喹諾酮類,或任何輔料過敏者。
妊娠和哺乳期婦女。
由於缺乏患有肝功能嚴重損傷(Child Pugh C級)的患者和轉氨酶升高大於5倍正常值上限的患者使用莫西沙星的臨床數據,該藥在這類患者中禁止使用。
18歲以下患者。
注意事項
莫西沙星能夠延長一些患者心電圖的QT間期。該藥應避免用於QT間期延長的患者、患有無法糾正的低鉀血症患者及接受Ia類(如:奎尼丁,普魯卡因胺)或III類(如:胺碘酮,索他洛爾)抗心律失常藥物治療的患者。
莫西沙星和可能延長QT間期的藥物:西沙比利,紅黴素,抗精神病藥和三環類抗抑鬱藥,聯合用藥時可能存在累加效應。所以,應慎重與這些藥物合用。
莫西沙星在致心律失常的條件存在時應慎用,如:嚴重的心動過緩或急性心肌缺血。
和男性相比,由於女性患者往往擁有更長的QTc間期,她們對引發QTc間期延長的藥物可能更敏感。老年患者也更容易遭受藥物引發的QT間期延長的影響。
QT間期延長的程度隨著藥物濃度的增加而增加。所以不應超過推薦劑量。但是,在肺炎患者中沒有觀察到莫西沙星血藥濃度和QT間期延長相關。QT間期延長可以導致室性心律失常包括尖端扭轉型室速的發生危險增高。在莫西沙星治療的超過9000名患者的臨床研究中,沒有因QT間期延長導致的心血管的發病率或死亡率,但某些潛在條件可以增加室性心律失常的危險。
女性患者和老年患者對引發QTc間期延長的藥物更加敏感。
曾經報告莫西沙星可引起爆發性肝炎,並可能因此而導致肝衰竭(包括死亡病例)。如果發生了肝衰竭相關症狀,應建議患者在繼續治療前立即聯繫醫生。
曾經報告莫西沙星引起的大皰性皮膚反應,如Stevens-Johnson綜合徵或中毒性表皮壞死松解症。如果發生了皮膚和/或黏膜反應,應建議患者在繼續治療前立即聯繫醫生。
喹諾酮類使用可誘發癲癇的發作,對於已知或懷疑有能導致癲癇發作或降低癲癇發作域值的中樞神經系統疾病的患者,莫西沙星在使用中要注意。
在使用包括莫西沙星的喹諾酮類治療中有可能出現肌腱炎和肌腱斷裂,特別是在老年患者和使用激素治療的患者中。一旦出現疼痛或炎症,患者需要停止服藥並休息患肢。
有報導在使用包括莫西沙星在內的廣譜抗生素時出現偽膜性腸炎,因此,在使用莫西沙星治療中如患者出現嚴重的腹瀉時,需要考慮這個診斷,這一點很重要。在這種情況下需立即採取足夠的治療措施,在發生了嚴重腹瀉的患者中,禁忌使用可抑制胃腸蠕動的藥物。
重症肌無力患者應慎用莫西沙星,因為可加重症狀。
已經證實,喹諾酮類藥物能夠導致患者光敏反應。但是,在特別設計的臨床前和臨床研究中,沒有觀察到莫西沙星的光敏反應。另外,上市以來沒有臨床證據證明莫西沙星引起光敏反應。儘管如此,仍應建議患者避免在紫外線及日光下過度暴露。
在有些病例,如果在首次服用後已經發生過敏反應和變態反應,應該立即告知醫生。
在首次服用後極少的病例能夠發生由過敏性反應導致威脅生命的休克。在這些病例莫西沙星應停用並給予治療(如針對休克的治療)。
針對複雜盆腔感染患者(如伴有輸卵管-卵巢或盆腔膿腫)治療時,需考慮經靜脈給藥進行治療,而不推薦口服400mg莫西沙星片進行治療。
對於那些在臨床需關注鈉攝入量的患者(充血性心力衰竭,腎衰,腎病綜合症等),應考慮額外的鈉負荷。
因中樞神經系統(CNS)反應,包括莫西沙星在內的氟喹諾酮類藥物可能會損害患者的駕駛或操作機械的能力。
請將輸液器針頭垂直扎入橡膠塞內環中心,勿用力過大以避免膠塞受損。
孕婦及哺乳期婦女用藥
孕婦:人類在懷孕期間使用莫西沙星的安全性尚未被證實,兒童服用喹諾酮類可引起可逆性關節損傷,但是,尚未見報導這種作用出現於妊娠用藥者的胎兒。動物研究顯示莫西沙星有生殖毒性,但對人的潛在危險性尚不明確。因此,莫西沙星禁用於妊娠期的婦女。
哺乳期婦女:與其它喹諾酮類藥物相同,莫西沙星可造成未成年試驗動物負重關節的軟骨損傷。臨床前研究證實小量的莫西沙星可以分布到人類的乳汁中,尚缺乏哺乳期婦女的數據。因此,莫西沙星禁用於哺乳期的婦女。
兒童用藥
莫西沙星對兒童和青少年的療效和安全性尚未確定。
老年用藥
莫西沙星的藥代動力學不受年齡的影響。
藥物相互作用
臨床上未證實莫西沙星與下述藥物相互作用:阿替洛爾、雷尼替丁、鈣補充劑、茶鹼、口服避孕藥、格列本脲、伊曲康唑、地高辛、嗎啡、丙磺舒。對這些藥物不需要調整劑量。
抗酸藥、礦物質和多種維生素:莫西沙星與抗酸藥、礦物質和多種維生素同時服用會因為與這些物質中的多價陽離子形成多價螯合物而減少藥物的吸收。這將導致血漿中的藥物濃度比預期值低,因此,抗酸藥、抗逆轉錄病毒藥(如去羥肌苷)、其他含鎂或鋁的製劑、硫糖鋁、以及含鐵或鋅的礦物質,至少需要在口服莫西沙星4小時前或2小時後服用。
雷尼替丁:與雷尼替丁合併用藥並不改變莫西沙星的吸收參數。吸收參數(Cmax,tmax,AUC)的比較,表明胃PH值對莫西沙星從胃腸道的吸收沒有影響。
鈣補充劑:服用大劑量鈣補充劑時,僅輕微減少吸收速率而對吸收程度沒有影響。可以認為,大劑量鈣補充劑對莫西沙星的影響不具有臨床相關意義。
茶鹼:與人體外研究數據一致,莫西沙星對穩態時的茶鹼的藥代動力學無影響,提示莫西沙星對P450酶的1A2亞型無影響。
華法令:據觀察,莫西沙星與華法令同時服用未發現對藥代動力學,凝血酶原時間和其他凝血參數有影響。
國際標準化比值的改變(International Normalized Ratio, INR):曾有報導患者同時服用抗凝劑和包括莫西沙星在內的抗生素,抗凝活性升高。其危險因素包括患者的感染(及其炎症過程),年齡,和一般狀況。儘管莫西沙星和華法令的相互作用在臨床試驗中未經證實,但應監測INR,如有必要相應調整口服抗凝劑的劑量。
口服避孕藥:莫西沙星與口服避孕藥同時服用未發現相互作用。
抗糖尿病藥:格列本脲和莫西沙星同時服用未發現有臨床意義的相互作用。
伊曲康唑:莫西沙星與伊曲康唑同時服用時伊曲康唑的暴露(AUC)僅少量改變。伊曲康唑對莫西沙星的藥代動力學無顯著性影響。當服用伊曲康唑時同時給予莫西沙星不需要調整劑量,反之亦然。
地高辛:莫西沙星對地高辛的藥代動力學沒有嚴重影響,反之亦然。在健康受試者多劑量給藥達穩態後,莫西沙星將地高辛穩態Cmax提高約30%,而沒有影響AUC和波谷水平。
嗎啡:腸外給予嗎啡同時服用莫西沙星,並不減少口服莫西沙星的生物利用度,且Cmax(17%)僅稍有下降。
阿替洛爾:莫西沙星對阿替洛爾的藥代動力學無顯著性影響。健康受試者單次給藥時,藥時曲線下面積(AUC)邊緣增加(約4%),峰值濃度減少10%。
丙磺舒:在一項觀察丙磺舒對腎臟排泄功能影響的臨床研究中未發現丙磺舒對莫西沙星的全身清除率和腎臟清除率有明顯影響。
炭:同時口服炭及0.4g莫西沙星在體內能阻止80%藥物吸收,從而減少藥物的全身利用。藥物過量時,在吸收早期套用活性炭能阻止藥物的進一步全身暴露。靜脈給藥後,活性炭只能輕度減少藥物的全身暴露(約20%)。
食物和乳製品:食物(包括乳製品)的攝入不影響莫西沙星的吸收。因此,莫西沙星的服用時間不受進食的影響。
藥物過量
關於過量的研究資料非常有限,單次最大劑量1.2g和每日0.6g連續10天多次給藥在健康志願者中未發現有任何顯著的不良反應。一旦服用過量莫西沙星時,應根據患者臨床狀況採取適當支持治療。
在莫西沙星吸收階段的早期,口服活性炭後可有效防止莫西沙星系統暴露的過量增加。靜脈給予活性炭後只能輕微減少莫西沙星的系統暴露(約20%),且對靜脈給藥過量的作用有限。
藥理毒理
1. 藥理作用
(1) 作用機制
莫西沙星是具有廣譜活性和殺菌作用的8-甲氧基氟喹諾酮類抗菌藥。莫西沙星在體外顯示出對革蘭陽性菌、革蘭陰性菌、厭氧菌、抗酸菌和非典型微生物如支原體、衣原體和軍團菌具有廣譜抗菌活性。
殺菌作用機制為干擾拓撲異構酶Ⅱ和Ⅳ。拓撲異構酶是控制DNA拓撲和在DNA複製、修復和轉錄中關鍵的酶。
莫西沙星表現為濃度依賴性的殺菌活性。最低殺菌濃度和最低抑菌濃度基本一致。
莫西沙星對β-內醯胺類和大環內酯類耐藥的細菌亦有效。通過感染的實驗動物模型證實,莫西沙星體內活性高。
(2) 耐藥
導致對青黴素類、頭孢菌素類、氨基糖苷類、大環內酯類和四環素類耐藥的耐藥機制不影響莫西沙星的抗菌活性。莫西沙星和這些抗菌藥間無交叉耐藥性。至今未發現質粒介導的耐藥性出現。
莫西沙星的8-甲氧基部分與8-氫部分相比具有對革蘭陽性菌高活性和耐藥突變的低選擇性。龐大的7位二氮雜環取代基能阻止主動外排,該主動外排為氟喹諾酮耐藥機制。
體外試驗顯示經過多步變異才能緩慢地出現對莫西沙星的耐藥性。總之其耐藥率很低(10-7~10-10)。序列地將細菌暴露在低於莫西沙星MIC濃度時只能使MIC值有少量的增加。
與其它喹諾酮類藥物之間存在交叉耐藥。但是,一些對其它喹諾酮類耐藥的革蘭陽性菌和厭氧菌對莫西沙星敏感。
(3) 對人類腸道菌群的作用
在兩項志願者口服莫西沙星的研究中觀察到下列變化:大腸埃希菌,芽孢桿菌屬,普通擬桿菌,腸球菌,克雷伯氏菌屬和厭氧菌如雙歧桿菌,真桿菌和消化鏈球菌等的減少,這些變化在兩周內可以恢復正常,未發現艱難梭菌毒素。
(4) 體外試驗敏感數據
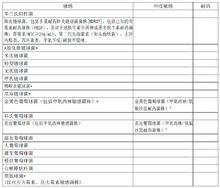 鹽酸莫西沙星氯化鈉注射液
鹽酸莫西沙星氯化鈉注射液*/**已經證實能對敏感菌導致的已批准的臨床適應症有效
+莫西沙星僅對由MecA基因介導的甲氧西林耐藥葡萄球菌的體外MIC值在其敏感範圍內。因此,如果發現這類菌株不推薦使用莫西沙星。
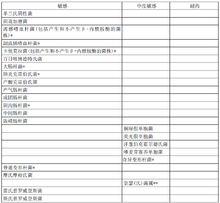 鹽酸莫西沙星氯化鈉注射液
鹽酸莫西沙星氯化鈉注射液*/**已經證實能對敏感菌導致的已批准的臨床適應症有效
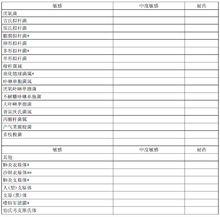 鹽酸莫西沙星氯化鈉注射液
鹽酸莫西沙星氯化鈉注射液*/**已經證實能對敏感菌導致的已批准的臨床適應症有效
對於某些細菌的獲得性耐藥率可能隨地理和時間而改變。局部耐藥是可能出現的,特別是治療嚴重感染時。上述體外敏感試驗結果可用來指導判斷微生物是否對莫西沙星敏感。
單劑量靜脈和口服給予0.4g莫西沙星的PK/PD比較。
需住院病人的AUC/MIC值大於125且Cmax/MIC為8~10為臨床治癒的期望值。門診病人的參數值通常較低,AUC/MIC大於30~40。
下表為單劑量靜脈和口服給予0.4g莫西沙星的PK/PD的計算值比較:
 鹽酸莫西沙星氯化鈉注射液
鹽酸莫西沙星氯化鈉注射液a)1h 輸液
2. 毒理研究
莫西沙星與其他喹諾酮類藥物一樣,毒性靶器官均為血液系統(狗及猴的骨髓細胞減少)、中樞神經系統(猴的驚厥)和肝臟(大鼠、狗及猴的肝酶升高、單細胞壞死),這些變化均於大劑量或長期套用莫西沙星後出現。
在狗體內進行的局部耐受性研究中,靜脈注射莫西沙星後未出現局部不耐受的徵象。經動脈內注射用藥後,動脈周圍軟組織可見炎性變化,提示應避免經動脈內注射使用莫西沙星。
致癌性、遺傳毒性
雖然有關莫西沙星致癌作用的常規長期研究尚未進行,但該藥進行了基因毒性體外和體內實驗。此外,對大鼠進行了對於人類的致癌作用加速實驗(誘癌/促癌試驗)。Ames實驗中4株為陰性,中國倉鼠卵巢HPRT的突變實驗和大鼠原發肝細胞的UDS實驗也均為陰性。與其他喹諾酮類一樣TA102的Ames實驗為陽性,體外實驗顯示大劑量莫西沙星(300ug/ml)可導致中國倉鼠的V79細胞出現染色體異常。然而,小鼠體內微核實驗為陰性結果。此外,體內實驗測定其對小鼠的顯性致死實驗為陰性。總之,體內實驗的結果充分反應了其體內的基因毒性。在大鼠的誘癌/促癌試驗中未發現其有致癌的證據。
光毒性
莫西沙星對光很穩定且潛在光毒性很低。體外實驗和動物實驗均顯示莫西沙星的光毒性較其他喹諾酮小。給小鼠一些喹諾酮類藥物並同時照射紫外線,這些喹諾酮類藥物可增加紫外線的光致癌作用。尚未進行莫西沙星的光致癌作用研究,在志願者的I期研究中證實莫西沙星無潛在的光毒性。
心電圖
高濃度的莫西沙星對心臟延遲整流鉀電流有抑制作用,因此導致QT間期延長。給狗口服大於90mg/kg莫西沙星進行毒理研究,導致血藥濃度大於16mg/l,引起QT間期延長,但未出現心律失常。僅當累積靜脈給藥高於50倍人用劑量(]0.3g/kg)後,可導致血藥濃度≥0.2g/l(高於靜脈給藥治療濃度的30倍),可見可逆的非致命的室性心律失常。
眼毒性
大鼠和猴的毒性試驗(反覆給藥6個月)顯示無眼毒性。在狗實驗中,給予高劑量(≥60mg/kg)時血漿濃度≥20mg/l,可引起視網膜電流圖的變化,個別動物出現視網膜萎縮。
關節毒性
眾所周知,喹諾酮類可以造成未成年實驗動物的承重關節軟骨的病變。可造成幼年狗的關節毒性的最小口服莫西沙星是推薦最大治療劑量(0.4g/50kg人體重)的4倍,其血藥濃度為推薦治療劑量時血藥濃度高2~3倍。
生殖毒性
以大鼠、兔和猴進行的生殖研究表明,莫西沙星可以通過胎盤。對大鼠(口服和靜脈注射)和猴(口服)的研究表明,給予莫西沙星後未顯示致畸作用和對生殖力的損害。兔靜脈給藥20mg/kg可觀察到骨骼畸形。該研究結果與已知的喹諾酮類藥物對骨骼發育的影響一致。在人治療濃度,猴和兔的流產發生率增多。在大鼠,當口服劑量為按mg/kg體重計算使血藥濃度在人治療劑量範圍內所推薦的最大藥物劑量的63倍時,會出現胎鼠體重減少、流產增多、輕度延長孕期和一些雌性和雄性幼鼠自發活動增加等現象。
藥代動力學
吸收和生物利用度
莫西沙星口服後迅速、幾乎完全被吸收。絕對生物利用度總計約91%。
在50~1200mg單次劑量和每日0.6g連服10天的藥代動力學呈線性。3天內達穩態。口服0.4g後0.5~4小時達到峰值3.1mg/l。每日一次0.4g口服後達到穩態時其峰濃度和谷濃度分別為3.2mg/l和0.6mg/l。
莫西沙星與食物同服能稍延長達峰時間約2小時並降低峰濃度約16%。吸收程度保持不變。由於AUC/MIC最能預測喹諾酮類藥物的抗菌作用,該影響與臨床無關。因此,莫西沙星給藥不受進食影響。
單劑量0.4g靜脈滴注1小時後,在滴注結束時血藥濃度達峰值約為4.1mg/l,與口服相比平均約增加26%。反映藥物暴露的藥時曲線下面積(AUC)約為39mg*h/l,與絕對生物利用度約為91%的口服給藥暴露(35mg*h/l)相比略高。
多劑量靜脈給藥(滴注1小時),每日0.4g給藥穩態峰、谷濃度分別為4.1至5.9及0.43至0.84mg/l。在給藥間隔內穩態藥物暴露比首劑約高30%。輸液1小時後觀測到病人穩態濃度為4.4mg/l。
分布
莫西沙星可以很快分布到血管外間隙。該藥的藥時曲線下面積(AUCnorm)高(6kg*h/l),穩態時表觀分布容積Vss約為2l/kg。唾液中藥物峰濃度比血藥濃度高。在0.02~2mg/l範圍的體外和體內試驗表明,無論藥物濃度如何,蛋白結合率約為45%。莫西沙星主要與血漿白蛋白結合,由於蛋白結合率低,游離峰濃度>10倍MIC。
莫西沙星在下列組織中達到高濃度:如肺(上皮液,肺泡巨噬細胞,支氣管組織),竇(篩竇,上頜竇,鼻息肉)和炎症損傷(斑蝥皰疹液),其總藥物濃度超過血藥濃度。組織間液有很高的游離藥物濃度(唾液、肌肉內、皮下)。
另外經檢測,在腹腔的組織及體液和女性生殖道中有高藥物濃度。
口服及靜脈單次劑量給藥0.4g後人體組織中的藥物平均峰濃度如下:
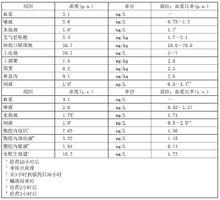 鹽酸莫西沙星氯化鈉注射液
鹽酸莫西沙星氯化鈉注射液不同靶組織中的峰濃度及血漿比率表明兩種單劑量0.4g的給藥方法的結果具有可比性。
代謝
莫西沙星經過第二階段的生物轉化後經過腎臟和膽汁/糞便以原形和硫化物(M1)和葡萄糖醛酸苷(M2)的形式排出。M1和M2隻是在人體內的相關代謝產物,均無微生物學活性。在體外試驗及I期臨床研究中,均未發現莫西沙星與其它有細胞色素P450酶參與的進行一相生物轉化的藥物有相互作用。代謝產物M1和M2的血藥濃度比母藥低,並與給藥途徑無關。對代謝物進行了充分的臨床前研究,表明代謝物是安全、可耐受的。
排泄
莫西沙星從血漿中被排出的平均半衰期約為12小時。口服0.4g藥物後的平均總體表觀清除率為179~246ml/min。腎清除率為24~53ml/min,提示腎臟通過腎小管能部分重吸收該藥。同時服用雷尼替丁和丙磺舒不改變藥物通過腎臟的排泄。(見下表)
莫西沙星的原形和第二階段的代謝產物在達到平衡後幾乎能完全回收,回收率為96~98%,且與給藥途徑無關,無氧化代謝的跡象。下表按照排泄途徑(腎與非腎,代謝與非代謝)和給藥方式對這一平衡給予了詳細說明。
0.4g單劑量給藥回收率(算數平均數±標準差(SD))
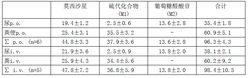 鹽酸莫西沙星氯化鈉注射液
鹽酸莫西沙星氯化鈉注射液老年
莫西沙星的藥代動力學不受年齡的影響。
性別
男性和女性受試者莫西沙星的藥代動力學參數(AUC,Cmax)相差33%。該AUC及Cmax的差別可歸因於體重不同而不是性別。因此藥物吸收不受性別影響,該差別無臨床意義。
種族差異
對高加索人種、日本人、黑人及其他種族進行了可能存在的種族差異試驗。藥代動力學試驗表明無臨床相關的種族差異。
兒童
未對兒童患者進行莫西沙星藥代動力學研究。
腎損害
腎功能受損的病人(包括肌酐清除率<30ml/min/1.73m2)和慢性透析,如血液透析和持續性不臥床腹膜透析的病人的莫西沙星藥代動力學無明顯改變。
肝損害
肝功能受損的病人(Child Pugh A to C)與健康志願者或肝功能正常的患者血漿藥物濃度在臨床上無明顯差別。
中國人PK研究
[u]單劑量給藥[/u]:10名健康受試者按拉丁方設計,隨機分為3組(第一組3人,第二組3人,第三組4人),分別交叉給藥0.2g、0.3g、0.4g本品,輸液時間均為90min,每次試驗間隔為7天。(註:國外本品的輸液時間為30-60min不等。根據中國健康受試者心臟所能耐受的輸液速率計算出本品在試驗中的輸液時間為90min。)
所得藥時曲線均較好地符合二房室模型。具體參數如下:
 鹽酸莫西沙星氯化鈉注射液
鹽酸莫西沙星氯化鈉注射液[u]多劑量給藥[/u]:10名健康受試者每日一次靜脈滴注本品0.4g,連續輸注10天。
血藥濃度約在第4天達穩態。達穩態後的平均峰濃度為5.351±0.533mg/L,平均谷濃度為1.084±0.177mg/L,經計算後波動係數為1.39。穩態後AUCss0~24與第一次服藥後的AUC0~∞無顯著性差異。半衰期約為14h,表明連續給藥10天后藥物在體內無蓄積。
中國人PK試驗結果與國外文獻報導相比,其峰濃度有差異,原因主要是靜脈輸液速率不同所致,而藥物的分布及消除過程基本一致。
貯藏
遮光,密閉,在15℃以上保存。在原包裝中貯存。不要冷藏或冷凍。冷藏可發生沉澱,室溫下可再溶解。因此建議不要將鹽酸莫西沙星氯化鈉注射液貯藏在冰櫃中。將藥品置於兒童觸及不到的地方。
包裝
無色玻璃瓶包裝。每瓶250毫升,每盒1瓶。
有效期
36個月
執行標準
進口藥品標準JX20030339
