簡介
電解鈍化(electrolysis passivation)是指電化學鈍化。一種陽極金屬的電化學溶解陡然大幅度減緩乃至幾乎不溶的現象。和化學鈍化一樣,電化學鈍化也是由於金屬表面形成了一層難溶的緻密、牢固的氧化物或別的化合物薄膜,隔開了金屬和溶液的接觸(成相理論),或者吸附上了一層氧或含氧粒子,使金屬表面的反應能力大大降低所致 。
鈍化曲線
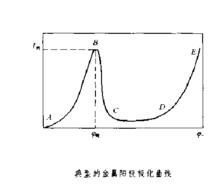
各種金屬電化學鈍化的難易,可以通過測定其鈍化曲線即陽極極化曲線來確定。圖示為恆電位法穩態側定的典型的金屬陽極極化曲線。曲線的AB段表明,電流(金屬的電化溶解速度)隨極化電位的提高而增大,金屬正常電化溶解。當極化電位提高超過B點時,電流反而陡降至C點,這說明金屬已發生鈍化。在CD段里,金屬始終處於比較穩定的鈍態,電流實際上不隨極化電位改變,稱其為限溶解電流,極化電位提高過D點以後。電流又重新增大.這可能是陽極金屬的電化溶解速度重新增大(如出現鈍化膜在高極化電位下氧化成可溶性高價離子的所謂“超鈍化現象”),或者發生了別的電極過程(如氧化析出)。非惰性不溶陽極就屬於後一種情況。相當於B點的極化電位稱為臨界鈍化電位。與之對應的電流(電流密度)稱為臨界鈍化電流(電流密度) 。
 圖示
圖示保持陽極鈍態
臨界鈍化電位愈低的金屬。愈易鈍化。在電化冶金中,陽極金屬的鈍化對於可溶陽極電解精煉以及電鍍、化學電源十分有害,它使槽電壓升高和電耗增大的同時,嚴重阻礙待精鍊金屬的溶解,極端情況下甚至會停止溶解而變為析出氧氣。採取選擇適當的電流密度、攪拌和加熱溶液,調整溶液pH,通入還原性氣體,添加去鈍化劑(如Cl 離子),使陰極極化(如周期反向電解、脈衝電解、等措施,均可減輕乃至完全消除電解鈍化現象。而在不溶陽極的金屬電解提取或金屬防腐的情況下,則需利用陽極鈍化現象來延長不溶陽極的壽命和確保陰極沉積金屬的質量,或阻止受保護的金屬被腐蝕。往陽極金屬摻入易鈍化的合金元素(如鐵中摻入鎳、鉻、鉛中摻入銀、鈣)、除去溶液中的去鈍化劑(特別是Cl 離子),避免陽極表面的機械損傷等,都是保持陽極鈍態的有效辦法 。

