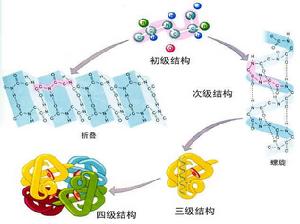
 蛋白質因受某些物理或化學因素的影響,分子的空間構象被破壞,從而導致其理化性質發生改變並失去原有的生物學活性的現象稱為蛋白質的變性作用(denaturation)。變性作用並不引起蛋白質一級結構的破壞,而是二級結構以上的高級結構的破壞,變性後的蛋白質稱為變性蛋白。
蛋白質因受某些物理或化學因素的影響,分子的空間構象被破壞,從而導致其理化性質發生改變並失去原有的生物學活性的現象稱為蛋白質的變性作用(denaturation)。變性作用並不引起蛋白質一級結構的破壞,而是二級結構以上的高級結構的破壞,變性後的蛋白質稱為變性蛋白。如果變性條件劇烈持久,蛋白質的變性是不可逆的。如果變性條件不劇烈,這種變性作用是可逆的,說明蛋白質分子內部結構的變化不大。這時,如果除去變性因素,在適當條件下變性蛋白質可恢復其天然構象和生物活性,這種現象稱為蛋白質的復性(renaturation)。例如胃蛋白酶加熱至80~90℃時,失去溶解性,也無消化蛋白質的能力,如將溫度再降低到37℃,則又可恢復溶解性和消化蛋白質的能力。
分離包含體並復性蛋白質的操作步驟並不複雜,從破碎細胞開始,然後將細胞勻漿離心,回收包含體後,加入變性劑溶解包含體,使之成為可溶性伸展態,再除去變性劑使表達產物摺疊恢復天然構象及活性。但在實際研究中發現,在體外摺疊時,蛋白質分子間由於存在大量錯誤摺疊和聚合,復性效率往往很低。究其原因,蛋白質的立體結構雖然由其胺基酸順序決定,然而伸展肽鏈摺疊為天然活性結構的過程還受到周圍環境的影響。
為了有的放矢地開發輔助蛋白質復性的技術,研究工作者紛紛開展了對蛋白質摺疊機制的探討。目前有兩種不同的假設:一種假設認為,肽鏈中的局部肽段先形成一些構象單元,如α螺鏇、β摺疊、β轉角等二級結構,然後再由二級結構單元的組合、排列,形成蛋白質三級結構;另一種假設認為,首先是由肽鏈內部的疏水相互作用導致一個塌陷過程,然後經逐步調整,形成不同層次的結構。儘管是不同的假設,但很多學者都認為有一個所謂‘熔球態’的中間狀態。在熔球態中,蛋白質的二級結構已基本形成,其整體空間結構也初具規模。此後,分子立體結構再做一些局部調整,最終形成正確的立體結構[2]。總之,蛋白質摺疊的具體步驟可用下式描述:
U→I→N
↓
A
即伸展態U經過早期變化成為中間體I,然後由中間體過渡到最後的天然態N。但是從中間體摺疊為天然態的同時,另有一條旁路,即中間體相互聚集為凝聚物A(包含體)。在摺疊反應中,從伸展態到中間體的形成是非常快速的,一般在毫秒範圍內完成,但從中間體轉變為天然態的過程比較緩慢,是反應的限速步驟。當溶液中離子強度或變性劑濃度很低,又無其它輔助手段存在時,聚集趨勢占主導地位,導致蛋白質的自發復性效率極低。
一般認為,蛋白質在復性過程中,涉及兩種疏水相互作用,一是分子內的疏水相互作用,二是部分摺疊的肽鏈分子間的疏水相互作用。前者促使蛋白質正確摺疊,後者導致蛋白質聚集而無活性,兩者互相競爭,影響蛋白質復性收率[3]。因此,在復性過程中,抑制肽鏈間的疏水相互作用以防止聚集,是提高復性收率的關鍵。
2. 蛋白質復性研究的初期成果
80年代後期,人們開展了廣泛的蛋白質復性研究。例如,Carlson等發現,單克隆抗體具有協助蛋白質復性的作用[4];Cleland等發現,向稀釋的變性蛋白質溶液中加入適當濃度的聚乙二醇,可抑制蛋白質復性過程中的凝聚沉澱,使蛋白質復性收率提高兩倍[5];Hagen等利用反膠團萃取人工變性的蛋白質後去除變性劑進行復性,復性率可達100%[6](但由於變性劑的存在,萃取率很低);Batas等利用凝膠過濾色譜介質的分子篩作用可防止變性蛋白質間的接觸和凝聚,輔助其正確摺疊[7];Zardeneta等利用去污劑及混合膠團,成功地輔助了脲變性硫氰酸酶復性[8]。
3. 環糊精與直鏈糊精輔助蛋白質復性的研究
1995年,Karuppiah 和Sharma發表文章,介紹了使用環糊精輔助碳酸酐酶B的復性[9]。環糊精由澱粉通過環糊精葡萄糖基轉移酶降解製得,是由D-吡喃葡萄糖單元以α-1,4-糖苷鍵相互結合成互為椅式構象的環狀低聚糖,其分子通常含有6~12個吡喃葡萄糖單元。有實用意義的是含6、7、8個吡喃葡萄糖單元的α、β、γ-環糊精,但α-環糊精空腔較小,γ-環糊精價格昂貴,常用的是β-環糊精[10]。環糊精的特徵是能形成包絡化合物,客體分子從寬口端進入其分子空腔。包絡物的形成主要靠非共價鍵相互作用如范德華力、氫鍵、疏水相互作用、幾何形狀匹配等。利用環糊精的疏水性空腔結合變性蛋白質多肽鏈的疏水性位點,可以抑制其相互聚集失活,從而促進肽鏈正確摺疊為活性蛋白質。
1999年,Sundari等報導了用直鏈糊精輔助胰島素、碳酸酐酶和雞蛋白溶菌酶復性[11],發現直鏈糊精基本上能夠模擬環糊精在輔助蛋白質復性方面的作用,而且具有這樣一些優點:直鏈糊精的螺鏇結構形成一個疏水性空管,可以結合更多的蛋白質分子;在水中溶解度較高,有利於提高復性酶濃度和實驗操作;價格比環糊精便宜,實際套用前景廣闊。
4. 分子伴侶輔助蛋白質復性的研究
近來,越來越多的有關蛋白質摺疊的研究已轉向利用分子伴侶GroE家族。有些學者已成功地利用分子伴侶在體內和體外輔助蛋白質復性[12、13]。但分子伴侶在實際套用中尚存在費用高並需要與復性蛋白質分離等缺點,因此研究開發分子伴侶的重複利用性及穩定性是實現其套用的關鍵。
GroEL具有結合蛋白質的作用,相當於變性蛋白質的親和配基。固定化GroEL柱(固定床)相當於變性蛋白質的親和吸附層析柱,從而可提高樣品的處理量,並使蛋白質在復性的同時得到濃縮和純化。其特點在於:①不僅可以解決分子伴侶的重複利用問題,而且由於固定床的利用(近於平推流),可提高分子伴侶的利用效率;②由於採用連續操作,原料處理量大,產品可以得到濃縮、純化;③易於建立相關的模型,對於放大生產具有重要的指導作用。Teshima等利用固定化分子伴侶,在體外輔助了澱粉酶、碳酸酐酶、DNA酶的摺疊復性[14]。
還有報導利用“小分子伴侶”對目標蛋白質進行復性[15、16]。“小分子伴侶”是指GroEL的一個片段,而這個片段並不是GroEL的水解產物,而是由基因重組後包括GroEL191-345胺基酸殘基片段(16.7kD)或191-376胺基酸殘基片段(21kD)密碼的基因片段在大腸桿菌中的表達產物。它們能有效地促進親環蛋白A、硫氰酸酶以及芽孢桿菌RNA酶的復性。由於“小分子伴侶”分子較小,更適合於固定化,且不需另加復性輔助因子(如GroES和ATP等),因此具有很大的套用前景。 5. 人工分子伴侶在蛋白質復性中的套用
受蛋白質分子伴侶輔助蛋白質復性的啟發,Rozema和Gellman對人工分子伴侶體系(去污劑+環糊精)輔助碳酸酐酶和雞蛋白溶菌酶復性進行了研究[17、18]。與分子伴侶GroEL+ATP輔助復性的作用機制相似,其復性過程分為兩步進行:第一步捕獲階段,在變性蛋白質溶液中加入去污劑,去污劑分子通過疏水相互作用與蛋白質的疏水位點結合形成複合體,抑制肽鏈間的相互聚集;第二步剝離階段,加入環糊精,由於環糊精分子對去污劑分子有競爭性吸附作用,去污劑分子被剝離下來,從而使多肽鏈在此過程中正確摺疊為活性蛋白質[17、18]。其反應機制可用下式表示:
U→U-dn→→→U-dn-m→→→F→N
即伸展態U首先與去污劑d形成複合物U-dn,加入環糊精後,小分子去污劑被逐次剝離下來,變為部分摺疊、不含去污劑分子的非活性狀態F,進而摺疊為天然活性蛋白質N。
與GroE等蛋白質分子伴侶相比,聯合使用去污劑和環糊精作為人工分子伴侶輔助蛋白質復性具有明顯的優點:①人工分子伴侶不屬於蛋白質,不易受環境影響而失活,操作條件較為寬鬆;②去污劑和環糊精均可直接購買,省去分離純化的步驟;③去污劑與環糊精的分子量較小,容易與蛋白質分離,有利於提高工業生產效率。
