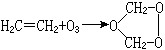定義
含臭氧離子O婣的化合物。其中O婣離子呈 V形,如在NaO3中O婣的夾角為100°,O─O鍵長為1.2埃。
形式
鹼金屬、鹼土金屬、銨離子的臭氧化物有LiO3·4NH3、KO3、Ca(O3)2、NH4O3。有機臭氧化物有烯烴(如乙烯)的加成產物:
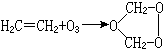
2MO3─→2MO2+O2
(M代表金屬)其熱穩定性隨鈉、鉀、銣、銫順序而遞增。鉀、鈉的臭氧化物可作為高能氧化劑。
形成
ko3為棕紅色順磁性.在室溫下分解為KO2和O2.鹼土金屬的臭氧化合物在液氨中穩定.
乾燥的鉀/銣/銫/鍅的氫氧化物固體與臭氧反應和臭氧通入它們的液氨溶液均可得到相應臭氧化物.
6CsOH+4O3====4CsO3+CsOH.H2O(水合晶體)+O2
 KO3
KO3K+O3==(NH3,l)===KO3
臭氧化物與水反應,放出O2.
4RbO3+2H2O=====4RbOH+5O2
鹼金屬的臭氧化物在常溫下緩慢分解,生成超氧化物與氧氣.