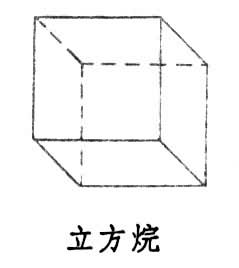
結構
立方烷的八個碳原子位於立方體的頂點,互以單鍵相連,是一種籠形結構,張力很高的五縮環體系。八個碳原子對稱的排列在立方體的八個角上。C原子以sp3雜化軌道成鍵,分子為非極性分子。在催化劑作用下,容易發生異構化。製法
可以溴代環戊烯酮的二聚體經一系列複雜反應,最後從甲醇溶液中結晶析出;也可通過光化學反應合成;也可由環丁二烯與2,5-二溴對苯醌合成。合成路線
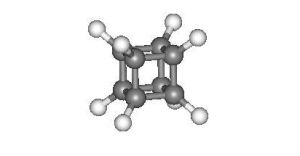 立方烷
立方烷第一部分:合成立方烷的前體2-溴代環戊二烯酮
在溶劑四氯化碳中,N-溴代丁二醯亞胺上的溴原子取代了2-環戊烯酮烯丙位上的氫,生成化合物1.2,然後在正戊烷-二氯甲烷混合溶劑中將其進一步溴化得到三溴代物1.3,後者再在乙醚中被二甲胺消除兩分子溴化氫便可得到2-溴代環戊二烯酮1.4。
第二部分:合成立方烷
在第二部分中,2.1首先自發地二聚為2.2,這是一個迪爾斯-阿爾德反應,與環戊二烯二聚為雙環戊二烯較為相似。因為每個溴原子都需要與另一溴原子以及羰基保持最小的位阻,另外生成內型產物的過渡態中有次級軌道作用,所以這步反應只生成內型產物,這是後續步驟成功的前提。接著在溶劑苯中,用對甲苯磺酸催化,以乙二醇保護兩個羰基,使其成為縮酮。其中一個被保護的羰基在鹽酸水溶液的作用下會被選擇性去保護,而得到2.3。
在下一步中,內型產物2.3(兩個碳碳雙鍵較為接近)通過光化學2+2環加成反應形成了籠狀化合物2.4。在氫氧化鉀的作用下,α-溴代酮通過法沃斯基重排而縮環,轉變為羧酸2.5。隨後,在氯化亞碸的作用下將羧基轉為醯氯,後者與過氧化叔丁醇反應,在吡啶中生成了叔丁基過氧酯2.6。將2.6加熱後可進行脫羧反應變為2.7。同樣地,將另一個羰基去保護,得到2.8,然後以相同的手法通過法沃斯基重排得到2.9,再脫羧得到2.10與2.11,最後在甲醇溶液中析出結晶而得到產品。