基本概念
指包括生物製品在內的生物體的初級和次級代謝產物或生物體的某一組成部分,甚至整個生物體用作診斷和治療的醫藥品。
藥物來源
正常機體之所以能保持健康狀態,具有抵禦和自我戰勝疾病的能力,正是由於生物體內部不斷產生各種與生物體代謝緊密相關的調控物質,如蛋白質、酶、核酸、激素、抗體、細胞因子等,通過它們的調節作用使生物體維持正常的機能。根據這一特點,可以從生物體內提取這些物質作為藥。
生物藥物的原料來源:
天然的生物材料:人體、動植物、微生物和各種海洋生物。
隨著生物技術的發展,有目的人工製得的生物原料成為當前生物製藥原料的重要來源,如用基因工程技術製得的微生物或細胞。
藥物特性
藥理學特性
(1)、治療的針對性強
細胞色素c用於治療組織缺氧所引起的一系列疾病。
(2)、藥理活性高
注射用的純ATP可以直接供給機體能量。
(3)、毒副作用小、營養價值高
蛋白質、核酸、糖類、脂類等生物藥物本身就直接取自體內。
(4)、生理副作用時有發生
生物體之間的種屬差異或同種生物體之間的個體差異都很大,所以用藥時會發生免疫反應和過敏反應。
特殊性
(1)、原料中的有效物質含量低
激素、酶在體內含量極低。
(2)、穩定性差
生物藥物的分子結構中具有特定的活性部位,該部位有嚴格的空間結構,一旦結構破壞,生物活性也就隨著消失。酶,很多理化因素使其失活。
(3)、易腐敗
生物藥物營養價值高,易染菌、腐敗。生產過程中應低溫、無菌。
(4)、注射用藥有特殊要求
生物藥物易被腸道中的酶所分解所以多採用注射給藥,注射藥比口服藥要求更嚴格,均一性、安全性、穩定性、有效性。理化性質、檢驗方法、劑型、劑量、處方、儲存方式。
檢驗特殊性
由於生物藥物具有生理功能,因此生物藥物不僅要有理化檢驗指標,更要有生物活性檢驗指標。
藥物分類
結構分類
按結構分類有利於比較一類藥物的結構與功能的關係、分離製備方法的特點和檢驗方法。
(1)、胺基酸及其衍生物類藥物
天然胺基酸和胺基酸混合物及衍生物。蛋氨酸可防治肝炎、肝壞死和脂肪肝,谷氨酸可用於防治肝昏迷、神經衰弱和癲癇。5-羥色氨酸。
(2)、多肽和蛋白質類藥物
化學本質性同,分子量有差異。蛋白質類藥物:血清白蛋白、丙種球蛋白、胰島素;多肽類藥物:催產素、胰高血糖素。
(3)、酶和輔酶類藥物
酶類藥物按功能分為:消化酶(胃蛋白酶、胰酶、麥芽澱粉酶)、消炎酶(溶菌酶、胰蛋白酶)、心血管疾病治療酶(激肽釋放酶擴張血管降血壓)等。輔酶類藥物在酶促反應中傳遞氫、電子和基團的作用,輔酶藥物已廣泛用於肝病和冠心病的治療。
(4)、核酸及其降解物和衍生物類藥物
DNA可用於治療精神遲緩、虛弱和抗輻射,RNA用於慢性肝炎、肝硬化和肝癌的輔助治療,多聚核苷酸是干擾素的誘導劑。
(5)、糖類藥物
抗凝血、降血脂、抗病毒、抗腫瘤、增強免疫功能和抗衰老。
(6)、脂類藥物
磷脂類:腦磷脂、卵磷脂可用於治療肝病、冠心病和神經衰弱症。脂肪酸降血脂、降血壓、抗脂肪肝。
(7)、細胞生長因子
干擾素、白細胞介素、腫瘤壞死因子等。
(8)、生物製品類
從微生物、原蟲、動物和人體材料直接製備或用現代生物技術、化學方法製成作為預防、治療、診斷特定傳染病或其它疾病的製劑。
按來源分類
有利於對不同原料進行綜合利用、開發研究。
(1)、人體組織來源
療效好、無副作用,來源有限。人血液製品類、人胎盤製品類、人尿製品類。
(2)、動物組織來源
動物臟器,來源豐富、價格低廉、可以批量生產。但由於種屬差異,要進行嚴格的藥理毒理實驗。
(3)、植物組織來源
中草藥,酶、蛋白質、核酸。
(4)、微生物來源
抗生素、胺基酸、維生素、酶。
(5)、海洋生物來源
動植物、微生物。
功能和用途
(1)、治療藥物
腫瘤、愛滋病、心腦血管疾病等。
(2)、預防藥物
傳染性強的疾病,疫苗、菌苗、類毒素。
(3)、診斷藥物
速度快、靈敏度高、特異性強。免疫診斷、酶診斷、放射性診斷、基因診斷試劑。
(4)、其它
生化試劑、保健品、化妝品、食品、醫用材料。
藥物製備
介紹
原材料和藥物種類和性質各不性同,提取和分離方法也有很大差異。
選擇預處理
(1)、原料選擇原則
有效成分含量高,原料新鮮,來源豐富、易得,產地較近,原料中雜質含量少,成本低。
(2)、預處理與保存
預處理:就地採集後去除結締組織、脂肪組織等不用的成分,將有用成分保鮮處理,收集微生物原料時,要及時將菌體與培養液分開,進行保鮮處理。
保存方法:冷凍法,適用於所有生物原料,-40℃;有機溶劑脫水法,丙酮,適用於原料少、價值高,有機溶劑對原料生物活性無影響;防腐劑保鮮,常用乙醇、苯酚等,適用於液體原料,如發酵液、提取液。
藥物提取
(1)、組織與細胞的破碎
常用破碎方法:磨切法,機械破碎法,設備為組織搗碎機、膠體磨、勻漿器、球磨機。壓力法,加壓和減壓,設備有法蘭西壓釜。反覆凍融法。超音波震盪破碎法,局部發熱,對活性有損失。自溶法或酶解法。
(2)、提取
根據具體對象選擇提取試劑,常用水、緩衝溶液、鹽溶液、乙醇、有機溶劑(氯仿、丙酮)。提取劑的用量,次數,時間,保證充分提取,且不變性。
提取方法
沉澱法(鹽析、有機溶劑、等電點);按分子大小分離(超濾、透析、層析、離心);電荷(離子交換、層析、電泳、等電聚焦);親和層析法(酶與底物、抗原與抗體、激素與受體)。
核酸類藥物
核酸類藥物生產方法提取法和發酵法。
糖類藥物
非降解法適用於從含一種粘多糖的動物組織中提取粘多糖,用水或鹽。
降解法適用於從組織中提取結合比較牢固的粘多糖,酶解。
分離用沉澱和離子交換。
脂類藥物
提取,用有機溶劑將所需成分從原料中溶解出來醇、氯仿、甲醇、水。純化,沉澱法、層析法、離子交換法。
胺基酸類藥物
胺基酸的生產:蛋白質水解,鹽酸水解迅速、完全,色氨酸被破壞,絲氨酸部分破壞;鹼水解易產生消鏇作用;酶水解不完全。發酵法,從發酵液中提取。和學合成與酶促合成法,化學合成產物混鏇需拆分,酶促合成效果較好。
分離方法:沉澱法(溶解度差異),吸附法(吸附能力差異),離子交換法(所帶電荷不同)。
市場現況
行業資產規模
據最新資料顯示,2012年4季度,生物藥品製造業資產規模增速扭轉了自2011年下半年以來的持續下滑態勢。2012年末,我國生物藥品製造業總資產達1848.07億元,同比增長14.9%,增速比上年同期下降3.97個百分點,比前三季度增長1.17個百分點 。
 生物藥品製造業總資產及同比增速
生物藥品製造業總資產及同比增速圖表2009年以來我國生物藥品製造業總資產及同比增速
由於我國生物醫藥行業起步較晚,上游技術同國外相比落後5年,下游技術卻比國外至少相差15年,產品多集中在較為低端的仿製疫苗、血液製品行業,技術壁壘較低,行業仍以中小型企業為主,大型企業占比偏低。2012年末,我國生物藥品製造業中,小型企業資產占比增至38.02%,比前三季度增長1.12個百分點,大型企業資產占比下滑至17.17%,比前三季度下降0.72個百分點。
圖表 2010年以來我國生物藥品製造業資產按企業規模分布
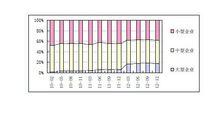 我國生物藥品製造業資產按企業規模分布
我國生物藥品製造業資產按企業規模分布供給現況
2012年,疫苗等生物製品批簽發量總體呈回升態勢,疫苗企業的批簽發量正逐步恢復。據中國食品藥品檢定研究院統計數據顯示,2012年,甲、B型肝炎聯合疫苗、肺炎疫苗、狂犬疫苗、b型流感嗜血桿菌結合疫苗、麻風二聯疫苗等疫苗的批簽發量增幅超過20%,分別同比增長136.41%、42.30%、39.76%、34.83%、26.51%,由於MMR(麻腮風三聯疫苗)完全替代麻疹、麻風、麻腮是疫苗市場的未來發展趨勢,腮腺炎、麻疹疫苗、風疹疫苗等批簽發量持續下降,批簽發量分別同比下降43.48%、47.03%、6.37%。
圖表2012年我國主要疫苗批簽發量及同比增速單位:萬人份,%
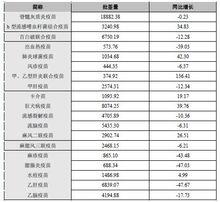 主要疫苗批簽發量
主要疫苗批簽發量
