玻恩-蘭德公式
玻恩-蘭德公式:
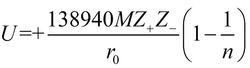 玻恩-蘭德公式
玻恩-蘭德公式在公式中,U表示離子晶體的晶格能,M表示馬德隆常數(與離子晶體結構有關),Z+,Z-表示晶體中陰、陽離子電荷。r0相鄰陰、陽離子間距。U以KJ/mol為單位,r0以pm為單位。
| 離子的晶體類型 | NaCl 型 | CsCl型 | CaF2型 | 閃鋅礦型 | 纖鋅礦型 |
| M | 1.74756 | 1.76767 | 5.03878 | 1.63805 | 1.64132 |
推導過程
晶格能的理論計算是依據靜電作用定律,即陰、陽離子間的吸引力與電子之間、核之間的排斥力達到平衡時,體系能量達到最低。計算說明,陰、陽離子在晶體中比單獨離子對中更穩定。在實際的三維晶體結構,以NaCl(s)為例,每個Na+有最鄰近的6個Cl-(r0),有次鄰近的12個Na+(1.414r0),有次鄰近的8個Cl-(1.732r0)等,因此,受到的靜電作用能為
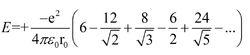 玻恩-蘭德公式
玻恩-蘭德公式括弧中數值收斂於1.74756,此數成為馬德隆常數(Madelung constant)
馬德隆常數(M)與離子晶體結構有關,上表列出了典型無機晶體結構的馬德隆常數。
由於陰、陽離子的電子之間、原子核之間存在排斥作用,排斥能正比於1/r^n,所以
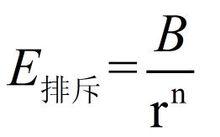 玻恩-蘭德公式
玻恩-蘭德公式上式中,B為比例常數,n為玻恩指數,n與離子的電子構型的關係如下表所示。正負離子的電子構型不同時,取各自玻恩指數的平均值。
| 離子的電子構型 | He | Ne | Ar | Kr | Xe |
| n | 5 | 7 | 9 | 10 | 12 |
考慮靜電作用能和排斥能,1mol離子晶體的總能量為
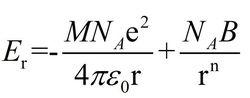 玻恩-蘭德公式
玻恩-蘭德公式晶體最穩定狀態是在r=r0時,所以上式必有極值,則Er對r的一階導數應為0,這樣可求出常數B:
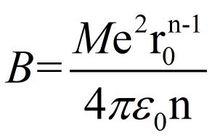 玻恩-蘭德公式
玻恩-蘭德公式把B值帶入Er公式中,當r=r0時,並帶入所有常數,若晶體中的陰、陽離子電荷為Z+,Z-,得到玻恩-蘭德公式
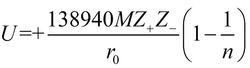 玻恩-蘭德公式
玻恩-蘭德公式用此公式計算所得的NaCl的晶格能為753.5KJ/mol,與玻恩-哈伯循環推算的結果相近。
