簡介
基本熱力學關係的含義
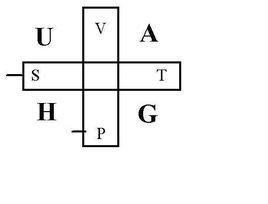
基本熱力學關係(basic relation of thermody-namics)是熱力學的一個基本規律,指熱力學中關於熱學參量溫度、熵和力學參量壓力、體積之間的微分關係.對於粒子數不變的熱力學系統,在只考慮膨脹作功時,可以給出四個熱力學函式U, H, F和G,它們分別表示內能、熵、自由能和吉布斯函式。
基本熱力學關係的套用
基本熱力學關係式共有11個。從這11個基本關係式出發,可以導出許多其它衍生關係式,它們表示出各不同物理量間的相互關係,利用它們可以幫助我們由易於直接測量的物理量出發以計算難於直接測量的物理量的數值。
基本熱力學關係式
基本關係式
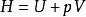 基本熱力學關係
基本熱力學關係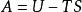 基本熱力學關係
基本熱力學關係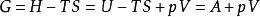 基本熱力學關係
基本熱力學關係Gibbs方程
又稱為恆組成均相封閉系統的熱力學基本方程。
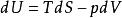 基本熱力學關係
基本熱力學關係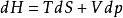 基本熱力學關係
基本熱力學關係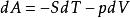 基本熱力學關係
基本熱力學關係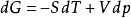 基本熱力學關係
基本熱力學關係麥克斯威關係式
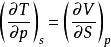 基本熱力學關係
基本熱力學關係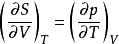 基本熱力學關係
基本熱力學關係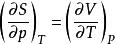 基本熱力學關係
基本熱力學關係