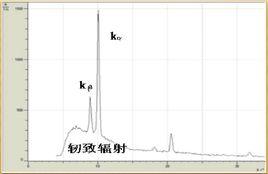
吸收邊介紹
X光若要電離某一殼層(如K層)的電子,其能量E必須大於該殼層的電子結合能Ek,由波長等於hc/E知,波長必須小於hc/Ek,越接近此值,越容易激發電離,吸收係數變大;但一旦波長大於前面所說的極限值,吸收係數會突然下降。因而在極值附近吸收係數有一個突變,這個突變對應的波長是吸收限,這個突變成為吸收邊或吸收突躍 。
計算方法
與最小激發電壓V0(KeV)的關係如下式:
 吸收邊
吸收邊結構理論
在X射線吸收譜中,吸收邊之上60eV以內的低能區的譜出現強的吸收特性,稱之為近邊吸收結構(XANES)。它是由於激發光電子經受周圍原子的多重散射造成的。它不僅反映吸收原子周圍環境中原子幾何配置,而且反映凝聚態物質費米能級附近低能位的電子態的結構。因此成為研究凝聚態物質的有用工具 。
1913 年英國物理學家H.莫塞萊研究了許多種元素的X射線標識譜(見X射線譜),發現譜線頻率的二次方根與該元素在元素周期表中排列的順序號成線性關係。他認識到這些標識譜是由於原子內層電子躍遷而產生。莫塞萊把各元素的Kα線系和Lβ線系的頻率表達為:
vKα= Rc( Z- σK)2(1/12-1/22)
vLβ= Rc( Z- σL)2(1/22-1/32)
式中 R是里德伯常數, Z是原子序數, σ是禁止因子, c是光速。他發現各元素 σK和 σL分別都近似等於1和7.4。對於其他線系則不再適用。
莫塞萊利用上述規律,並用實驗測出的X射線標識譜線的頻率來確定元素在周期表上排列的序號Z,發現只在Co—Ni,Ar—K,Te—I等相鄰元素處與原來按原子量大小排列的次序不符。改動後能使周期表上元素的化學、物理性質的周期性規律更符合實際。因此莫塞萊把按X射線譜排列的序號稱為原子序數,認為這正是元素原子核所帶的正電荷數,也是決定元素化學、物理性質的最主要因素。後來把莫塞萊定律推廣到原子光譜中,用來描述光譜項值的二次方根與原子序數的線性關係,由此而畫出的圖稱莫塞萊圖。
量子力學證明,描述各元素X射線標識譜規律的莫塞萊定律只是一種近似的規律。但它曾對確定原子序數,預言當時還未發現的元素,研究等電子離子序列光譜和原子結構都有過重要作用。