基本原理
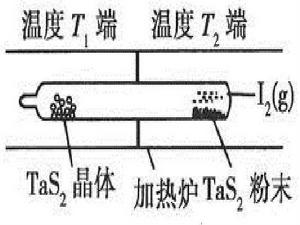
化學遷移反應(CTR):早在十九世紀中葉,Bunsen在敘述火山噴氣中含HCl時,提到過FeO能隨發生遷移。這一遷移基於如下的一個可逆反應:
FeO(固)+HCl(氣)⇌2FeCl(氣)+3HO(氣)
FeO在高溫下被HCl所氯化生成了揮發性的FeCl,而當溫度降低時生成的FeCl又可重新變成FeO,這樣,FeO就發生了一個從原固相混合物所在的“區域”(源區)到新的“ 區域” (澱積區或還原區)的遷移過程。在這一過程中,遷移的物質對象是FeO稱之為源物質,而僅起一種介質作用的HCl,則被稱作輸運劑。
我們把上述的整個化學反應過程,,稱作化學遷移反應。
所謂化學遷移反應是這樣一種化學遷移過程, 在這一過程中, 藉助於適當的輸運劑與源物質反應, 形成一種氣態化合物該氣態化合物經過化學遷移或物理載送, 被遷移到與源區溫度不同的澱積區, 再發生逆向反應, 使源物質重新澱積出來。
區別
化學還移反應類似於升華或蒸餾,但與之不同的是在CTR中,對於給定的溫度,源物質並不一定具有可觀的蒸汽壓,源物質發生的是“化學上的遷移”, 即通過多相化學反應而發生的遷移。
鑒於上述,化學遷移反應可表述為下述兩大步驟:
源物質的氣化→遷移→源物質的澱積或再生
可見,源物質的氣化和再生,是一個可逆反應的兩端。通過對可逆反應的熱力學分祝控制一定的溫度、壓力條件,即可促使上述過程得以完成。因此,完成化學遷移反應的總過程,就需要實現氣態化合物從源區到澱積區的遷移。
實現方法
實現氣態化合物的遷移通常有三種方法:
(1)開管系統中依靠輸運劑的流動來完成。
(2)閉管系統中依靠氣體的擴散運動
(3)侶因溫差引起的熱對流來完成。
理想模型
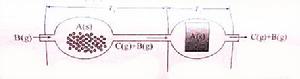 化學轉移反應的理想裝置
化學轉移反應的理想裝置如右圖所示為固體物質A發生轉移反應的理想裝置,在原料放置區(即圖中T1段),A和B儘可能生成C並向沉澱區 移動,在沉澱區(T2)段,C儘可能分解沉積出A。
實際套用及研究
化學遷移反應的早期研究和套用,是從貴金屬的提取和純化開始的。後來,隨著半導體工業的發展,以化學遷移反應為基礎發展起來的化學氣相沉積(CVD)方法,獲得了廣泛的實際套用。由於氣相沉積過程可以在氣相中進行也可以在一種作為基底的材料在表面上進行,因而在製備表面複合材料和表面塗層以及製造超細、超純金屬粉末方瓦化學遷移反應將發揮更為獨特的作用,從而進一步拓廣CTR的工程套用領域。
有色金屬再生
近年研究處理廢料再生鎢的方法有電解法,鋅熔法、高溫氧化法,化學溶解法及氯化法等。其中氯化法所用設備簡單,對原料適應性廣, 因此,被認為是較有前途的方法之一。
鎢條垂熔時夾頭兩端的切塊(純度>99%以上)在950℃時在氯化管內用氯氣進行氯化,氯化物經氬氣輸送到還原管內用氫氣還原。工業瓶裝氯氣通過濃硫酸脫水後與氬氣混合。氫氣把石棉350℃ 脫氧, 再用矽膠、分子篩乾燥。反應產出的超細鎢粉收集在收粉管中,含氫廢氣經淨化吸收其中的氯化氫後排放燃燒。
汽車冶金
化學遷移反應的另一個重要的工程套用,就是汽化冶金。作為一種新的冶金技術,在材料加工方瓦例如,可利用氯化物化學氣相還原一澱積方法,生產超細金屬粉末和超純金屬等。
所謂汽化冶金就是利用金屬或金屬化合物的蒸汽壓大小的不同,即揮發能力的差異,通過化學遷移反應,來進行各種金屬的熔煉或精煉的一種提取冶金方法。
汽化冶金不同於其它冶金方法,就在於汽化冶金中發生了金屬的化學遷移,即金屬首先生成一種揮發性化合物而從原礦石中分離出來,然後通過對該揮發性金屬化合物的處理,如澱積反應、熱分解、電解、直接還原、歧化反應等來提取和純化金屬。
表面複合材料
化學遷移反應在材料科學領域中的一個突出的工程套用,就是表面複合材料的加工。
在製備表面複合材料以及各種材料的塗層工藝中, 基於化學遷移反應發展起來的各種氣相蒸汽沉積工藝,起著重要的作用。
氣相沉積過程包括表面與活潑氣體之間的相互作用,故可用於產生高性能的表面塗層或者利用金屬有機化學氣相沉積以及其它工藝,能獲得特殊功能的原子尺度規則的薄膜。正由於氣相沉積工藝在製備各種新材料中具有特殊功能,因而對採用這些新材料的新技術、高技術領域, 如微電子學、半導體光電技術、太陽能利用中光電轉換功能的無機材料、單晶薄膜、宇航技術、CdS/InP電池、生物材料與生物醫學工程以及光纖通訊中光導纖維的製造等等領域, 它正獲得廣泛套用,促進了這些新技術的發展。