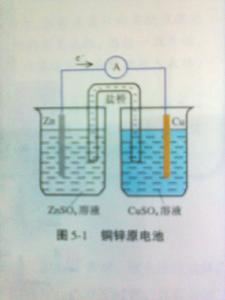
此時,在該原電池中,Zn失電子,做負極;Cu得電子,做正極。
電極反應為:
負極 Zn—2e-=Zn2+
正極 Cu2++2e-=Cu
———————————————
電池反應 Zn+Cu2+=Zn2++Cu
在外電路中,電子由負極流出正極流入,電流方向則相反。

此時,在該原電池中,Zn —2e-=Zn +Cu2+=Zn

化學電源俗稱為電池,是一種利用物質的化學反應所釋放出來的能量直接轉化為電能的裝置。顧名思義,電池是裝電的電池,尤如水池,電池的電壓及容量類似於水池的水位...
電池的工作原理 電池的常用標準 電池的主要特點 電池的發展簡史 電池的分類化學電源俗稱為電池,是一種利用物質的化學反應所釋放出來的能量直接轉化為電能的裝置。電池是指盛有電解質溶液和金屬電極以產生電流的杯、槽或其他容器或複合容器...
發展歷程 工作原理 常用標準 特點 電池技術在電池反應中,1千克反應物質所產生的電能稱為電池的理論比能量。 電池的容量與電極物質的數量有關,即與電極的體積有關。 電池的理論充電時間電池的理論充電時...
事實上,純電動車所採用的電池,是所有電池種類中電容量最大,同時也是技術難度最高的一種蓄電池。 於是,能夠經過多次充電放電循環,反覆使用的蓄電池成為新的方...
電池200年發展簡史 “環保” 青蛙腿帶來靈感 從“便攜”到重複使用 新勢力風起雲湧電動勢也可用組成電池的各界面電勢差的加和表示,(11-47) 在消除或忽略了液接電勢和接觸電勢後,電池電動勢僅取決於兩個半電池的電極~溶液界面電勢差: ...
基本簡介 相關詞條 相關連結劇情簡介Mike Ross是一個年輕聰明的大學輟學生,為了生活,他幫助別人考試賺取生活費,為了為生病的奶奶交上足額的住院費用,他...
劇情簡介 分集劇情 演職員表 角色介紹 幕後花絮a-Si,接著再蒸鍍金屬電極鋁(Al).光從玻璃面入射,電池電流從透明導電膜和...視窗層、梯度界面層、μC-SiC p層等,明顯改善了電池的短波光譜回響...太陽光,達到拓寬光譜回響、提高轉換效率之目的。在提高疊層電池效率方面還採用了...
概念基本 物理優勢 原理 參數 模組結構,丹尼爾發明了世界上第一個實用電池,並用於早期鐵路信號燈。套用 1.直接...原電池 化還原反應的可逆性很差,放完電後,不能重複使用,故又稱一次電池...、汞、二氧化硫、氟化碳等)分為鋅錳電池、鋅空氣電池、鋅銀電池、鋅汞電池...
基本簡介 常見類型 工作原理 發明歷史 套用