三相點
三相點是指在熱力學裡,可使一種物質三相(氣相,液相,固相)共存的一個溫度和壓力的數值。舉例來說,水的三相點在0.01℃(273.16K)及611.73Pa 出現;而汞的三相點在−38.8344°C及0.2MPa出現。
物質的三相點可以用三相池來測量,水的三相點更用於制定熱力學的國際單位制基本單位之一的熱力學溫標定義。由於水的三相點有確實的數值,所以若用溫度的數值作為熱力學溫標的定義是較測量出來的數值更為準確
(1)定義
一般指的是,各種化學性質穩定的純物質處於固、液、氣三個相(態),在平衡共存時的三條平衡線的交點。三相共存時具有固定的溫度和壓強。
(2)說明
①所謂相,是指在某一系統中,具有相同成分及相同物理、化學性質的均勻物質部分。各相之間有顯明的界面。如有冰、水組成的混合物,冰是一個相,水又是一個相,共有兩個相。而酒精可以溶解於水,水和酒精的混和物卻只有一個相。又如兩塊晶形相同的硫黃是一個相,而兩塊晶形不同的硫黃(如斜方晶形和單斜晶形)則是兩個相。不同的相之間的相互轉變叫做相變。相變是十分普遍的物理過程。物態變化就是一種相變過程。例如,固體、液體之間的物態變化過程就是物質 從固相轉變為液相(熔解)或液相轉變為固相(凝固)的過程。
②在熔點時,固、液兩相平衡共存。如果低於熔點,物質就以固相存在;如果高於
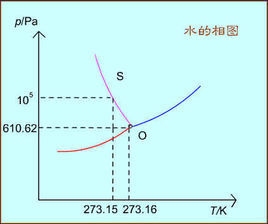
熔點,物質就以液相存在。因此在p-T圖中,畫出熔點和壓強的關係曲線OL(熔解曲線)就可以表示固、液兩相存在的區域。在OL的左方是固相存在的區域,OL和汽化曲線OK(氣相和液相平衡共存的相平衡曲線)之間,是液相存在的區域(如圖),OL與0K的交點O叫做三相點。這一點既在熔解曲線上,又在汽化曲線上,因此三相可以平衡共存。
各種物質,處在三相點時都具有固定的溫度和壓強。如水的三相點溫度為0.01℃,壓強為4.58mmHg。
幾種物質三相點的數據
__溫度(K)/壓強(帕)
氫13.84/7038.2
氘18.63/17062.4
氖24.57/43189.2
氮63.18/12530.2
二氧化碳216.55/517204
水273.16/610.5