材料歷史
·C3N4被認為是最古老的人工合成化合物之一,其歷史可以追溯到1834,由Berzelius和Liebig首次報導。 ·1922年Franklin通過熱解Hg(CN)2和Hg(SCN)2等前驅體得到一種無定型氮化碳,他還提出了其可能結構。 ·1937年由Pauling和Sturdivant首次提出C3N4是以共面三均三嗪為基本結構單元的多聚類化合物,並通過X射線晶體學研究證明了這一觀點。
·20世紀90年代,C3N4在長時間的冷落後再次引起研發人員的關注,但這一時期主要是在超硬材料β-C3N4方向有突破性進展。
·1996年Teter和Hemley採用第一性原理對C3N4重新計算,提出C3N4具有5種結構,即α相、β相、c相、p相和g相,其中前四種為超硬材料,而g-C3N4是軟質相,在常溫常壓下穩定。
·2006年g-C3N4開始套用於多相催化領域,由福州大學王心晨教授課題組於2009年證實g-C3N4非金屬半導體可以在光照下催化水產生氫氣。
·近年來,由於特殊的結構和優異的性能, g-C3N4成為研究熱點,也有企業成功實現量產並推動g-C3N4在光催化領域的商業化套用。
物化性質
 g-C3N4實物 g-C3N4實物 | 化學式:g-C3N4 | 禁頻寬度:2.7 e |
| 分子量:92 | 層間距:0.326nm | |
| 外觀:淡黃色粉末 | 比表面積:46.87m2/g | |
| 晶體結構:類石墨相 | 孔容:0.3099cc/g | |
| 空間構型:平面二維片層結構 | 孔尺寸:26.45nm | |
| 酸鹼性:中性 | 松裝密度:約0.114g/cm3 | |
| 中文名:類石墨相氮化碳 | 水溶性:微溶於水 | 毒性:無毒,粉末吸入會引起呼吸道疾病 |
| 英文名:Graphitic carbon nitride | 套用方向:可見光催化材料、催化劑載體、儲能、感測等方向 | |
結構
·g-C3N4是一種近似石墨烯的平面二維片層結構,有兩種基本單元,分別以三嗪環(C3N3,左圖)和3-s-三嗪環(C6N7,右圖)為基本結構單元無限延伸形成網狀結構,二維納米片層間通過范德華力結合。Kroke等通過密度泛函理論(DFT)計算表明3-s-三嗪環結構較三嗪環結構連線而成的g-C3N4更穩定。
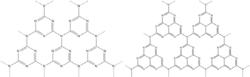 g-C3N4分子結構
g-C3N4分子結構g-C3N4光催化原理
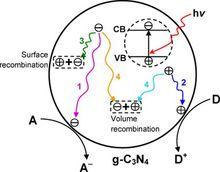 光催化原理
光催化原理Schematicillustration of photoexcitedelectron−hole pairs in g-C3N4 with possible decay pathways. A and D denoteelectron acceptor and electron donor, respectively.
g-C3N4受光激發產生電子-空穴對的示意圖
hν表示光子能量,A表示電子受體,D表示電子供體
主要優點
·g-C3N4作為新型非金屬光催化材料與傳統的TiO2光催化劑相比, g-C3N4 吸收光譜範圍更寬,不需要紫外光僅在普通可見光下就能起到光催化作用;同時,比起TiO2,g-C3N4更能有效活化分子氧,產生超氧自由基用於有機官能團的光催化轉化和有機污染物的光催化降解,更適用於室內空氣污染治理和有機物降解。
·1.可見光回響
·g-C3N4作為新型非金屬光催化材料與傳統的TiO2光催化劑相比, g-C3N4 吸收光譜範圍更寬,不需要紫外光僅在普通可見光下就能起到光催化作用;同時,比起TiO2,g-C3N4更能有效活化分子氧,產生超氧自由基用於有機官能團的光催化轉化和有機污染物的光催化降解,更適用於室內空氣污染治理和有機物降解。
·2.穩定無毒無污染
·g-C3N4具有良好的熱穩定性和化學穩定性。 g-C3N4能在高溫下性能穩定。在超過600℃時熱穩定性才會開始下降。
·g-C3N4能在強酸強鹼下保持性能穩定。
·g-C3N4經測試對SPF級KM小鼠急性經口毒性LD50>5000 mg/kg·BW,屬於實際無毒。對大腸桿菌、金黃色葡萄球菌有良好的抑菌作用。
·g-C3N4對環境友好,無二次污染。
·3.易製備
·g-C3N4能通過多種富氮前驅體(如雙氰胺、尿素、三聚氰胺、硫脲等)、多種製備手段製得,具有工藝流程短、使用設備少、對設備要求低、製備時間短等特點。但由於產率低、成品穩定性低等問題存在,主要還是實驗室級少量製備,也有企業成功實現規模量產。
套用方向
·1.光催化劑
·1.1光催化分解水制氫制氧 ·g-C3N4 的導帶和價帶跨立在H+/H2 和H2O/O2還原電勢的兩側,所以g-C3N4 可用來催化水的分解 ·Oxidation:
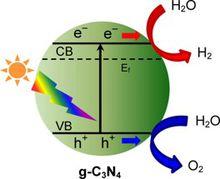 光催化分解水制氫制氧
光催化分解水制氫制氧H2O + 2h+ → 2H+ + ½ O2 (1)
·Reduction:
2H+ + 2e− → H2 (2)
·Overall reaction:
H2O → H2 + ½ O2 (3)
·1.2光催化降解污染物
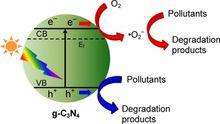 光催化降解污染物
光催化降解污染物·光催化反應的本質是氧化還原反應,當半導體光催化材料受到光照射時會吸收光能,一旦能量超過其閾值時材料將受到激發,從而產生光生電子(e-)和空穴(h+),電子和空穴遷移到催化材料表面,其中電子被溶解氧所捕獲形成超氧自由基(·O2-),而空穴則將吸附在催化劑表面,將水和氫氧根離子氧化成羥基自由基(·OH),這兩類物質均具有很強的氧化性,從而將材料表面的污染物/細菌氧化成CO2和H2O,最終起到防污、除菌和淨化功能。
·光催化降解污染物方面與傳統納米二氧化鈦對比:
| 對比項 | 納米TiO2 | g-C3N4 |
| 光回響類型 | 紫外光(<380 nm) | 可見光(<475 nm) |
| 占太陽光能量 | 4% | 43% |
| 所用光線對人體影響 | 有害,長期照射會致癌 | 無害 |
| 是否含重金屬 | 是 | 非金屬材料 |
| 材料對人體的影響 | 低毒性,潛在致癌物質 | 無毒 |
| 材料對環境的影響 | 可能造成重金屬污染 | 環境友好 |
| 產品套用是否需要額外提供光源 | 需要提供紫外光源 | 使用自然光 |
| 產品套用是否加裝加保護裝置 | 需要紫外光保護裝置 | 不需要 |
·2.感測器
·g-C3N4半導體由於表面含有大量的氨基,近年來開始作為感測器用於金屬離子的檢測、酸性氣體的檢測和生物成像等方面。
·3.催化劑載體和儲能材料
·g-C3N4納米材料由於具有優異的化學惰性、較高的比表面積和種類豐富的納米多級結構,常被用作傳統催化領域綠色載體和儲能材料。
·4.有機反應催化劑
·g-C3N4由於獨特的化學組成和π共軛電子結構, 具有較強的親核能力、易形成氫鍵以及Bronsted 鹼功能和Lewis鹼功能, 使其可以成為一種多功能的催化劑, 套用於傳統的有機催化反應中。
製備方法
·g-C3N4的製備方法主要分為物理法和化學法
·1.固相反應法
·固相反應法製備g-C3N4一般選擇含有三嗪結構的化合物作為反應前驅體,如三聚氰氯、三聚氰胺等,以LiN3、NaN3等作為氮源,在一定溫度下進行固相反應製得g-C3N4 。該方法可靈活地調整C/N摩爾比、可控制材料的納米結構和形貌。
·2.溶劑熱法
·溶劑熱法製備g-C3N4一般選擇以三聚氰胺、三聚氰氯等為原料,NH2NH2、Et3N等為溶劑在一定溫度下結晶合成。該方法具有反應條件溫和、構成易於控制和體系均勻性好等優點。
·3.電化學沉積法
·電化學沉積法近年來套用於g-C3N4薄膜的製備,該方法設備簡單、易於控制,能能降低反應體系溫度。
·4.熱聚合法
·熱聚合法通過熱誘導前驅物發生縮聚反應形成g-C3N4 ,是一種直接而簡便的材料製備方法,近年來逐漸成為製備g-C3N4的一種常用和重要的合成方法, 廣泛套用於製備g-C3N4基催化劑、催化劑載體和儲能材料等。
·熱聚合法選用富氮前驅體種類多、成本低,對設備和控制要求低,操作簡單,易於放大,成為規模化製備g-C3N4的首選途徑。
研究方向
·性能提升
·1.元素摻雜是將額外的元素引入g-C3N4框架的過程,來調節g-C3N4的光學、電子、發光和其他性質,根據摻雜的元素通常分為兩類:非金屬摻雜和金屬摻雜。非金屬摻雜主要有O、C、S、B、I、F等,金屬摻雜主要有Zn、Fe、Ni、Cu、Co和鹼金屬。
·2. g-C3N4的共聚合
·g-C3N4的光催化活性來源於π共軛結構,共聚法是調節π體系、電子性質、光吸收、能帶結構和重要的光催化性能的典型分子摻雜。
·3.構築異質結結構
·g-C3N4中的載流子複合會大大降低光催化效率,為抑制載流子複合,構築g-C3N4的異質結結構引起了廣泛的關注。主要有金屬/g-C3N4異質結、其他半導體/g-C3N4異質結、碳材料/g-C3N4異質結、導電聚合物/g-C3N4異質結等。
·4.微觀形貌調整
·g-C3N4的性能與其比表面積和孔結構有著重要的關係。通常採用溶劑剝離和熱剝離來增大比表面積,採用模板法來引入多孔結構。
·固載技術
·傳統的均相催化過程不利於g-C3N4催化劑回收,也會降低其光催化性能,所以如何將g-C3N4固載至合適的基材表面成為提高g-C3N4材料利用效率的一個熱點方向。
發展前景
·g-C3N4由於其獨特的結構和優異的性能,受到研究和套用方面廣泛關注,在能源、催化、感測領域的潛在價值不斷被開發,且在化學、材料、物理、生物、環境、能源等領域取得重要成果。隨著科研人員和民眾對g-C3N4的認識不斷加深, g-C3N4在未來將會被套用於更多的領域、更多的場景中。

