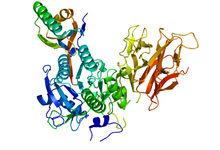
PCSK9的分子結構
 PCSK9抑制劑
PCSK9抑制劑PCSK9主要在內質網合成,首先形成一個75 kDa的前體,其未成熟的前體包含一個N端信號肽序列、一個前結構域、一個催化結構域和一個富含半光氨酸的C端結構域。隨後在內質網中PCSK9在其第152位殘基處經歷一次自動催化性裂解,形成一個14 kDa的前結構域片段和一個包含催化結構域和C端結構域的57 kDa成熟片段。裂解後的前結構域仍然以非共價鍵結合在催化結構域上,與成熟片段形成一個複合體,並作為一個分子伴侶與成熟片段一起離開內質網轉運到高爾基體中,在高爾基體中經過乙醯化等一系列修飾後最終分泌到血液中。前結構域的結合可能發揮著抑制蛋白酶催化活性的作用,是PCSK9正確摺疊並離開內質網所必需的。大多數前蛋白轉化酶在離開內質網後會經歷二次蛋白酶解加工作用,從而釋放前結構域,暴露酶活性。而離開內質網後的 PCSK9沒有經歷這種二次加工過程,因此PCSK9是唯一沒有蛋白質底物的枯草桿菌蛋白酶樣絲氨酸蛋白酶。
肝臟是血液中PCSK9的主要來源。由於檢測時使用的特異性抗體以及標準值的不同,人血漿中PCSK9濃度的平均值變化範圍較大,在500 ng·mL~4 μg·mL之間。小鼠血中PCSK9的半衰期大約為5 min。
PCSK9的功能
 PCSK9抑制劑
PCSK9抑制劑PCSK9是一種肝源性分泌蛋白,它與LDLR的胞外區結合,然而,PCSK9對LDLR降解作用是胞內的。PCSK9並不需要激酶的催化活性來影響LDLR 的轉化,激酶的催化活性不能引導帶受體的複合體到複合體降解的溶酶體中或是抑制複合體的循環。PCSK9作為一種神經細胞凋亡調節轉化酶,不但參與肝臟再生,調節神經細胞凋亡,還能通過降低肝細胞上LDLR的數量,影響 LDL內化,使血液中LDL不能清除,從而導致高膽固醇血症。研究表明,PCSK9水平與膽固醇、ox-LDL、甘油三酯顯著相關。PCSK9作為一種絲氨酸蛋白酶,除了能夠降解 LDLR,升高血LDL水平之外,還有其他多種生物學功能,例如,參與神經系統發育、神經細胞的凋亡和調節鈉通道、胰島細胞功能等。PCSK9 的產生過程是首先在內質網中合成 PCSK9酶原,其在內質網或者高爾基體內發生自我催化反應,裂解釋放出前肽,形成成熟的蛋白酶,並立即分泌入血,通過調節LDLR維持血漿脂質的穩態,其不僅能影響血漿膽固醇的水平,調節神經細胞的凋亡,還與炎症反應有一定的相關性。
已上市的PCSK9抑制劑
 PCSK9抑制劑
PCSK9抑制劑Evolocumab由安進開發(在日本安進和安斯泰來合作研發),於2015年7月17日獲得歐洲藥物管理局(EMA)批准,2015年8月28日獲得美國食品藥物管理局(FDA)批准,2016年1月22日獲得日本醫藥品醫療器械綜合機構(PMDA)批准上市,並由安進在美國和歐洲市場銷售,由安斯泰來在日本市場銷售,商品名為Repatha。Evolocumab是一種全人源IgG2型單克隆抗體,作為前蛋白轉化酶枯草桿菌蛋白酶Kexin-9(PCSK9)抑制劑,能結合PCSK9並抑制循環型PCSK9與低密度脂蛋白受體(LDLR)的結合,從而阻止PCSK9介導的低密度脂蛋白受體降解。該藥批准的適應症為高膽固醇血症和混合血脂異常。Repatha是一種皮下注射液,每支預填充的注射器含140 mg/mL Evolocumab。推薦劑量為每次140 mg,每兩周一次(成人原發性疾病)或每次420 mg,每月一次(成人和12歲及以上兒童純合子型家族性膽固醇血症)。
Alirocumab 由賽諾菲(Sanofi)和再生元(Regeneron)聯合研發,於2015年7月24日獲得美國食品藥物管理局(FDA)批准,2015年9月23日獲得歐洲藥物管理局(EMA)批准,2016年7月4日獲得日本醫藥品醫療器械綜合機構(PMDA)批准上市,並由賽諾菲和再生元公司在美國、歐洲和日本市場共同銷售,商品名為Praluent。Alirocumab是一種全人源IgG1型單克隆抗體,作為前蛋白轉化酶枯草桿菌蛋白酶Kexin-9(PCSK9)抑制劑,能結合PCSK9並抑制循環型PCSK9與低密度脂蛋白受體(LDLR)的結合,從而阻止PCSK9介導的低密度脂蛋白受體降解。該藥用於治療成人雜合子型家族性高膽甾醇血症和臨床動脈粥樣硬化心血管疾病(如需降低低密度膽固醇的心臟病或中風)。Praluent是一種皮下注射用溶液,含75 mg或150 mg Alirocumab。推薦劑量為每次75 mg或150 mg,每兩周一次。
