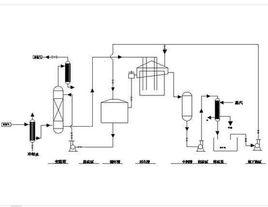
水煤氣
一氧化碳和氫氣都是會燃燒的氣體,工業上把這樣的混合氣叫“水煤氣”。因為水分子裡有一個氧原子和兩個氫原子,水一遇上火熱的煤(C),氧原子立刻被煤(C)奪走了,結果生成一氧化碳和氫氣。水煤氣是一種低熱值煤氣,由蒸汽與灼熱的無煙煤或焦炭作用而得。其主要成分為氫氣和一氧化碳,也含有少量二氧化碳、氮氣和甲烷等組分;各組分的含量取決於所用原料及氣化條件。主要用作合成氨、合成液體燃料等的原料,或作為工業燃料氣的補充來源。
反應機理
水煤氣變換反應是放熱反應,較低的反應溫度有利於化學平衡,但反應溫度過低則會影響反應速率,從純化學的角度來看,水煤氣變換反應的正向反應是水合反應,逆向反應是一個加氫及脫水反應。
水煤氣變換反應屬於中等程度放熱。按照操作溫度,可分為低溫水氣變換反應(180~250℃)和中溫水氣變換反應(220~350℃)。現有的低變反應機理類型主要有以下四種:
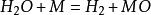 水煤氣變換反應
水煤氣變換反應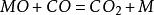 水煤氣變換反應
水煤氣變換反應(1)氧化還原機理:,;M為銅系金屬,MO為與M相對應的金屬氧化物。
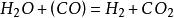 水煤氣變換反應
水煤氣變換反應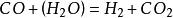 水煤氣變換反應
水煤氣變換反應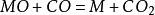 水煤氣變換反應
水煤氣變換反應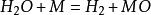 水煤氣變換反應
水煤氣變換反應(2)三途反應機理:,,,;(CO)、(HO)表示被吸附的CO、HO,M為銅系金屬,MO為與M相對應的金屬氧化物。
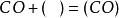 水煤氣變換反應
水煤氣變換反應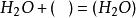 水煤氣變換反應
水煤氣變換反應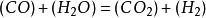 水煤氣變換反應
水煤氣變換反應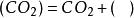 水煤氣變換反應
水煤氣變換反應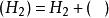 水煤氣變換反應
水煤氣變換反應(3)Langmuir-Hinshelwood機理:,,,,;( )表示催化劑表面未被吸附活潑部位,(CO)、(HO)、(CO)、(H)表示被吸附的CO、HO、CO、H。
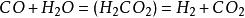 水煤氣變換反應
水煤氣變換反應(4)甲酸型中間絡合物機理:;(HCO)表示吸附在催化劑表面且與甲酸具有相同化學計量式的中間和活化絡合物。
變換反應的功能
水煤氣變化反應在工業中有以下功能:
(1)反應:採用中串低變換工藝流程,變換觸煤採用耐硫寬溫Co-M0系變換催化劑,反應式如下:
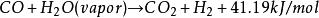 水煤氣變換反應
水煤氣變換反應;
(2)回收熱量,產生蒸汽;
(3)處理冷凝液(氣提)。
影響因素
水煤氣變換反應在反應過程中主要受以下因素影響:
溫度
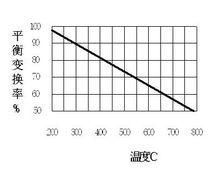 水煤氣變換反應平衡變換率與溫度的關係.jpg
水煤氣變換反應平衡變換率與溫度的關係.jpg由於變換反應為放熱反應,從反應平衡上看應該是溫度越低越有利於反應的進行,但溫度低了反應速度也降低了,達到同樣的反應深度就需要較長的反應時間,這就增加了催化劑的裝填量,提高了成本。
同時,由於受溫度的控制,出口一氧化碳的含量受到限制。即為什麼合成氨變換需要設定兩個變換爐,在不同的溫度下操作。
中變爐的熱點溫度≤450-460℃,低變爐的熱點溫度在250-260℃。
壓力
壓力對變換反應平衡沒有影響,增加壓力可提高反應速度。因此,變換的壓力由氣化和後系統決定。
(1)壓力對低溫甲醇洗的影響:由於低溫甲醇洗物理吸收,壓力高有利於對HS、CO的吸收,能耗低,綜合吸收效果好。
(2)對甲醇系統的影響:甲醇合成壓力在5.0MPa左右,淨化氣直接可以進入甲醇合成塔,循環氣可以通過循環機增壓後進入合成塔,減少了投資,減低了消耗。
在正常操作時,要保證壓力穩定,防止催化劑顆粒受壓不均勻出現破碎,增大阻力,影響變換效果。加壓變換與常壓相比,有以下優點:
(1)可以加快反應速度和提高催化劑的生產能力,從而可採用較大的空間速度,提高生產強度;
(2)設備體積小,布置緊湊,投資較少;
(3)濕變換氣中水蒸汽的冷凝溫度高,有利於熱能的回收利用。
車間定期對同氣量下的變換爐出入口壓差進行測量來判斷催化劑床層的阻力即催化劑破碎粉化程度。
水氣比
水氣比是指是指水蒸汽與水煤氣中乾基工藝氣的體積比。其計算方法為水蒸汽/工藝氣,或在飽和狀態下用P/(P-P);水汽比的增加能夠提高變換反應的平衡變換率,加快反應速度。從反應方程式來看,提高水氣比即增加水的含量有利於CO的轉化。同時,一定的水氣比可以帶走大量的反應熱,起到降低床層溫度的作用。
在飽和狀態下,提高氣體的溫度,或者在不飽和狀態下,保溫好,提高飽和度,都可以提高水氣比。通過降低氣體的溫度,使水蒸汽冷卻,則可以降低水氣比。
在甲醇變換時,由於氣化氣體成分中水汽比高,超過變換的需要,在流程設計時,變換爐前設計了水煤氣廢鍋來降低水汽比,通過控制廢鍋產生蒸汽的壓力來調節水氣比,使之滿足變換工藝要求。
空速
空速是指單位時間,通過單位催化劑體積的氣體數稱為空間速度,簡稱空速。空速過大,停留時間短,反應不完全,變換出口超標,同時大空速很易將床層溫度拉垮;空速過低,停留時間長,床層熱量不能及時移出,易造成床層超溫,燒壞催化劑。
在保證一定變換率的前提下,催化劑活性好,反應速度快,可以採用較大的空速,充分發揮設備的生產能力。如果催化劑活性差,反應速度慢,可以適當降低空速。
水煤氣變換反應中的催化劑
水煤氣變換反應常常藉助於催化劑而進行。人們早期工作的著眼點,是鐵系氧化物催化劑,然而由於這一催化體系活性較底,必須在高溫下進行操作,造成變換率降低,這樣就限制之中催化劑的套用,隨後人們研製出以銅系氧化物為主體的變換催化劑,但這一催化劑仍存在缺陷。進年來整體式(構件型)蜂窩狀WGSR催化劑與負載型催化劑引起了人們極大興趣,尤其是負載金超微粒子催化劑。
催化劑活性評價主要由以下兩種方式:
(1)用CO轉化率表示:CO轉化率(%)=(1-Vco'/Vco)/(1+Vco')×100%;式中Vco為原料氣中CO的體積百分數,Vco'為變換氣中CO的體積百分數。
(2)催化劑的選擇性:催化劑的選擇性=變化氣中氫氣的量/原料中一氧化碳的量×100%。
銅催化劑
低變反應所選用的催化劑,是活性高而缺陷少的CuO-ZnO系催化劑其操作溫度控制在150℃-250℃之間。在這類催化劑中一般具有第三組分,早期人們常常選用氧化鉻,但由於製備這種催化劑時,會生成相當量的Cr 而在催化劑使用之前的還原過程中,可使Cr 變成Cr ,從而放出大量的熱,使催化劑燒結,造成環境污染,故近期人們所採用的催化劑多以CuO、ZnO、AlO為主要組份。
整體式蜂窩狀WGSR催化劑
許多相互隔離且均勻分布的直孔或曲孔的蜂窩狀陶瓷或金屬載體,將催化活性組分均勻地分布在孔道的內壁,改變了傳統催化劑的形狀,從根本上克服了傳統顆粒狀催化劑及其採用的固定床反應器存在的局限,流動阻力小,催化效率高,可以實現大空速、小體積的化工強化過程,單位反應器體積的表面積大,反應速率快。
負載金超微粒子催化劑
有關金催化劑的研究開發引起了人們的極大興趣。負載型金催化劑的突出特點是具有較高的低溫催化活性、較好的抗中毒性和穩定性,同時作為一種貴金屬催化劑,金催化劑的價格要遠遠低於鉑和鈀。金原子位於周期表第IB族,分子量為79,與Cu和Ag為同族元素。金的表面與表面分子之間的相互作用力很弱。在單晶金的表面,連極具反應活性的分子如氫、氧等,都不易吸附,然而對納米金屬負載催化劑來說,其表面的化學吸附及反應活性卻隨結構明顯地發生變化,超微顆粒金常被負載於載體上,,大多含有幾千個原子,形成粒度很小的金顆粒,這種小的顆粒很容易吸附簡單分子。但是更為重要的是當金屬粒子小到一定程度以後,金屬本身的電子性質將發生變化,從而導致其化學和物理性質出現突變。正是由於這些性質上的突變使得高分散金催化劑的研究成為催化領域中一個新的熱點。
催化劑的注意事項
裝填的注意事項
(1)裝填前,先對催化劑過篩,對爐內襯檢查、清理;
(2)嚴格檢查爐篦是否牢固可靠,篦上鋪好鋼絲網,圍邊壓好;
(3)自下而上分層裝填,不允許集中傾倒再扒平,以防偏流;
(4)裝填時,嚴禁人員在觸媒上踐踏。必須入爐時,應先鋪木板,人站在木板上操作;
(5)裝完後,表面扒平,覆蓋一層鋼絲網,儘量多加耐火球;
(6)裝完後,應密封進出口,以防吸潮或其它有害氣體進入;
(7)新舊催化劑混裝時,一般應將舊催化劑裝在上面。
變換觸媒正常操作的注意事項
(1)催化劑床層的進口溫度控制在指標之內,床層入口溫度要高於露溫度至少30℃;
(2)儘可能在低溫下操作,床層提溫須遵循“慢慢少提”的原則;
(3)嚴禁帶水入爐;
(4)為防止反硫化,氣體中的硫含量不低於200mg/m ,同時控制操作溫度與汽氣比在正常範圍內;
(5)長期停車降溫過程中,注意保持變換爐正壓。
反硫化注意事項
耐硫變換催化劑的活性組份只有處於硫化狀態才具有催化活性,因此對工藝氣中硫含量的上限不加限制,但對下限有明確的要求,即要求使用的原料煤的含硫量不能小於某一數值,否則將出現反硫化現象而使催化劑失活。催化劑中的活性組分MoS較易於水解,因此催化劑允許工藝氣中的最低硫含量與溫度和水蒸汽分壓有關。
事故分析
水煤氣帶水
 水煤氣變換爐
水煤氣變換爐(1)少量帶水:由於氣化來氣體為飽和水煤氣,受到溫度和壓力的影響會產生水滴。為了防止水滴產生,變換氣入變換爐的溫度一般要高於露點30℃以上。因此,通過變換爐入口溫度和排放低點導淋可以解決少量帶水問題。
(2)大量帶水:氣化來氣體帶水量大,或管道溫度較低,或入工段煤氣水分離器液位較高排放不及時,會產生大量水,應即時停車處理。
系統開車時最容易帶水入爐,要保證氣化壓力穩定。
水煤氣中氧含量超標
水煤氣氧含量過高會引起變換爐床溫度暴漲,燒壞催化劑,嚴重時會引發惡性爆炸事故。一旦發生水煤汽過氧,應立即按系統緊急停車處理。然後根據情況對變換系統分段降溫(用氮氣)。
變換爐超溫
變換爐超溫一般發生在系統開車時和操作不正常時(系統加減量幅度過大,入口溫度調節不及時),特別是系統開車時,最容易發生超溫現象。這種情況出現的原因主要是操作的水氣比過低,使反應進入甲烷化反應區域。同時,應從催化劑方面進行改進,控制在低水/氣條件下甲烷化副反應起活的溫度範圍。
變換系統的銨鹽結晶
水煤氣中含有少量氮氣,在經過變換系統時在催化劑的作用下和氣體中的氫氣反應而生成少量的氨。這些氨在高濃度二氧化碳存在的條件下,則反應生成碳銨化合物,在溫度較低時,就有結晶析出。發生的部位在低於40℃的區域。如:變換工段出口到低溫甲醇洗之間。