核磁共振
發現病變
核磁共振成像是一種利用核磁共振原理的最新醫學影像新技術,對腦、甲狀腺、肝、膽、脾、腎、胰、腎上腺、子宮、卵巢、前列腺等實質器官以及心臟和大血管有絕佳的診斷功能。與其他輔助檢查手段相比,核磁共振具有成像參數多、掃描速度快、組織解析度高和圖像更清晰等優點,可幫助醫生“看見”不易察覺的早期病變,目前已經成為腫瘤、心臟病及腦血管疾病早期篩查的利器。
據了解,由於金屬會對外加磁場產生干擾,患者進行核磁共振檢查前,必須把身體上的金屬物全部拿掉。不能佩戴如手錶、金屬項鍊、假牙、金屬紐扣、金屬避孕環等磁性物品進行核磁共振檢查。此外,戴心臟起搏器,體內有順磁性金屬植入物,如金屬夾、支架、鋼板和螺釘等,都不能進行磁共振成像檢查。進行上腹部(如肝、胰、腎、腎上腺等)磁共振檢查時必須空腹,但檢查前可飲足量水,有利於胃與肝、脾的界限更清晰。
發現腫瘤
核磁共振對顱腦、脊髓等疾病是目前最有效的影像診斷方法,不僅可以早期發現腫瘤、腦梗塞、腦出血、腦膿腫、腦囊蟲症及先天性腦血管畸形,還能確定腦積水的種類及原因等。而針對危害中國女性生命健康的第一大婦科疾患—乳腺癌,通過核磁共振精準篩查,可以幫助發現乳腺癌早期病灶;而針對“高血壓、高血脂、高血糖”等三高人群,可以通過對頭部及心臟等部位的核磁檢查,在身體健康尚未發出紅燈警訊前,早期發現心臟病、腦梗等高風險疾病隱患。此外,核磁共振還可進行腹部及盆腔的檢查,如肝臟、膽囊、胰腺、子宮等均可進行檢查,腹部大血管及四肢血管成像可以明確診斷真性、假性動脈瘤,夾層動脈瘤及四肢血管的各種病變。核磁共振對各類關節組織病變診斷非常精細,對骨髓、骨的無菌性壞死十分敏感。
據了解,北京大學深圳醫院醫學影像科是深圳市醫學重點專科,廣東省臨床醫學影像學重點專科。該院醫學影像科目前擁有世界上先進的3台磁共振(MR)掃瞄器,分別是1台3.0T磁共振掃瞄器、2台1.5T磁共振掃瞄器。針對超聲定位不準的局限,該科目前採用前列腺虛擬活檢術,對前列腺癌早期診斷和鑑別。
對人無害
由於核磁共振是磁場成像,沒有放射性,所以對人體無害,是非常安全的。據了解,目前世界上既沒有任何關於使用核磁共振檢查引起危害的報導,也沒有發現患者因進行核磁共振檢查引起基因突變或染色體畸變發生率增高的現象。雖然核磁共振在篩查早期病變有著獨到之處,但任何檢查都是有限度的,比如有些病人不適合核磁共振,就不要過度檢查。他呼籲,任何患者都應遵醫囑進行檢查,不要以為影像檢查越貴越好,只有適合自己的檢查才是最好的。
連續波核磁共振波譜儀 CW-NMR
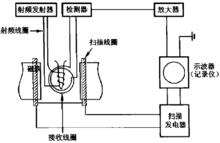 核磁共振儀示意圖
核磁共振儀示意圖如今使用的核磁共振儀有連續波(continal wave,CW)及脈衝傅立葉(PFT)變換兩種形式。連續波核磁共 振儀主要由磁鐵、射頻發射器、檢測器、放大器及記錄儀等組成(見下圖)。磁鐵用來產生磁 場,主要有三種:永久磁鐵,電磁鐵[磁感應強度可高達24000 Gs(2.4 T)],超導磁鐵[磁感應強度可高達190000 Gs(19 T)]。
核磁共振波譜儀的解析度多用頻率表示(也稱“兆數”)其定義是在儀器磁場下激發氫原子所需的電磁波頻率。如一台磁場強度為9.4T的超導核磁中,氫原子的激發頻率為400MHz,則該儀器為“400兆”的儀器。頻率高的儀器,解析度好,靈敏度高,圖譜簡單易於分析。磁鐵上 備有掃描線圈,用它來保證磁鐵產生的磁場均勻,並能在一個較窄的範圍內連續精確變化。射頻 發射器用來產生固定頻率的電磁輻射波檢測器和放大器用來檢測和放大共振信號。記錄儀將 共振信號繪製成共振圖譜。
CW-NMR價格低廉,溫度,易操作,但是靈敏度差。因此需要樣品量大,且只能測定如1H/19F/31P之類天然豐度很高的核,對諸如13C之類低豐度的核則無法測定。
PFT-NMR
20世紀70年代中期出現了脈衝傅立葉核磁共振儀,它的出現使13C核磁共振的研究得以迅速開展。
脈衝變換傅立葉核磁共振波譜儀(pulse Fourier transform-NMR)與連續波儀器不同,它增設了脈衝程式控制器和數據採集處理系統,利用一個強而短(1~50μs)的脈衝將所有待測核同時激發,在脈衝終止時及時打開接收系統,採集自由感應衰減信號(FID),待被激發的核通過弛豫過程返回平衡態時再進行下一個脈衝的激發。得到的FID信號是時域函式,是若干頻率的信號的疊加,在計算機中經過傅立葉變換轉變為頻域函式才能被人們識別。PFT-NMR在測試時常進行多次採樣,而後將所得的總FID信號進行傅立葉變換,以提高靈敏度和信噪比(進行n次累加,信噪比提高n^0.5倍)。
PFT-NMR靈敏度很高,可以用於低豐度核,測試時間短(掃一次一到幾秒),還可以測定核的弛豫時間,使得利用核磁共振測定反應動態成為現實 。
基本原理
原子核的自旋
核磁共振主要是由原子核的自旋運動引起的。不同的原子核,自旋運動的情況不同,它們可 以用核的自旋量子數I來表示。自旋量子數與原子的質量數和原子序數之間存在一定的關係,大致分為三種情況,如下表。
| 分類 | 質量數 | 原子序數 | 自旋量子數I | NMR信號 |
| I | 偶數 | 偶數 | 0 | 無 |
| II | 偶數 | 奇數 | 1,2,3,…(I為整數) | 有 |
| III | 奇數 | 奇數或偶數 | 0.5,1.5,2.5,…(I為半整數) | 有 |
I值為零的原子核可以看做是一種非自旋的球體, I為1/2的原子核可以看做是一種電荷分 布均勻的自旋球體,1H,13C,15N,19F,31P的 I均為1/2,它們的原子核皆為電荷分布均勻的自旋 球體。 I大於1/2的原子核可以看做是一種電荷分布不均勻的自旋橢球體。
核磁共振現象
原子核是帶正電荷的粒子,不能自旋的核沒有磁矩,能自旋的核有循環的電流,會產生磁場,形成磁矩( μ)。
μ= γP
式中, P是角動量矩,γ是磁旋比,它是自旋核的磁矩和角動量矩之間的比值,因此是各種核的特徵常數。
當自旋核(spin nuclear)處於磁感應強度為 B0的外磁場中時,除自旋外,還會繞 B0運動,這種運動情況與陀螺的運動情況十分相像,稱為拉莫爾進動(larmor process)。自旋核進動的角速度 ω0與外磁場感應強度 B0成正比,比例常數即為磁旋比(magnetogyric ratio) γ。式中 ν0是進動頻率。
ω0=2 πν0= γB0
原子核在無外磁場中的運動情況如下圖,微觀磁矩在外磁場中的取向是量子化的(方向量子化),自旋量子數為 I的原子核在外磁場作用下只可能有2 I+ l個取向,每一個取向都可以 用一個自旋磁碟子數 m來表示, m與 I之間的關係是
m= I, I-1, I-2…- I
 1H自旋核在外磁場中的兩種取向示意圖
1H自旋核在外磁場中的兩種取向示意圖原子核的每一種取向都代表了核在該磁場中的一種能量狀態, I值為1/2的核在外磁場作用下只有兩種取向,各相當於 m=1/2 和 m=-1/2,這兩種狀態之間的能量差 ΔE值為
Δ E = γhB0/ 2 π
一個核要從低能態躍遷到高能態,必須吸收Δ E的能量。讓處於外磁場中的自旋核接受一定頻率的電磁波輻射,當輻射的能量恰好等於自旋核兩種不同取向的能量差時,處於低能態的自旋核 吸收電磁輻射能躍遷到高能態。這種現象稱為核磁共振。當頻率為 ν射的射頻照射自旋體系時,由於該射頻的能量 E射= h ν射,因此核磁共振要求的條件為
hν射=ΔE(即2πν射=ω射=γ B0) ①
目前研究得最多的是1H的核磁共振和13C的核磁共振。1H的核磁共振稱為質子磁共振 (Proton Magnetic Resonance),簡稱 PMR,也表示為1H-NMR。13C核磁共振(Carbon- 13 Nuclear Magnetic Resonance)簡稱 CMR,也表示為13C-NMR。
核磁共振飽和與馳豫
1H的自旋量子數是 I=1/2,所以自旋磁量子數 m=±1/2,即氫原子核在外磁場中應有兩種取向。1H的兩種取向代表了兩種不同的能級,在磁場中, m=1/2時, E=- μB0,能量較低, m=-1/2時, E= μB0,能量較高,兩者的能量差為Δ E=2 μB0,見下圖。
式 ①,式 ②說明:處於低能級的1H核吸收E射的能量時就能躍遷到高能級。也即只有當電磁波的輻射能等於lH的能級差時,才能發生1H的核磁共振。
E射= hν射=Δ E= hν0 ②因此1H發生核磁共振的條件是必須使電磁波的輻射頻率等於1H的進動頻率,既符合下式。
ν射=ν0=γ B0/2π ③由式 ③可知:要使ν射=ν0,可以採用兩種方法。一種是應強度,逐漸改變電磁波的輻射頻率ν射,進行掃描,當ν射與B0匹配時,發生核磁共振。另一種方法是固定輻射波的輻射頻率,然後從低場到高場,逐漸改變B0,當 B0與ν射匹配時,也會發生核磁共振(見右圖)。這種方法稱為掃場。—般儀器都採用掃場的方法。固定磁感
在外磁場的作用下,有較多1H傾向於與外磁場取順向的排列,即處於低能態的核數目比 處於高能態的核數目
多,但由於兩個能級之間 能差很小,前者比後者只占微弱的優勢1H-NMR的訊號正是依靠這些微弱過剩的低能態核吸收射頻電磁波的輻射能躍遷到高級而產生的。如高能態核無法返回到低能態,那么隨著躍遷的不斷進行,這種微弱的優勢將進一步減弱直到消失,此時處於低能態的1H核數目與處於高能態核數目逐漸趨於相等,與此同步,PMR的 訊號也會逐漸減弱直到最後消失。上述這種現象稱為飽和。
1H核可以通過非輻射的方式從高能態轉變為低能態,這種過程稱為弛豫(relaxation),正是 因為各種機制的弛豫,使得在正常測試情況下不會出現飽和現象。弛豫的方式有兩種,處於高能態的核通過交替磁場將能量轉移給周圍的分子,即體系往環境釋放能量,本身返回低能態,這個 過程稱為自旋晶格弛豫。其速率用1/T1表示,T1稱為自旋晶格弛豫時間。自旋晶格弛豫降低了磁性核的總體能量,又稱為縱向弛豫。兩個處在一定距離內,進動頻率相同、進動取向不同的 核互相作用,交換能量,改變進動方向的過程稱為自旋-自旋弛豫。其速率用1/T2表示,T2稱為自旋-自旋弛豫時間。自旋-自旋弛豫未降低磁性核的總體能量,又稱為橫向弛豫。
核磁共振豐度和靈敏度
天然豐富的12C的I值為零,沒有核磁共振信號。13C的I值為1/2,有核磁共振信號。通常 說的碳譜就是13C核磁共振譜。由於13C與1H的自旋量子數相同,所以13C的核磁共振原理與1H相同。但13C核的γ值僅約為1H核的1/4,而檢出靈敏度正比於γ3,因此即使是豐度100%的13C 核,其檢出靈敏度也僅為1H核的1/64,再加上13C的豐度僅為1.1%,所以,其檢出靈敏度僅約 為1H核的1/6000。這說明不同原子核在同一磁場中被檢出的靈敏度差別很大,13C的天然豐度 只有12C的1.108%。由於被檢靈敏度小,豐度又低,因此檢測13C比檢測1H在技術上有更多的困難。下表是幾個自旋量子數為1/2的原子核的天然豐度和相對靈敏度。
| 元素核 | 天然豐度/% |
| 1H | 99.9844 |
| 13C | 1.108 |
| 15N | 0.365 |
| 19F | 100 |
| 31P | 100 |
化學位移
氫的核磁共振譜提供了三類極其有用的信息:化學位移、偶合常數、積分曲線。套用這些信 息,可以推測質子在碳胳上的位置。
根據前面討論的基本原理,在某一照射頻率下,只能在某一磁感應強度下發生核磁共振。例如:照射頻率為60 MHz,磁感應強度是 14.092 Gs(14.092×10^-4 T),100 MHz—23.486 Gs(23.486×10^-4 T),200 MHz—46.973 Gs(46.973×10^-4 T)。600 MHz—140.920 Gs(140.920×10^-4 T)。但實驗證明:當1H在分子中所處化學環境(化學環境是指1H的核外電子以及與1H 鄰近的其它原子核的核外電子的運動情況)不同時,即使在相同照射頻率下,也將在不同的共振磁場下顯示吸收峰。下圖是乙酸乙酯的核磁共振圖譜,圖譜表明:乙酸乙酯中的8個氫,由 於分別處在a,b,c三種不同的化學環境中,因此在三個不同的共振磁場下顯示吸收峰。同種核由於在分子中的化學環境不同而在不同共振磁感應強度下顯示吸收峰,這稱為化學位移(chemical shift)。
起因
化學位移是怎樣產生的?分子中磁性核不是完全裸露的,質子被價電子包圍著。這些電子 在外界磁場的作用下發生循環的流動,會產生一個感應的磁場,感應磁場應與外界磁場相反(楞次定律),所以,質子實際上感受到的有效磁感應強度應是外磁場感應強度減去感應磁場強度。即
B有效= B0(1-σ)= B0- B0σ= B0- B感應
外電子對核產生的這作用稱為禁止效應(shielding effect),也叫抗磁禁止效應(diamagnetic effect)。稱為禁止常數(shielding constant)。與禁止較少的質子比較,禁止多的質子對外磁場感受較少,將在較高的外磁場 B 0作用下才能發生共振吸收。由於磁力線是閉合的,因此感應磁 場在某些區域與外磁場的方向一致,處於這些區域的質子實際上感受到的有效磁場應是外磁場 B 0加上感應磁場 B 感應。這種作用稱為去禁止效應(deshielding effect)。也稱為順磁去禁止效應(paramagnetic effect)。受去禁止效應影響的質子在較低外磁場B0作用下就能發生共振吸收。綜上所述:質子發生核磁共振實際上應滿足:
ν射=γB有效/2π
因在相同頻率電磁輻射波的照射下,不同化學環境的質子受的禁止效應各不相同,因此它們發生 核磁共振所需的外磁場B0也各不相同,即發生了化學位移。
對1H化學位移產生主要影響的是局部禁止效應和遠程禁止效應。核外成鍵電子的電子云 密度對該核產生的禁止作用稱為局部禁止效應。分子中其它原子和基團的核外電子對所研究的 原子核產生的禁止作用稱為遠程禁止效應。遠程禁止效應是各向異性的。
表示方法
化學位移的差別約為百萬分之十,要精確測定其數值十分困難。現採用相對數值表示法,即選用一個標準物質,以該標準物的共振吸收峰所處位置為零點,其它吸收峰的化學位移值根據這 些吸收峰的位置與零點的距離來確定。最常用的標準物質是四甲基矽(CH3)4Si簡稱TMS。選TMS為標準物是因為:TMS中的四個甲基對稱分布,因此所有氫都處在相 同的化學環境中,它們只有一個銳利的吸收峰。另外,TMS的禁止效應很高,共振吸收在高場出現,而且吸收峰的位置處在一般有機物中的質子不發生吸收的區域內。現規定化學位移用 δ來 表示,四甲基矽吸收峰的 δ值為零,其峰右邊的 δ值為負,左邊的 δ值為正。測定時,可把標準物與樣品放在一起配成溶液,這稱為內標準法。也可將標準物用毛細管封閉後放人樣品溶液中進 行測定,這稱為外標準法。此外,還可以利用溶劑峰來確定待測樣品各個峰的化學位移。
由於感應磁場與外磁場的 B 0成正比,所以禁止作用引起的化學位移也與外加磁場 B0成正 比。在實際測定工作中,為了避免因採用不同磁感應強度的核磁共振儀而引起化學位移的變化, δ一般都套用相對值來表示,其定義為
δ=(ν樣-ν標)/ν儀×10^6 ④
在式 ④中, ν樣和 ν標分別代表樣品和標準化合物的共振頻率, ν儀為操作儀器選用的頻率。多數有機物的質子信號發生在0~10處,零是高場,10是低場。 需注意也有一些質子的信號是在小於0的地方出現的。如安扭烯的環內的質子,受到其外芳環磁各向異性的影響,甚至可以達到-2.99。此外,在不同兆數的儀器中,化學位移的值是相同的。
影響因素
化學位移取決於核外電子云密度,因此影響電子云密度的各種因素都對化學位移有影響,影 響最大的是電負性和各向異性效應。
⑴電負性(誘導效應)
電負性對化學位移的影響可概述為:電負性大的原子(或基團)吸電子能力強,1H核附近的吸電子基團使質子峰向低場移(左移),給電子基閉使質子峰向高場移(右移)。這是因為吸電子基團降低了氫核周圍的電子云密度,禁止效應也就隨之降低,所以質子的化學位 移向低場移動。給電子基團增加了氫核周圍的電子云密度,禁止效應也就隨之增加,所以質子的 化學位移向高場移動。下面是一些實例。
實例一:
| 電負性 | C 2.6 | N 3.0 | O 3.5 |
| δ | C—C H3(0.77~1.88) | N—C H3(2.12~3.10) | O—C H3(3.24~4.02) |
實例二:
| 電負性 | Cl 3.1 | Br 2.9 | I 2.6 |
| δ | C H3—Cl(3.05) C H2—Cl2(5.30) C H—Cl3(7.27) | C H3—Br(2.68) | C H3—I(2.16) |
電負性對化學位移的影響是通過化學鍵起作用的,它產生的禁止效應屬於局部禁止效應。
⑵各向異性效應
當分子中某些基團的電子云排布不呈球形對稱時,它對鄰近的1H核產 生一個各向異性的磁場,從而使某些空間位置上的核受禁止,而另一些空間位置上的核去禁止, 這一現象稱為各向異性效應(anisotropic effect)。
除電負性和各向異性的影響外,氫鍵、溶劑效應、van der Waals效應也對化學位移有影響。氫鍵對羥基質子化學位移的影響與氫鍵的強弱及氫鍵的電子給予體的性質有關,在大多數情況 下,氫鍵產生去禁止效應,使1H的δ值移向低場。有時同一種樣品使用不同的溶劑也會使化學位移值發生變化,這稱為溶劑效應。活潑氫的溶劑效應比較明顯。
當取代基與共振核之間的距離小於van der Waals半徑時,取代基周圍的電子云與共振核周圍的電子云就互相排 斥,結果使共振核周圍的電子云密度降低,使質子受到的禁止效應明顯下降,質子峰向低場移動,這稱為van der Waals效應。氫鍵的影響、溶劑效應、van der Waals效應在剖析NMR圖譜時很有用。
(3)共軛效應
苯環上的氫若被推電子基取代,由於P-π共軛,使苯環電子云密度增大,質子峰向高場位移。而當有拉電子取代基則反之。對於雙鍵等體系也有類似的效果。
質子化學位移
由於不同類型的質子化學位移不同,因此化學位移值對於分辨各類質子是重要的,而確定質子類型對於闡明分子結構是十分有意義的。下表列出了一些特徵質子的化學位移,表中黑體字的H是要研究的質子。
| 質子的類型 | 化學位移 | 質子的類型 | 化學位移 |
| RC H3 | 0.9 | ArO H | 4.5-4.7(分子內締合10.5~16) |
| R2C H2 | 1.3 | ||
| R3C H | 1.5 | R2C=CR—O H | 15~19(分子內締合) |
![核磁共振[物理現象結構分析手段]](/img/0/d51/wZwpmL4ETO4UDM1YzM4EDN0UTMyITNykTO0EDMwAjMwUzL2MzL2EzLt92YucmbvRWdo5Cd0FmL0E2LvoDc0RHa.jpg) 核磁共振[物理現象結構分析手段] 核磁共振[物理現象結構分析手段] | 0.22 | RCH2O H | 3.4~4 |
| R2C=C H2 | 4.5~5.9 | ROC H3 | 3.5~4 |
| R2C=CR H | 5.3 | RC HO | 9~10 |
| R2C=CR—C H3 | 1.7 | RCOCR2— H | 2~2.7 |
| RC≡C H | 7~3.5 | HCR2COO H | 2~2.6 |
| ArCR2— H | 2.2~3 | R2C HCOOR | 2~2.2 |
| RC H2F | 4~4.5 | RCOOC H3 | 3.7~4 |
| RC H2Cl | 3~4 | RC≡CCOC H3 | 2~3 |
| RC H2Br | 3.5~4 | RN H2或R2N H | 0.5~5(峰不尖銳,常呈饅頭形) |
| RC H2I | 3.2~4 | ||
| RO H | 0.5~5.5(溫度、溶劑 、濃度改變時影響很大) | RCONR H或ArCONR H | 5~9.4 |
烷烴
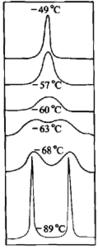 C6D11H在不同溫度下的1H-NMR譜
C6D11H在不同溫度下的1H-NMR譜甲烷氫的化學位移值為0.23,其它開鏈烷烴中,一級質子在高場 δ≈0.91處出現,二級質子移向低場在 δ≈1.33處出現,三級質子移向更低場在 δ≈1.5處出現。例如:
| 烷烴 | C H4 | C H3—C H3 | C H3—C H2—C H3 | (C H3)3C H | ||||
| δ | 0.23 | 0.86 | 0.86 | 0.91 | 1.33 | 0.91 | 0.86 | 1.50 |
甲基峰一般具有比較明顯的特徵,亞甲基峰和次甲基峰沒有明顯的特徵,而且常呈很複雜的峰形,不易辨認。當分子中引人其它官能團後,甲基、次甲基及亞甲基的化學位移會發生變化,但其 δ值極少超出0.7~4-5這一範圍。
環烷烴能以不同構象形式存在,未被取代的環烷烴處在一確定的構象中時,由於碳碳單鍵的 各向異性禁止作用,不同氫的 δ值略有差異。例如,在環己烷的椅型構象中,由於C-I上的平伏鍵氫處於C⑵ — C⑶鍵及C⑸ — C⑹鍵的去禁止區,而C-I上的直立鍵氫不處在去禁止區,(圖環己烷的各向異性禁止效應)。所以平伏鍵氫比直立鍵氫的化學位移略高0.2~0.5。在低溫(-100℃)構象固定時,NMR譜圖上可以清晰地看出兩個吸收峰,一個代表直立鍵氫,一個代表平伏鍵氫。但在常溫下,由於構象的迅速轉換(圖環己烷構象的轉換),一般只看到一個吸收峰(見右圖)。
其它未取代的環烷烴在常溫下也只有一個吸收峰。環丙烷的 δ值為0.22,環丁烷的 δ值為1.96,別的環烷烴的 δ值在1.5左右。取代環烷烴中,環上不同的氫有不同的化學位移,它們的圖譜有時呈比較複雜的峰形,不易辨認。
烯烴
烯氫是與雙鍵碳相連的氫,由於碳碳雙鍵的各向異性效應,烯氫與簡單烷烴的氫相比 δ值均向低場移動3~4乙烯氫的化學位移約為5.25,不與芳基共軛的取代烯氫的化學位移約在 4.5~6.5範圍內變化,與芳基共軛時 δ值將增大。乙烯基對甲基、亞甲基、次甲基的化學位移也 有影響。例如:
| 化合物 | C H4 | C H3—CH=CH2 | C H3—C H3 | C H3—C H2—CH=CH2 | (CH3)2C H2 | (CH3)2C H—CH=CH2 | ||
| δ | 0.23 | 1.71 | 0.86 | 0.86 | 1.00 | 2.00 | 1.33 | 1.73 |
從上面的數據可以看出,同碳上有乙烯基的氫 δ值約在1.59~2.14之間,變化較大,鄰碳上有乙烯基的氫, δ值變化較小。
炔烴
炔基氫是與三鍵碳相連的氫,由於炔鍵的禁止作用,炔氫的化學位移移向高場,一般 δ=1.7~3-5 處有一吸收峰。例如,HC≡C H(1.80),RC≡C H(1.73~1.88),ArC≡C H(2.71~3-37),—CH=CH-C≡C H(2.60~3.10),—C≡C—C≡CH(1.75~2.42),CH3-C≡C-C≡C-C≡C H(1.87)。HC≡C—若連在一個沒有氫的原子上,則炔氫顯示一個尖銳的單峰。炔基對甲基、 亞甲基的化學位移有影響,與炔基直接相連的碳上的氫化學位移影響最大,其 δ值約為1.8~2.8。
芳烴
由於受π電子環流的去禁止作用,芳氫的化學位移移向低場,苯上氫的 δ=7.27。萘上的質 子受兩個芳環的影響 δ值更大,α質子的 δ為7.81,β質子的 δ為7.46。一般芳環上質子的在 δ值在6.3~8.5範圍內,雜環芳香質子的 δ值在6.0~9.0範圍內。
鹵代烴
由於鹵素電負性較強,因此使直接相連的碳和鄰近碳上質子所受禁止降低,質子的化學位移向低場方向移動,影響按F,Cl,Br,I的次序依次下降。與鹵素直接相連的碳原子上的質子化學位移一般在 δ=2.16~4.4之間,相鄰碳上質子所受影響減小, δ=1.25~1.55之間,相隔一個碳原子時,影響更小, δ= 1.03~1.08之間。
羧酸衍生物
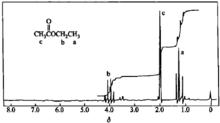 乙酸乙酯的核磁共振氫譜
乙酸乙酯的核磁共振氫譜酯中烷基上的質子RCOOCH2R的化學位移 δH=3.7~4。醯胺中氮上的質子RCONHR 的化學位移,一般在 δ= 5~9.4之間,往往不能給出一個尖銳的峰。
羰基或氮基附近α碳上的質子具有類似的化學位移= 2~3,例如,CH3COCl δH=2.67,CH3COOCH3 δH=2.03, RCH2COOCH3 δH=2.13,CH3CONH2 δH= 2.08,RCH2CONH2 δH=2.23,CH3CN δH=1.98,RCH2CN δH=2.30。
其他
醇的核磁共振譜的特點參見後文。醚α-H的化學位移約在3.54附近。
酚羥基氫的核磁共振的 δ值很不固定,受溫度、濃度、溶劑的影響很大,只能列出它的大致范 圍。一般酚羥基氫的 δ值在4~8範圍內,發生分子內締合的酚羥基氫的 δ值在10.5~16范 圍內。
羧酸H的化學位移在2~2.6之間。羧酸中羧基的質子由於受兩個氧的吸電子作用,屏 蔽大大降低,化學位移在低場。R2CHCOOH δH=10~12。
胺中,氮上質子一般不容易鑑定,由於氫鍵程度不同,改變很大,有時N— H和C一H質子 的化學位移非常接近,所以不容易辨認。一般情況在α-H δH=2.7~3.1,β-H δ=1.1~1.71。N-H δ=0.5~5,RNH2,R2NH的 δ值的大致範圍在0.4~3.5,ArNH2,ArzNH,ArNHR的 δ值的大 致範圍在2.9~4.8之間。
碳化學位移
13C的化學位移亦以四甲基矽為內標,規定 δTMS = 0,其左邊值大於0,右邊值小乾0。與1H的化學位移相比,影響13C的化學位移的因素更多,但自旋核周圍的電子禁止是重要因素之一, 因此對碳核周圍的電子云密度有影響的任何因素都會影響它的化學位移。碳原子是有機分子的骨架,氫原子處於它的外圍,因此分子間碳核的互相作用對 δc的影響較小,而分子本身的結構及 分子內碳核間的相互作用對 δc影響較大。碳的雜化方式、分子內及分子間的氫鍵、各種電子效 應、構象、構型及測定時溶劑的種類、溶液的濃度、體系的酸鹼性等都會對 δc產生影響。如今已 經有了一些計算 δc的近似方法,可以對一些化合物的 δc作出定性的或半定量的估算,但更加完 善的理論還有待於進一步的探討研究。下表是根據大量實驗數據歸納出來的某些基團中C的化學位移,表中黑體字的碳是要研究的對象。
| 碳的類型 | 化學位移 | 碳的類型 | 化學位移 |
| CH4 | -2.68 | 醚的α 碳(三級) | 70~85 |
| 直鏈烷烴 | 0~70 | 醚的α 碳(二級) | 60~75 |
| 四級 C | 35~70 | 醚的α 碳(一級) | 40~70 |
| 三級 C | 30~60 | 醚的α 碳(甲基碳) | 40~60 |
| 二級 C | 25~45 | R COOH R COOR | 160~185 |
| 一級 C | 0~30 | R COCl R CONH2 | 160-180 |
| CH2=CH2 | 123.3 | 醯亞胺的羰基 碳 | 165~180 |
| 烯 碳 | 100~150 | 酸酐的羰基 碳 | 150-175 |
| CH≡CH | 71.9 | 取代尿素的羰基 碳 | 150~175 |
| 炔 碳 | 65~90 | 胺的α 碳(三級) | 65~75 |
| 環丙烷的環 碳 | — 2.8 | 胺的α 碳(二級) | 50~70 |
| ( CH2)n 4~7 | 22~27 | 胺的α 碳(一級) | 40~60 |
| 苯環上的 碳 | 128.5 | 胺的α 碳(甲基碳) | 20~45 |
| 芳烴,取代芳烴中的芳 碳 | 120~160 | 氰基上的 碳 | 110~126 |
| 芳香雜環上的 碳 | 115~140 | 異氰基上的 碳 | 155~165 |
| - CHO | 175~205 | R2 C=N-OH | 145~165 |
| C=C- CHO | 175~195 | RN CO | 118~132 |
| α-鹵代醛的羰基 碳 | 170~190 | 硫醚的α 碳(三級) | 55~70 |
| R2C=O(包括環酮)的羰基 碳 | 200~220 | 硫醚的α 碳(二級) | 40~55 |
| 不飽和酮和芳酮的羰基 碳 | 180~210 | 硫醚的α 碳(一級) | 25~45 |
| α-鹵代酮的羰基 碳 | 160~200 | 硫醚的α 碳(甲基碳) | 10~30 |
偶合常數
自旋偶合的量度稱為自旋的偶合常數(coupling constant),用符號J表示,J值的大小表示 了偶合作用的強弱J的左上方常標以數字,它表示兩個偶合核之間相隔鍵的數目,J的右下方 則標以其它信息。就其本質來看,偶合常數是質子自旋 裂分時的兩個核磁共振能之差,它可以通過共振吸收的位置差別來體現,這在圖譜上就是裂分峰 之間的距離。
偶合常數的大小與兩個作用核之間的相對位置有關,隨著相隔鍵數目的增加會很快減弱,一 般來講,兩個質子相隔少於或等於三個單鍵時可以發生偶合裂分,相隔三個以上單鍵時,偶合常 數趨於零。例如在丁酮中,Ha與Hb之間相隔三個單鍵,因此它們之間可以發生偶合裂分,而 Ha與Hb或Hb與Hc之間相隔三個以上的單鍵,它們之間的偶合作用極弱,也即偶合常數趨於零。但中間插人雙鍵或三鍵的兩個質子,可以發生遠程偶合。
化學位移隨外磁場的改變而改變。偶合常數與化學位移不同,它不隨外磁場的改變而改變。因為自旋偶合產生於磁核之間的相互作用,是通過成鍵電子來傳遞的,並不涉及外磁場。因此, 當由化學位移形成的峰與偶合裂分峰不易區別時,可通過改變外磁場的方法來予以區別。
自旋偶合和自旋裂分
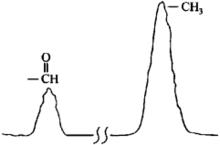 乙醛的低分辨核磁共振譜圖
乙醛的低分辨核磁共振譜圖兩張圖譜分別是低分辨核磁共振儀和高分辨核磁共振儀所作的乙醛 (CH3CHO)的PMR圖譜。對比這兩張圖譜可以發現,用低分辨核磁共振儀作的圖譜,乙醛只有 兩個單峰。在高分辨圖譜中,得到的是二組峰,它們分別是二重峰、四重峰。乙醛在低分辨圖譜 和高分辨圖譜中峰數不等是因為在分子中,不僅核外的電子會對質子的共振吸收產生影響,鄰近 質子之間也會因互相之間的作用影響對方的核磁共振吸收。並引起譜線增多。這種原子核之間的相互作用稱為自旋-自旋偶合(spin-spin coupling),簡稱自旋偶合(spin coupling)。因自旋偶合而引起的譜線增多的現象稱為自旋-自旋裂分,簡稱自旋裂分。
自旋耦合的起因
譜線裂分是怎樣產生的?在外磁場的作用下,質子是會自旋的,自旋的質子會產生一個小的磁矩,通過成鍵價電子的傳遞,對鄰近的質子產生影響。質子的自旋有兩種取向,假如外界磁場感應強度為自旋時與外磁場取順向排列的質子,使受它作用的鄰近質子感受到的總磁感應 強度為B0+B',自旋時與外磁場取逆向排列的質子,使鄰近的質子感受到的總磁感應強度為B0-B',因此當發生核磁共振時,一個質子發出的信號就分裂成了兩個,這就是自旋裂分。一般只有相隔三個化學鍵之內的不等價的質子間才會發生自旋裂分的現象。
磁等價磁不等價性
在分子中,具有相同化學位移的核稱為化學位移等價的核。分子中兩相同原子處於相同的 化學環境時稱為化學等價(chemical equivalence),化學等價的質子必然具有相同的化學位移,例 如CH2Cl2中的兩個1H是化學等價的,它們的化學位移也是相同的。但具有相同化學位移的質 子未必都是化學等價的。判別分子中的質子是否化學等價,對於識譜是十分重要的,通常判別的依據是:分子中的質子,如果可通過對稱操作或快速機制互換,它們是化學等價的。通過對稱軸 旋轉而能互換的質子叫等位質子(homotopic proton)。
等位質子在 任何環境中都是化學等價的。通過鏡面對稱操作能互換的質子叫對映異位質子(enantiotopic Pmton)。一組化學位移等價(chemical shift equivalence)的核,如對組外任何其它核的偶合常數彼此之間 也都相同,那么這組核就稱為磁等價(magnetic equivalence)核或磁全同核。顯然,磁等價的核一定是化學等價的,而化學等價的核不一定是磁等價的。
在判別分子中的質子是否化學等價時,下面幾種情況要予以注意。
⑴與不對稱碳原子相連的CH2上的兩個質子是化學不等價的。不對稱碳原子的這種影響可以延伸到更 遠的質子上。
⑵在烯烴中,若雙鍵上的一個碳連有兩個相同的基團,另一個雙鍵碳連有兩個氫,則這兩 個氫是化學等價的,與帶有某些雙鍵性質的單鍵相連的兩 個質子,在單鍵旋轉受阻的情況下,也能用同樣的方法來判別它們的化學等價性。
⑶有些質子在某些條件下是化學不等價的,在另一些條件下是化學等價的。例如環己烷 上的CH2,當分子的構象固定時,兩個質子是化學不等價的,當構象迅速轉換時,兩個質子是化學等價的。只有化學不等價的質子才能顯示出自旋偶合。
曲線和峰面積
核磁共振譜中,共振峰下面的面積與產生峰的質子數成正比,因此峰面積比即為不同類型質 子數目的相對比值,若知道整個分子中的質子數,即可從峰面積的比例關係算出各組磁等價質子 的具體數目。核磁共振儀用電子積分儀來測量峰的面積,在譜圖上從低場到髙場用連續階梯積 分曲線來表示。積分曲線的總髙度與分子中的總質子數目成正比,各個峰的階梯曲線髙度與該 峰面積成正比,即與產生該吸收峰的質子數成正比。各個峰面積的相對 積分值也可以在譜圖上直接用數字顯示出來,如果將含一個質子的峰的面積指定為1,則圖譜上 的數字與質子的數目相符。
圖譜的剖析
1H核磁共振圖譜提供了積分曲線、化學位移、峰形及偶合常數等信息。圖譜的剖析就是合 理地分析這些信息,正確地推導出與圖譜相對應的化合物的結構。通常採用如下步驟。
⑴標識雜質峰在1H-NMR譜中,經常會出現與化合物無關的雜質峰,在剖析圖譜前,應 先將它們標出。最常見的雜質峰是溶劑峰,樣品中未除盡的溶劑及測定用的氘代溶劑中夾雜的 非氘代溶劑都會產生溶劑峰。為了便於識別它們,下表列出了最常用溶劑的化學位移。
| 常用溶劑 | 化學位移 | 常用溶劑 | 化學位移 |
| 環己烷 | 1.40 | 丙酮 | 2.05 |
| 苯 | 7.20 | 乙酸 | 2.05 8.50(COOH)* |
| 氯仿 | 7.27 | 四氫呋喃 | (α)3.60(β)1.75 |
| 乙腈 | 1.95 | 二氧六環 | 3.55 |
| 1,2-二氯乙烷 | 3.69 | 二甲亞碸 | 2.50 |
| 水 | 4.7 | N,N-二甲基甲醯胺 | 2.77,2.95,7.5(CHO)* |
| 甲醇 | 3.35 4.8* | 矽膠雜質 | 1.27 |
| 乙醚 | 1.16 3.36 | 吡啶 | (α)8.50(β)6.98(γ)7.35 |
| *數值隨測定條件而有變化。 | |||
還有兩個需要標識的峰是旋轉邊峰和13C同位素邊峰。在1H-NMR測定時,旋轉的樣品管 會產生不均勻的磁場,導致在主峰兩側產生對稱的小峰,這一對小峰稱為旋轉邊峰,旋轉邊峰與 主峰的距離隨樣品管旋轉速度的改變而改變。在調節合適的儀器中旋轉邊峰可消除。13C與1H 能發生偶合併產生裂分峰,這對裂分峰稱為13C同位素邊峰。由於13C的大然豐度僅為1.1%,只有在濃度很大或圖譜放大時才會發現13C同位素邊峰。
⑵根據積分曲線計算各組峰的相應質子數,若圖譜中已直接標出質子數,則此步驟可省。
⑶根據峰的化學位移確定它們的歸屬。
⑷根據峰的形狀和偶合常數確定基團之間的互相關係。
⑸採用重水交換的方法識別活潑氫由於一OH,一NH2,一COOH上的活潑氫能與D2O發生交換。而使活潑氫的信號消失,因此對比重水交換前後的圖譜可以基本判別分子中是否含有活潑氫。
⑹綜合各種分析,推斷分子結構並對結論進行核對。
圖譜的簡化
一級圖譜比較簡單,可以直接根據上面所述幾個方面來進行剖析,但解剖的順序可以根據實 際情況靈活掌握。高級圖譜的譜線一般都很複雜,難以直接剖析,為了便於解剖,最好在剖析前, 先採用合理的方法簡化圖譜a簡化圖譜常用的方法請參閱有關專著。
去偶處理
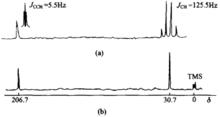 丙酮的13C譜圖
丙酮的13C譜圖13C的核磁共振原理與1H的核磁共振原理相同,因此13C與直接相連的氫核也會發生偶合作用。由於有機分子大都存在碳氫鍵,從而使裂分譜線彼此交疊,譜圖變得複雜而難以辨認,只有通過去偶處理,才能使譜圖變得清晰可辨。最常用的去偶法是質子(噪聲)去偶法。該法採用雙照射法,照射場(H2)的功率包括所有處於各種化學環境中氫的共振頻率,因此能將13C與所有氧核的偶合作用消除,使只含C、H、O、N的普通有機化合物的13C-NMR譜圖中,13C的信號都變成單峰,即所有不等性的13C核都有自己的獨立信號。因此,該法能識別分子中不等性的碳核。下圖是丙酮的13C譜。(a)是偶合譜,(b)是質子去偶譜。在偶合譜中,羰基碳( δ=206.7)與六個氫發生二鍵偶合,裂分成七重峰,α碳( δ=30.7)與三個氫發生一鍵偶合,裂分成四重峰。在質子去偶譜中,羰基碳和α碳的裂分峰均變成了單峰。丙酮有兩個相同的α碳和一個羰基碳,α碳的峰強度較羰基碳的峰強度大。質子(噪聲)去偶碳譜就是通常說的碳譜,又稱為寬頻去偶碳譜,用13C{H}表示。其它去偶的方 式還很多,有興趣的讀者請參閱有關專著。
![核磁共振[物理現象結構分析手段] 核磁共振[物理現象結構分析手段]](/img/5/4e1/nBnauM3X4cTO5AzN2UDNyIDN0UTMyITNykTO0EDMwAjMwUzL1QzL1czLt92YucmbvRWdo5Cd0FmLxE2LvoDc0RHa.jpg)
