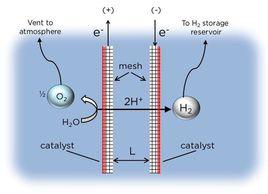
塔菲爾反應公式
 塔菲爾反應
塔菲爾反應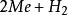 塔菲爾反應
塔菲爾反應⇌
氫超電勢
關於氫在陰極析出的機理,從20世紀30年代開始就有人提出了不同的理論,例如遲緩放電理論和複合理論等,雖然不同的人提出的理論不同,但也有一些共同點,如:都提出了H 的放電可分為幾個步驟進行:
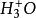 塔菲爾反應
塔菲爾反應(1) 從本體溶液擴散到電極附近;
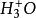 塔菲爾反應
塔菲爾反應(2) 從電極附近的溶液中移到電極;
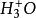 塔菲爾反應
塔菲爾反應(3) 在電極上以下列機理放放電機制有兩類:
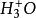 塔菲爾反應
塔菲爾反應(a) 在電極表面上放電而形成H原子,吸附在電極表面(伏爾默反應)
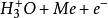 塔菲爾反應
塔菲爾反應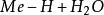 塔菲爾反應
塔菲爾反應⇌
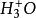 塔菲爾反應
塔菲爾反應其中Me表示金屬電極。在鹼性溶液中,由於 離子少,而直接在陰極上放電的可能是水分子
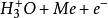 塔菲爾反應
塔菲爾反應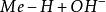 塔菲爾反應
塔菲爾反應⇌
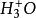 塔菲爾反應
塔菲爾反應(b) 與已經吸附在電極表面上的氫原子H反應生成H(稱為海洛夫斯基反應)
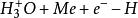 塔菲爾反應
塔菲爾反應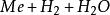 塔菲爾反應
塔菲爾反應⇌
(a)、(b)都是電化學步驟,由於(b)中還包含吸附氫的脫附過程,故反應(b)又稱為電化學脫附步驟。
(4)塔菲爾反應
(5)已經證明,步驟(1)、(2)不能影響反應速率,至於步驟(2)、(3)、(4)究竟哪一步是影響反應速率的慢步驟,各種意見並不一致。遲緩放電理論認為(3)是決速步,而複合理論則認為(4)是慢步驟,但不同的理論最後都得到塔非爾關係式。
塔菲爾經驗公式
1905年,塔菲爾提出了氫超電勢的經驗公式,表示了氫超電勢與電流密度的定量關係,即:
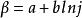 塔菲爾反應
塔菲爾反應式中j是電流密度;a、b是常數。a是電流密度等於10000A·m 時的超電勢值,它與電極材料、電極表面狀態、溶液組成及實驗溫度等有關。b的數值對於大多數金屬而言相差不大,在常溫下接近0.050V。因此,氫超電勢的大小基本上取決於a的大小,a愈大,氫超電勢也愈大,電極反應的不可逆程度也愈大。