實驗器材
儀器
分光光度計,恆溫水浴鍋
試劑
(1) 95%乙醇或無水乙醇。
(2) 70%乙醇。
(3) 乙醚。
(4) 0.05mol/L鹽酸溶液。
(5) 0.5mol/L氫氧化鈉溶液。
(6) 0.15%咔唑試劑
稱取化學純咔唑0.15g,溶解於精製乙醇中,並定容到100mL。咔唑溶解緩慢,需加以攪拌。
(7) 精製乙醇
取無水乙酵或95%乙醇1000mL,加入鋅粉4g,硫酸(1:1) 4mL,在水浴中回流10h,用全玻璃儀器蒸餾,餾出液每1000mL加鋅粉和氫氧化鉀各4g,重新蒸餾一次。
(8) 半乳糖醛酸標準貯備溶液
準確稱取半乳糖醛酸100mg,溶於蒸餾水並定容到100mL,得濃度為1 mg/mL半乳糖醛酸標準貯備液。
(9) 半乳糖醛酸標準工作液
分別準確吸取0mL、1.0mL、2.0mL、3.0mL、4.0mL、5.0mL、6.0mL、7.0mL半乳糖醛酸標準貯備溶液於8個100mL容量瓶中,用水稀釋至刻度,得一組濃度分別為0mg/L、10mg/L、20mg/L、30mg/L、40mg/L、50mg/L、60mg/L、70mg/L的半乳糖醛酸標準工作液。
(10) 濃硫酸優級純。
(11) 甲基紅指示劑。
實驗步驟
樣品處理
(1) 新鮮樣品稱取試樣30~50g,用小刀切成薄片,置於預先放有無水乙醇的500mL錐形瓶中。裝上回流冷凝器,在水浴上沸騰回流15min後,冷卻。用布氏漏斗過濾,殘渣移至研缽中,一邊慢慢磨碎,一邊滴加70%的熱乙醇,冷卻後再過濾,反覆操作至濾液不呈糖的反應(用苯酚一硫酸法檢驗)為止。殘渣用無水乙醇洗滌脫水,再用乙醚洗滌以除去脂類和色素,漏斗中殘渣在空氣中揮發去乙醚。
(2) 乾燥樣品 研細,過60目篩,取5~10g樣品於燒杯中,加入熱的70%乙醇,充分攪拌以提取糖類,過濾。反覆操作至濾液不呈糖的反應。殘渣用無水乙醇洗滌,再用乙醚洗滌,最後讓乙醚揮發掉。
提取果膠
(1) 水溶性果膠提取用150mL水將上述揮發至乾的殘渣移人250ml燒杯中,加熱至沸並保持沸騰1h,隨時補足蒸發的水分,冷卻後移入250mL容量瓶中,加水定容,搖勻,過濾,棄去初濾液,收集濾液即為水溶性果膠提取液。
(2) 總果膠的提取用150mL加熱至沸的0.05mol/L鹽酸溶液把揮乾的殘渣移入250mL錐形瓶中,裝上冷凝器,於沸水浴中加熱回流1h,冷卻後移入250mL容量瓶中,加甲基紅指示劑2滴,加0.5mol/L氫氧化鈉中和後,用水定容,搖勻,過濾,收集濾液即為總果膠提取液。
(3) 標準工作曲線的製作取8支50mL比色管,各加入12mL濃硫酸,置冰水浴中,邊冷卻邊緩緩依次加入濃度為0mg/L、10mgL/、20mg/L、30mg/L、40mg/L、50mg/L、60mg/L、70mg/L的半乳糖醛酸標準溶液2mL,充分混合後,再置冰水浴中冷卻。然後在沸水浴中準確加熱10min,用流動水迅速冷卻到室溫,各加入0.15%咔唑試劑1mL,充分混合,置室溫下放置30min,以0號管為空白在530nm波長下測定吸光度,繪製標準工作曲線。
(4) 測定取果膠提取液,用水稀釋到適當濃度(含半乳糖醛酸10~70mg/L)。取2mL稀釋液於50mL比色管中,以下按製作標準曲線的方法操作,測定吸光度。從標準曲線上查出半乳糖醛酸濃度(mg/L)。
計算
計算公式如下:
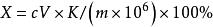 咔唑比色法
咔唑比色法式中X—樣品中果膠物質(以半乳糖醛酸計)的質量分數,%;
c—從標準曲線上查得的半乳糖醛酸濃度,mg/L;
V—果膠提取液總體積,mL;
K—提取液稀釋倍數;
m—樣品質量,g。
注意事項
(1) 糖分的存在對咔唑的呈色反應影響較大,使結果偏高,故樣品處理時應充分洗滌以除去糖分。
(2) 檢驗糖分的苯酚一硫酸法:取檢液1mL,置於試管中,加入5%苯酚水溶液1mL,再加入硫酸5mL,混勻,如溶液呈褐色,證明檢液中含有糖分。
(3)硫酸的濃度對呈色反應影響較大,半乳糖醛酸在低濃度的硫酸中與咔唑試劑的呈色度極低,甚至不顯色,只有在濃硫酸中才可使其顯色,且顏色深淺與濃硫酸濃度和純度有關。故在測定樣液和製作標準曲線時,應使用同規格、同批號的濃硫酸,以保證其濃度、純度一致。
(4 )本法的測定結果以半乳糖醛酸表示,因不同來源的果膠中半乳糖醛酸的含量不同,如甜橙為77.7%,檸檬為94.2%,柑橘為96%,蘋果為72%~75%。若把結果換算為果膠的含量,可按上述關係計算換算係數。

