基本信息
中文名稱:右美托咪定
英文名稱:dexmedetomidine
英文別名:Dexmedetomidine; 5-[(1S)-1-(2,3-dimethylphenyl)ethyl]-1H-imidazole; Dexmedetomidina; (S)-medetomidine; Dexmedetomidinum;
CAS號:113775-47-6
分子式:C13H16N2
分子量:200.28000
化學結構式:
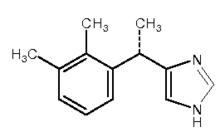 右美托咪定
右美托咪定精確質量:200.13100
PSA:28.68000
LogP:3.17830
物化性質
密度:1.053g/cm
沸點:381.9ºC at 760mmHg
閃點:191.3ºC
折射率:1.569
蒸汽壓:1.08E-05mmHg at 25°C
安全信息
海關編碼:2933290090
海關數據
中國海關編碼:2933290090
概述:2933290090. 其他結構含非稠合咪唑環的化合物. 增值稅率:17.0%. 退稅率:13.0%. 監管條件:無. 最惠國關稅:6.5%. 普通關稅:20.0%
申報要素:品名, 成分含量, 用途, 烏洛托品請註明外觀, 6-己內醯胺請註明外觀, 簽約日期
藥品相關信息概覽
藥品名稱
中文名稱:右美托咪定
英文名稱:Dexmedetomidine
別名:鹽酸右美托咪定;Dexmedetomidine Hydrochloride;Precedex
分類
神經系統藥物> 鎮靜及催眠藥物 > 其他
劑型
注射液
藥理作用
右美托咪定是一種相對選擇性α2-腎上腺素受體激動劑,具有鎮靜作用。動物緩慢靜脈輸注右美托咪定10~300μg/kg時可見對α2-腎上腺素受體的選擇性作用,但在較高劑量下(≥1000μg/kg)緩慢靜脈輸注或快速靜脈注射給藥時對α1和α2-受體均有作用。
藥代動力學
右美托咪定經皮下注射或肌注後快速吸收,達峰值時間為1h,右美托咪定靜滴後,分布半衰期約為6min,穩態分布容積約為118L。右美托咪定在體內經廣泛代謝後,代謝物主要隨尿液排出。消除半衰期約為2h,清除期約為39L/h。
適應證
右美托咪定適用於用於行全身麻醉的手術患者氣管插管和機械通氣時的鎮靜。
禁忌證
1.對右美托咪定過敏者禁用。
2.懷孕、哺乳期婦女,晚期心臟阻滯患者慎用。
注意事項
1.患者輸注右美托咪定時應進行連續監測。
2.右美托咪定不可與血液或血漿經同一靜注導管合用。
3.有明顯心血管機能障礙的患者需預先採取復甦措施。
4.右美托咪定連續輸注不可超過24h。
孕婦及哺乳期婦女用藥
在孕婦未進行充分良好的臨床研究。右美托咪定只有在潛在的好處大於對胎兒潛在的危險時才可以在孕婦使用。本品對待產和生產孕婦的安全性尚未研究。因此,在待產和生產期間包括剖腹產術時不推薦本品。
尚不知道本品是否分泌到人乳中。放射性同位素示蹤的右美托咪定皮下給予哺乳的雌鼠後在乳汁中分泌。因為許多藥物在人乳中分泌,哺乳期婦女應當慎用本品。
兒童用藥
本品在18歲以下的兒童患者的安全性和有效性尚不明確。因此,本品不推薦用於這些人群。
老年用藥
已知右美托咪定主要通過腎臟排泄,該藥在腎功能損傷的病人中發生不良反應的危險性更大。年老的病人腎功能降低,因此對年老的病人應當謹慎選擇劑量,並且監測腎臟功能可能是有用的。國外臨床研究中,重症監護室鎮靜試驗中共有729例患者≥65歲,200例患者≥75歲。65歲以上患者中,給予本品後心動過緩和低血壓的發生率較高。因此65歲以上患者使用本品時需考慮降低劑量。 程式鎮靜的臨床試驗中共有131例患者≥65歲,47例患者≥75歲。低血壓的發生率65歲或以上為72%、75歲或以上為74%,65歲以上患者為47%。因此65歲以上患者使用本品時應當減少負荷劑量,建議以0.5μg/kg,輸注10分鐘以上。
不良反應
右美托咪定耐受性良好,常見的不良反應包括低血壓、噁心、心搏徐緩、組織缺氧和心房顫動。
用法用量
成人劑量:配成4ug/ml濃度以1ug/kg劑量緩慢靜注,輸注時間超過10分鐘。本品在給藥前必須用0.9%的氯化鈉溶液稀釋達濃度4ug/ml,可取出2ml本品加入48ml0.9%的氯化鈉注射液中形成總的50ml溶液,輕輕搖動使均勻混合。
與其它藥物的相互作用
1.右美托咪定與麻醉劑、鎮靜劑、催眠藥和阿片類藥物(如七氟烷,異氟烷,丙泊酚,阿芬太尼,咪達唑侖)合用可能會提高療效。
2.右美托咪定不影響羅庫溴銨的神經肌肉阻滯作用。
毒理研究
遺傳毒性
右美托咪定Ames試驗、哺乳動物細胞正向基因突變試驗結果均為陰性;大鼠S9代謝活化條件下的體外人體淋巴細胞染色體畸變試驗、NMRI小鼠的體內微核試驗為陽性,但在有或無人體S9代謝活化條件下的體外人體淋巴細胞染色體畸變試驗、CD-1小鼠的體內微核試驗結果為陰性。
生殖毒性
雄性或雌性大鼠自交配前分別10周和3周直至交配期間,每日皮下注射給予右美托咪定劑量高達54μg/kg(根據μg/m計算,低於最大推薦人體靜脈注射給藥劑量)未見對生育力的影響。
大鼠妊娠第5~16天皮下注射給予右美托咪定劑量高達200μg/kg、家兔妊娠第6-18天皮下注射劑量高達96μg/kg,未見致畸作用。根據μg/m計算,大鼠劑量相當於最大推薦人體靜脈注射給藥劑量的2倍;根據血漿藥物AUC值,家兔的暴露量與最大推薦人體靜脈注射給藥劑量下的暴露量相似。大鼠在劑量為200μg/kg時可見胎仔毒性,表現為著床後丟失增加,存活幼仔數減少。無影響劑量為20μg/kg(根據μg/m計算,低於最大推薦人體靜脈注射給藥劑量)。大鼠自妊娠第16天至哺乳期間皮下注射給予右美托咪定,在劑量為8、32μg/kg(根據μg/m計算,低於最大推薦人體靜脈注射給藥劑量)時導致幼仔體重減輕,32μg/kg劑量組幼仔可見運動功能發育遲滯。32μg/kg劑量組F2代還可見胚胎與胎仔毒性。2μg/kg劑量下未見上述毒性。
妊娠大鼠皮下注射給予放射性標記的右美托咪定,可見胎盤轉運。

