公式
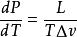 克克方程
克克方程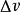 克克方程
克克方程此處dP/dT 是壓強隨溫度的變化率, L是相變焓(早年稱為潛熱),T 是相平衡溫度, 是相變過程中的比容變化。
在化學中一般討論理想氣體狀態下的克克方程,也是從理想狀態氣體開始推導。
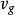 克克方程
克克方程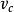 克克方程
克克方程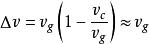 克克方程
克克方程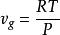 克克方程
克克方程對於有氣相參加的相變過程,氣相比容體積 要遠遠大於固體或液體的體積 ,所以固體和液體的體積可以忽略 在較低的壓力和氣體分子間作用力的前提下,氣體可以近似視為理想氣體 ,此處R是氣體常數。於是
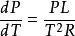 克克方程
克克方程這就被稱為克勞修斯-克拉佩龍方程。
相變焓
一般來說,相變焓是溫度的函式,但如果相變焓隨溫度變化不大, 那么可以積分得
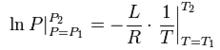 克克方程
克克方程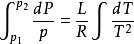 克克方程
克克方程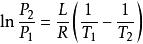 克克方程
克克方程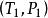 克克方程
克克方程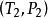 克克方程
克克方程這裡 和 是P-T圖上的兩個點,這是很有用的一個關係,因為他聯繫了飽和蒸汽壓、溫度和相變焓。不需要比容的數據,就可以估算飽和蒸汽壓隨溫度變化的關係。

