概述
將燃料與氧化劑的化學能通過電化學反應直接轉換成電能的發電裝置。燃料電池理論上可在接近100%的熱效率下運行,具有很高的經濟性。目前實際運行的各種燃料電池,由於種種技術因素的限制,再考慮整個裝置系統的耗能,總的轉換效率多在45%~60%範圍內,如考慮排熱利用可達80%以上。此外,燃料電池裝置不含或含有很少的運動部件,工作可靠,較少需要維修,且比傳統發電機組安靜。另外電化學反應清潔、完全,很少產生有害物質。所有這一切都使得燃料電池被視作是一種很有發展前途的能源動力裝置 。
原理
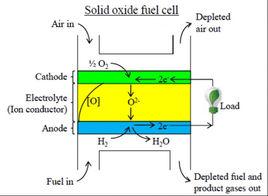
一氧化碳-氧燃料電池是一種能量轉化裝置,它是按電化學原理,即原電池工作原理,等溫的把貯存在一氧化碳和氧化劑中的化學能直接轉化為電能,因而實際過程是氧化還原反應。燃料電池主要由四部分組成,即陽極、陰極、電解質和外部電路。一氧化碳氣和氧化氣分別由燃料電池的陽極和陰極通入。一氧化碳氣在陽極上放出電子,電子經外電路傳導到陰極並與氧化氣結合生成離子。離子在電場作用下,通過電解質遷移到陽極上,與一氧化碳反應,構成迴路,產生電流。同時,由於本身的電化學反應以及電池的內阻,燃料電池還會產生一定的熱量。電池的陰、陽兩極除傳導電子外,也作為氧化還原反應的催化劑。當燃料為碳氫化合物時,陽極要求有更高的催化活性。陰、陽兩極通常為多孔結構,以便於反應氣體的通入和產物排出。電解質起傳遞離子和分離燃料氣、氧化氣的作用。為阻擋兩種氣體混合導致電池內短路,電解質通常為緻密結構。
反應過程
通CO的一極為負極,通O的一極為正極。
總反應為:2CO+O==2CO
正極反應為:O+4e +4H ==2HO
負極反應為:2CO-4e +2HO==2CO+4H
其中正極反應是O2在酸性條件下的反應,負極反應是通過總反應減去正極反應得到 。