歷史研究
關於在疏水色譜分離技術進行分離的概念最早在1948年就由Tiselius提出,“疏水作用”一詞是Kauzmann於1959年首次在“蛋白質進展”雜誌中提出的,隨後陸續有學者發表用疏水層析成功分離蛋白質的文獻報導;如鈣調蛋白、苯丙氨酸裂解酶、凝集素等。該技術真正得到發展和套用是在20世紀70年代早期開發出一系列適合進行疏水作用色譜的固定相以後。1972年,Erel Z.等人將不同鏈長的α,ω-二胺同系物鍵合在瓊脂糖上,以不同pH的含鹽緩衝液作流動相成功純化了糖原磷酸化酶,開始確立了疏水層析在分離純化某些疏水蛋白質、肽類等生物大分子的重要作用。此後隨著新型色譜介質的開發生產和對機理認識的逐步深人,該技術得到了廣泛的套用,並且隨著高效疏水作用色譜介質的出現,HIC已在HPLC平台上被使用,稱為高效疏水作用色譜(High performance hydrophobic interaction chromatography HP-HIC)。
概念與原理
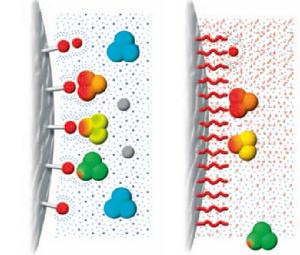
疏水色譜分離技術是利用樣品中各組分具有不同的疏水作用的性質進行分離,主要分離對象是蛋白質。疏水作用色譜固定相的非極性比較弱,流動相多採用高濃度鹽緩衝液進行梯度洗脫。溫和的分離條件,可以避免反相色譜中由於固定相較強的疏水性和有機流動相引起蛋白質的不可逆吸附和變性,因此特別適用於活性物質的分離與純化。疏水作用色譜的固定相表面為弱疏水性基團,它的疏水性比反相色譜用的固定相低幾十到幾百倍,而流動相為高離子濃度的鹽溶液。蛋白質分子在這樣的固定相和流動相中進行分配,蛋白質分子上的疏水性基團和固定相的疏水基團作用而被保留。當用流動相洗脫時逐漸降低流動相的離子強度,洗脫能力增強。利用被分離組分分子表面的疏水微區、(可逆)變性後暴露出的疏水殘基,或在高鹽環境下暴露於分子表面的疏水殘基與固定相的疏水性 配體之間的作用強弱,依次用從高至低離子強度洗脫液可將疏水作用由弱到強的組分分離開。蛋白質分子按其疏水性大小被依次洗脫出來,疏水性小的先流出。在這樣的高鹽水溶液中,蛋白質不會失活。高濃度鹽與水分子發生強烈作用,導致疏水分子周圍形成空穴的水分子減少,促進疏水性分子與介質的疏水配基之間發生結合。這種疏水作用的大小取決於固定相和溶質的極性、流動相的組成和濃度。由於各種蛋白質表面胺基酸殘基極性不同,因此有可能通過改變固定相的極性和流動相的組成使蛋白質得到分離。
疏水層析的原理完全不同於離子交換層析或凝膠過濾層析等技術,使該技術與後兩者經常聯合使用來分離複雜的生物樣品。目前該技術主要套用領域是在蛋白質的純化方面,成為血清蛋白、膜結合蛋白、核蛋白、受體、重組蛋白等,以及一些藥物分子,甚至細胞等分離時的有效手段。
填料
研製和開發新型的色譜填料仍是HIC 發展的技術核心。從疏水色譜填料的基質來看, 填料包括無機和有機填料兩種。
無機填料: 無機填料中, 矽膠在HIC 套用較廣泛, 其優點是機械性能好, 孔結構和表面積易於控制, 並有較好的化學穩定性。但矽膠的pH 值套用範圍較窄( 2. 0~ 8. 0) , 且矽膠表面上的矽羥基可對蛋白質產生不可逆吸附。另外, 矽羥基的解離可使填料具有陽離子交換性質, 使分離產生混合機理。
近年來, 多用高分子塗層矽膠填料替代單純矽膠填料。這種填料選用合適的聚合物、寡聚物或單體, 在矽膠表面形成緻密的聚合物塗層, 使其既具有高聚物的化學穩定性, 又具有矽膠基質的高機械強度。
有機填料: 在有機物填料中, 多聚糖( 如瓊脂糖) 最常用, 它具有表面基團豐富、pH 使用範圍較寬及與生物大分子良好的相容性等優點, 但其機械強度不能用於高壓疏水色譜。另外, 在與配基偶聯時,常需劇毒CNBr 活化, 且工藝較複雜。近年來, 有學者嘗試用殼聚糖為基質研製疏水色譜填料, 並成功用於A-澱粉酶、雞卵類黏蛋白的分離純化。疏水色譜填料配基的一個重要特徵是具有弱疏水性, 與蛋白質作用溫和, 從而能保證蛋白質的生物活性不喪失。疏水色譜填料配基密度較低, 碳鏈長度一般在C-Cs 之間。烷基、苯基是常用的HIC 填料配基。如果結合力過強, 蛋白質難以洗脫, 需用一些高離液序列鹽類( Chaotropic salt) 或有機溶劑洗脫,但此時蛋白質易喪失生物學活性。
操作過程
介質的選擇
在HIC中,應選機械強度較大的剛性基質;若待分離物質分子量很大,且樣品量較大,則應選大孔基質,如瓊脂糖凝膠;若待分離物質較小,或樣品量很小,但解析度的要求高,則可選孔徑小的基質甚至非孔型基質。
HIC介質中,烷基配基的鏈長大多在C4~C8之間,苯基的疏水性大致與戊基相當,因與溶質發生π-π相互作用,它與戊基有不同的選擇性,而寡聚乙二醇固定相的疏水性介於丁基與苯基之間。
樣品的準備
往樣品中添加足夠濃度的鹽,使樣品溶液中的鹽濃度達到與流動相A(平衡液)中基本一致,並調節樣品溶液的pH使其滿足吸附條件 ,同時選擇適當濃度及pH的緩衝液。
HIC的樣品體積受樣品中組分濃度和介質的結合容量的影響,對於稀釋樣品無需濃縮可以直接加樣。
層析條件的最佳化
最佳化目標:
目標分子達所需純度的基礎上,獲得儘可能高的回收率,同時力求縮短分離所需時間、降低分離成本。
HIC中,層析條件包括流動相A,流動相B,洗脫方式,層析柱的柱長,流速,溫度等。
流動相A的緩衝液的種類、pH ,鹽的種類和濃度的選擇:
緩衝液種類據所需的pH選擇,注意目標物的穩定性,濃度一般在0.01--0.05mol/L;
不同鹽類對疏水作用的強度有影響,層析中的選擇性也不盡相同;鹽濃度也隨目標分子的疏水性而異,(NH4)2SO4常用0.75~2mol/L,NaCl為1~4mol/L;
流動相B為含鹽量較低的緩衝液,緩衝液類型與流動相A一致。
洗脫的方式:
採用降低流動相中鹽濃度的方式洗脫(最常用);
通過往流動相中添加有機溶劑 ,如:乙二醇、丙醇、異丙醇等,降低流動相極性的方式洗脫 (溶劑中穩定性良好的物質);
往流動相中添加去污劑等 ,去污劑本身能與介質發生強烈吸附,從而將結合在其上的目標組分置換下來(分離膜蛋白)。
洗脫理論:
疏溶劑理論:1976年由Sinanoglu等人提出,認為由於溶質分子有減少其與水接觸的非極性表面的傾向,而增加了與疏水配基結合的機率。
自由能分離理論:1979年Vanoss等人提出,認為生物體界面自由能比水低,與配基產生范德華力,這個引力隨溶液鹽析能力的改變而改變。
熵分離理論:1984年Regnier提出,認為高鹽溶液中,蛋白質疏水區域的鄰近分子是有序排列,疏水部分易於配基結合,減弱了水分子排列的有序度,表面水分子被排斥開,使體系熵增加。
層析介質的再生、貯存
再生:常規用蒸餾水清洗,如有疏水性很強的物質如脂類、變性蛋白等牢固結合在介質上,則需合適的清洗劑進行清洗,NaOH溶液是其中常用的一種清洗劑,它在清洗層析柱的同時還能使微生物鈍化滅活起到消毒的效果。此外,促溶鹽類的水溶液也是良好的清洗劑。
貯存:一般懸浮在20%的乙醇中,如在水溶液體系中保存,則需添加一定量的防腐劑,以防止微生物的生長。
影響因素
鹽類和鹽組成
鹽的摩爾表面張力增大,蛋白質在疏水層析柱內的吸附能力相應增大。各種鹽離子和離子對具有破壞周圍水分子有序排列的能力。 流動相中鹽的組成對蛋白質在疏水層析介質上的吸附能力具有最為重大的影響。選擇合適的鹽對保證蛋白質的分離以及分離後蛋白質的活性都很重要。硫酸銨、醋酸銨、氯化鈉和磷酸鹽是疏水層析分離常用的幾種鹽。
離子強度
離子強度的大小直接影響樣品組分在固定相的保留值。一般增加離子強度來增加組分的保留值,降低離子強度來提高組分的解析附能力。
HIC實驗中,改變離子強度進行洗脫的方式,一般宜採用梯度洗脫法,可提高分離的選擇性。
溶液的酸鹼度
溶液的pH值主要考慮能維持生物大分子生物活性的pH環境。一般情況,溶液的pH接近蛋白質的等電點,其疏水性增加,有利於與固定相配基相互作用;遠離其等電點,其疏水性減少,不利於與固定相配基結合,但有利於蛋白質洗脫。因此通過改變溶液的pH也可以改變蛋白質的疏水性。
柱溫
一般柱溫升高,生物大分子的構象會發生變化,疏水作用增加,吸附能力增加,有利於提高層析柱的分離度,所以有時可以通過提高柱溫來增加疏水基團與配基間的相互作用,分離性質相近的化合物,如對分離一些小分子是非常有效的。但是對於具有生物活性的物質或酶類,在高溫條件下易變性失活,因此不宜在高溫條件下進行分離。一般都在常溫或低溫下操作。