放射性鐵的種類
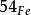 放射性鐵
放射性鐵 放射性鐵
放射性鐵 放射性鐵
放射性鐵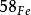 放射性鐵
放射性鐵 放射性鐵
放射性鐵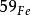 放射性鐵
放射性鐵鐵的同位素具放射性的有三種,其原子質量數為53,55和59,其穩定的同位素有4種,為 、 、 、 ,其臨床常用者為 , ,又以後者使用更多。
放射性鐵的毒理學
放射性鐵(Fe59,Fe55),也是工、農、醫各部門套用較廣的放射性核素。它套用於人體鐵代謝及血液系統疾病的研究中起到重要作用。近些年來,由於鐵的比活性大大提高;在醫學和生物學的研究及治療疾病中得到更廣泛地套用。
 放射性鐵
放射性鐵鐵59為p、y-輻射源,半衰期45天,β-粒子能量為1.56(o.3%)、0.46(54%)、0.27(45%)、0.13(1%)兆電子伏;主要Y一射線的能量為1.29(43%)、1.10(57%)兆電子伏,衰變後成為穩定性鈷( )。
常套用的放射性鐵製劑,有氯化高鐵,檸檬酸鐵和抗環血酸鐵。
放射性鐵及似鐵製劑
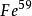 放射性鐵
放射性鐵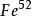 放射性鐵
放射性鐵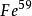 放射性鐵
放射性鐵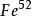 放射性鐵
放射性鐵正常人骨髓紅細胞生成占血漿鐵更新的80%一90%,因此,放射性鐵包括和加速器生產的(0.511MeV的正電子湮沒輻射和電子俘獲衰變伴隨γ射線能量為169kev)可用於骨髓顯像,優於骨髓RHS顯像的是,可以鑑別紅細胞生成活性的骨髓,因網狀內皮(RE)細胞(即吞噬細胞)活性的變化並不總是反映紅細胞生成系統的擴大與收縮。從生理觀點來看,評價功能性骨髓的放射性鐵是理想的。但可獲得的放射性鐵核素的顯像性能都不令人滿意。—檸檬酸亞鐵有時用於骨髓顯像。它是β衰變伴隨發射Y射線能量高(主要為1.1和1.3MeV),通常缺乏適於高能γ射線顯像的儀器,加上對病人輻射劑量高,因此被認為是不適用的。52Fe因物理半衰期短(8h),受限於靠近加速器生產的地方使用,價格又貴,故很少採用。雖然和PET儀器適用於紅細胞生成的骨髓顯像,對溶血性或高鐵成紅細胞性貧血,骨髓纖維化和少見的真性紅細胞增多症的病人都已證實有骨髓膨脹。但由於核素和儀器的限制,這種顯像方法仍不能廣泛套用。
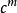 放射性鐵
放射性鐵放射性核素銦的化學性質與鐵相似,在可獲得的放射性銦同位素中以111In的顯像特性最佳。111ln—InCl3靜脈注射後,濃集部位與鐵很相似,也濃集於骨髓。注射後在低pH時,它與血清轉鐵蛋白結合,且與鐵有競爭性抑制,但生物學行為不同於鐵,可能因為與鐵有顯著不同的氧化還原特性。游離態的銦由血清除(T1/2=5h)比鐵慢、被骨髓攝取約30%ID、肝20%(較鐵高)、腎7%、脾1%、其餘均勻分布在全身的流體內。它濃集於骨髓的量比鐵少,紅細胞濃集也明顯不同。在12—14d循環的紅細胞中含鐵達到80%ID,而銦僅為4%。111In—InCl3結合紅細胞是可逆的,不與血紅蛋白而是與細胞膜結合,故不能用於鑑別紅細胞生成的真正靶細胞[3,5,50,52]。當pH>4時,它在水溶液中形成氫氧化物的絡合物。並不確知它在骨髓內的細胞和亞細胞分布。靜脈注射骨髓正常的病人後,顯像表現111In的分布與99T標記的膠體相似。用它診斷骨髓造血功能的原理還不完全清楚。它是骨髓早期鐵攝取的有效標誌,骨髓經5Gy輻照後,111In的骨髓攝取不受影響,而放射性鐵攝取明顯降低[3,5],因此它的顯像濃集不能代表放射性鐵的攝取。當鐵過剩和鐵結合容量飽和的病人,靜脈注射的111In—InCl3、形成膠態核隨後被RE系統的細胞吞噬,轉鐵蛋白飽和也起同樣作用,可以解釋它在這些病人中的RE系統行為。據報導它用作骨髓顯像劑,與再生障礙性貧血、骨髓纖維化及其他血液學疾病的臨床狀況相符,但美國仍未批准常規套用[5]。111In對肝和紅骨髓所致輻射吸收劑量較高,達到0.6mGy/MBq;有效劑量當量為0.26mSv/MBo[41]。
海水中放射性鐵的濃集方法
氫氧化鐵共沉澱法是從海水中濃集放射性鐵的常用方法,用NaOH或NH4OH調節海水的pH為10左右,使之生成Fe(OH),與Mg(OH):共沉澱,然後進行傾析和過濾:但是用氫氧化物沉澱回收海水中的痕量元素也有許多缺點:沉澱量多,顆粒細,難於過濾,沉澱物與海水比重差別不大.需要靜置較長的時間。為了加快沉降速度,縮短過濾時間,神戶弘已等研究了添加高分子凝集劑加速沉降過程的濃集方法,只需靜置10分鐘,鐵的回收率在90%以上。
甲田善生等用吡啶代替氨水使之生成吡啶絡合物從pH6—7的海水中沉澱若干种放射性核素,對59Fe的共沉澱率大於95%。此法的優點是pH較低,但由於毗啶用量大(100ml海水需要用5ml20%吡啶),臭味濃,實驗室需有良好的通風設備。
用MnOz從海水中濃集放射性鐵也很有效。Yamagat等選用1%( W/ V)的粉末狀的MnO2從pH 8.2的海水中濃集由核反應堆釋放的數種重要的放射性同位素,對55,59Fe的濃集率為96%。Langford用Mn02在pH8.0的條件下從海水中濃集55Fe,取得了良好的結果。
亞鐵氰化物具有選擇性吸附放射性核素的性質。Kwamura等用亞鐵氰化路吸附1升海水中的放財性核素,對59Fe的吸附率在95%以上。但是亞鐵氰化鋯的吸附能力較弱,只能用於l升海水的測定,當海水樣品體積超過1升時.回收率就大大減少。
如果只測定海水中顆粒態的或懸浮物中的放射性鐵,可用微孔過濾器收集濾物,然後再進行放射化學分離和測定。
危害
在大劑量的照射下,放射性對人體和動物存在著某種損害作用。
照射劑量在150rad以下,死亡率為零,但並非無損害作用,住往需經20年以後,一些症狀才會表現出來。放射性也能損傷遺傳物質,主要在於引起基因突變和染色體畸變,使一代甚至幾代受害。
套用
放射性鉄的套用對於人體鉄代謝及血液學研究等作出了貢獻。如果不用放射性鉄作示蹤,就無法區別新吸收入的鉄抑或體內原有的鈇,同時鉄的轉運、生化過程、體內分布、排出及紅血球生成等項研究工作,用一般的化學方法進行是有閒難的。因此,自1939年Hahn等用放射性鉄研究貧血以來,此法在臨床上逐漸被採用,由於鉄的比放射性大有提高,在生理學及臨床上更較廣泛地採用了。
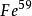 放射性鐵
放射性鐵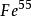 放射性鐵
放射性鐵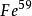 放射性鐵
放射性鐵 放射性鐵
放射性鐵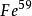 放射性鐵
放射性鐵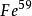 放射性鐵
放射性鐵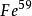 放射性鐵
放射性鐵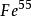 放射性鐵
放射性鐵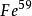 放射性鐵
放射性鐵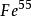 放射性鐵
放射性鐵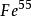 放射性鐵
放射性鐵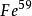 放射性鐵
放射性鐵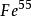 放射性鐵
放射性鐵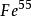 放射性鐵
放射性鐵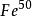 放射性鐵
放射性鐵示蹤用的放射性鉄有 和 二種。 的物理半衰期為45.1天,它按β衰變的方式放射出三組β射線【其最大能量分別為0.27(占46%)、0.46(占54%)和1.56(占0.3%)百萬電子伏特】及三支γ射線(其能量分別為1.29、1.1、0.19百萬電子伏特)之後,衰變成為穩定性的 。 可以從回旋加速器中產生,但是它的此放射性很低,不能滿足臨床使用的要求。自從有了反應堆以後, 的生產方法有了改善,提高了比放射性,成為臨床上所使用的 。 的物理半衰期為2.94年,它以K俘獲的方式衰變,放射出軟X射線。當時由於 的比放射性低,遂採用鉄 ,然而, 的半衰期較長且其射線能量低,因此在反應堆生產 之後,就被後者所代替。但是, 並未被摒棄,因為直到最近臨床上仍在套用 ,它多半是與 一起作雙標記用。
常用的放射性鉄的化學製劑有氯化高鉄、枸櫞酸鉄和抗壞血酸鉄三種,它們的比放射性都已達到合乎臨床使用的水平(0.6~1.6毫居里/毫克,0.1毫居里/毫升或更高些)。

