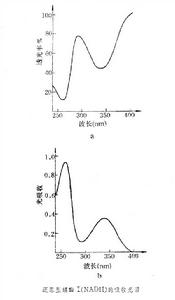
吸收光譜(紫外光和可見光)
正文
光透過某一物質時,某些波長的光被該物質吸收,因此在連續光譜中有一段或幾段波長的光減弱了或消失了,這種光譜稱為吸收光譜。不同物質的吸收光譜不同,這取決於物質的分子、原子和原子團,因此可用吸收光譜來鑑別物質和推測樣品的結構;同時吸收光譜的強弱和物質的濃度有關,這個性質可用來做定量分析。原理 入射光(I0)經過均勻而透明的溶液時,一部分光被溶質吸收(IA),一小部分被反射(IR),只有一部分可以透過(IT)。
I0=IA+IR+IT
在化學分析中,常用一個“空白”溶液作為參考去校正反射的光,則IR可以忽略不計。I0=IA+IT此處 I0又可以看作為透過“空白”的光強度,因為“空白”是不吸收任何光的。所以IT/I0是透光率(T),常用%來表示;但在實際套用中,往往用光吸收 (A)來表示。
A=logI0/IT
圖a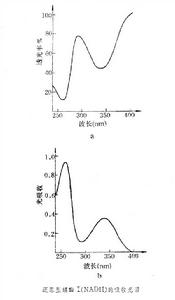 是以T來表示的吸收光譜,而圖b是文獻中常見的以A表示的吸收光譜,從這兩個圖譜可以了解到T和A的關係。
是以T來表示的吸收光譜,而圖b是文獻中常見的以A表示的吸收光譜,從這兩個圖譜可以了解到T和A的關係。 當某一物質吸收一定波長的光時,若此時A=1,即其透過光的強度為照射光的10%;若A=2,表示濃度大了一倍,其透過光的強度為照射光的1%。根據貝爾定律,A=ELC,A為光吸收,E為吸收係數,L為吸收杯光徑,C為濃度。在溶液濃度不很大的情況下,由光在溶液中被吸收的程度A,可以決定溶液的濃度C,這就是吸收光譜定量分析的原理。
分光光度計的構造和性能 分光光度計通常包括光源,分光系統和受光器等幾個主要部分:
光源 一般340納米以上採用鎢燈作為燈源,340納米以下採用氫燈或氘燈作為燈源。在安裝時,燈絲的位置要調節到恰好對準入光狹縫,此時靈敏度最佳。
分光系統 指把混合的燈源光分散成個別光波的裝置。一般是特殊玻璃或石英制的稜鏡;另一種色散系統是衍射光柵。
受光器 通常是光電池或光電倍增管。透過光的能量一般是很小的,受光器能把它轉變成電流並放大,光電流的訊號和強弱再用電流計或記錄儀顯示或記錄下來。光狹縫有兩種表示方法,一種以毫米表示實際狹縫寬度,另一種用光譜狹縫表示,單位是納米。狹縫愈小,光純度愈高,但透過的光強度也愈弱,在實際套用中要根據實驗的要求加以調整。存放樣品的吸收杯,在測可見光時可採用玻璃制的吸收杯,在測紫外部分時必須採用石英吸收杯。
常用的分光光度計是直接讀數或零點法,也有用記錄儀記錄的。
套用 任何物質只要它有吸收光譜,就可以用來做定性和定量分析。
定性分析 根據樣品吸收曲線的形狀,並與已知物質吸收光譜對比,可知其是否同一物質。譬如生物樣品中,蛋白質吸收高峰一般在280納米,核酸通常吸收高峰在260納米。氧化型輔酶Ⅰ吸收高峰在260納米,而還原型輔酶Ⅰ在 340納米出現一個新吸收峰。幾種不同的核苷酸,它們的250納米/260納米和280納米/260納米比值是各不相同的,可以方便地區別開。
定量分析 ①單組份定量,根據測量到的樣品的光吸收值和已知的樣品消光係數,可以計算出樣品的量。②多組份分析,如果樣品是個混合物,其中含有兩種或兩種以上的吸收物質,這些物質之間不起化學反應,其吸收光譜雖然互相重疊,但各自的吸收峰和峰谷是不同的,這樣可以不經分離而直接用光譜法對各個組分進行定量測定。以兩個組分A和B的混合物為例,選擇二個波長,一個是A組分的最大吸收(憶),另一個是B組分的最大吸收(憻),再分別以A和B溶液在這二個波長下測出各自的消光係數(E憶A、E憶B、E憻A和E憻b),然後再用混合物在這二波長下測出光吸收A憶和A憻。因此
A憶=E憶A·CA+E憶B·CCB
A憻=E憻A·CA+E憻B·CB這兩個式中除CA和CB是未知濃度外,其餘光吸收(A)和消光係數(E)均為已測知數,解這聯立方程,即可計算出濃度CA和CB。③酶活性測定,當酶反應的底物或產物中有一個明顯的吸收光譜時,借測這個生色基團的出現或消失速度可以跟蹤酶的反應。例如氧化型和還原型輔酶Ⅰ的互變在 340納米處有一個吸收峰的消失或生成,這一特性經常用於測定某些脫氫酶的活性。差光譜法 差示分光光度法是測二種吸收光譜之差。其優點是能檢出光吸收大的系統中比較小的光吸收變化。①當被測定物質濃度很大,而又不能稀釋後再測定,如此測定的誤差就會很大。有些高級的分光光度計雖然光吸收可以測到很高值,但也不能無限制的擴大。這種情況下可採用略低於樣品濃度的已知濃度純物質作為參考樣品置於空白對照光徑中,再進行未知樣品濃度的測定,使得欲測定樣品的讀數仍然落在刻度盤讀數範圍內。②在研究蛋白質構象中,蛋白質或酶在加入作用物後,光譜會產生微小的變化,而蛋白質本身濃度往往較大,不容易察覺到這種微小變化。此時可在參考光徑中把酶和作用物分別置於二個吸收杯中,而在測量光徑中把酶和作用物放在同一個吸收杯中,而測量光徑中的第二個吸收杯中僅為相應的緩衝液,這樣進行波長掃描,可以清楚地觀察到某些波長處的變化,並可定量。
光譜滴定 滴定法中會有 3個組分──滴定劑、被滴定物和生成物。只要這三個組分中任何一個組分有光吸收,且在滴定過程中光吸收會增強或減弱,則可利用光譜法測得其滴定終點,計算其濃度。例如滴定蛋白質中某個胺基酸殘基數,可用相應的試劑,每次加入一定體積後攪拌均勻並測其光吸收。儘管每次加入試劑體積極微,但仍需進行體積校正得到校正後的光吸收值。以光吸收為縱坐標,滴定劑量為橫坐標,可以得到一個光譜滴定曲線,其轉折點即為滴定終點。以蛋白質量與作用試劑的化學計量之比即可計算出此胺基酸殘基數。
在進行光譜分析時,除了儀器本身的性能,以及使用不妥會影響到測定結果外,還有一些因素也會影響實驗結果。例如同一樣品在不同溶劑中,它的吸收峰和消光係數往往不同;在不同PH下,光譜特性和光吸收也會有所變化。某些特殊情況下(例如酶反應),溫度也會影響到測定,都需加以注意。