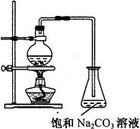
 實驗裝置示意圖
實驗裝置示意圖乙酸的酯化反應制乙酸乙酯的方程式:CH3COOH+CH3CH2OH===CH3COOC2H5+H2O (可逆反應、加熱、濃硫酸催化劑)
1:酯化反應是一個可逆反應。為了提高酯的產量,必須儘量使反應向有利於生成酯的方向進行。一般是使反應物酸和醇中的一種過量。在工業生產中,究竟使哪種過量為好,一般視原料是否易得、價格是否便宜以及是否容易回收等具體情況而定。在實驗室里一般採用乙醇過量的辦法。乙醇的質量分數要高,如能用無水乙醇代替質量分數為95%的乙醇效果會更好。催化作用使用的濃硫酸量很少,一般只要使硫酸的質量達到乙醇質量的3%就可完成催化作用,但為了能除去反應中生成的水,應使濃硫酸的用量再稍多一些。
2:製備乙酸乙酯時反應溫度不宜過高,要保持在60 ℃~70 ℃左右,溫度過高時會產生乙醚和亞硫酸等雜質。液體加熱至沸騰後,應改用小火加熱。事先可在試管中加入幾片碎瓷片,以防止液體暴沸。
3:導氣管不要伸到飽和Na2CO3溶液中去,防止由於加熱不均勻,造成飽和Na2CO3溶液倒吸入加熱反應物的試管中。
3.1:濃硫酸既作催化劑,又作乾燥劑。
3.2:飽和Na2CO3溶液的作用是:
(1)乙酸乙酯在無機鹽飽和Na2CO3溶液中的溶解度減小,容易分層析出。
(2)Na2CO3能跟揮發出的乙酸反應,生成沒有氣味的乙酸鈉,便於聞到乙酸乙酯的香味。
3.3:為有利於乙酸乙酯的生成,可採取以下措施:
(1)製備乙酸乙酯時,反應溫度不宜過高,保持在60 ℃~70 ℃。不能使液體沸騰。
(2)最好使用冰醋酸和無水乙醇。同時採用乙醇過量的辦法。
(3)起催化作用的濃硫酸的用量很小,但為了除去反應中生成的水,濃硫酸的用量要稍多於乙醇的用量。
(4)使用無機鹽飽和Na2CO3溶液吸收揮發出的乙酸。
