理化性質
物理性質
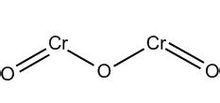 三氧化二鉻結構式
三氧化二鉻結構式溶解性:不溶於水,溶於酸和鹼,溶於金屬溴酸鹽溶液。
化學性質
溶於熱的鹼金屬溴酸鹽溶液。不溶於水、醇、酸和鹼。對光、大氣、高溫及二氧化硫和硫化氫等腐蝕性氣體均極穩定。有很高的遮蓋力。有毒。
與許多二價金屬的氧化物一起加熱至高溫能生成尖晶石型化合物。
具有α-Al₂O₃結構。Cr₂O₃對酸鹼都具有很好的穩定性,與酸鹼一般不反應。三價鉻的氫氧化物,Cr(OH)₃具有兩性,能夠與酸鹼發生反應。
經過灼燒的Cr₂O₃,晶型緻密,類似於剛玉,不溶於酸,但可用熔融法使它變為可溶性的鹽。如Cr₂O₃與焦硫酸鉀在高溫下反應:
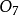 三氧化二鉻
三氧化二鉻Cr₂O₃+ 3K₂S₂
=3K₂SO₄+ Cr₂(SO₄)₃
用途
主要用於冶鍊金屬鉻和碳化鉻。用作搪瓷、陶瓷、人造革、建築材料的著色劑、有機化學合成的催化劑、耐曬塗料、研磨材料、綠色拋光膏和印刷紙幣的專用油墨。
亦用於生產高鉻磚、鉻剛玉磚等耐火材料。
使用注意
危險性概述
侵入途徑:皮膚接觸,吸入,食入。
健康危害:3價鉻對鼻、喉、皮膚無損害,6價鉻刺激鼻、喉、皮膚、眼睛。
急救措施
皮膚接觸:用肥皂、水沖洗5分鐘。
眼睛接觸:用大量水沖洗至少15分鐘;就醫。
吸入:將患者移至空氣新鮮處,輸氧或施行人工呼吸。
泄漏應急處理
應急處理:須穿戴防護用具進入現場;使用簡便的方法將粉末泄漏物收集至密閉容器中。
操作處置與儲存
儲存注意事項:存於密閉容器內,置於涼爽、通風處或規定的場所;避禁忌物。
製備
氧化還原法
由重鉻酸鉀和硫磺混合後進行還原反應,經濕磨、熱水洗滌、壓濾、乾燥、粉碎製得。
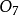 三氧化二鉻
三氧化二鉻K₂Cr₂
+ S == KSO₄ + Cr₂O₃
三氧化鉻分解法
可用鉻酸酐經1100℃熱分解,冷卻,高速粉碎製得。
4CrO₃ =1100°C= 2Cr₂O₃ + 3O₂↑
氫氧化鉻分解法
或用氫氧化鉻在高溫下熱分解,經洗滌,乾燥,粉碎製得。
2Cr(OH)₃ =△= Cr₂O₃ + 3H₂O
重鉻酸銨分解法
(NH₄)₂Cr₂O7 == N₂↑ + Cr₂O₃ + 4H₂O

