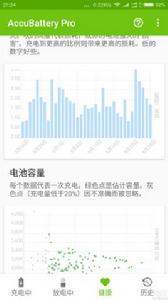
概述
 電池損耗
電池損耗電池在使用之後,出現電池損耗是很正常的情況。電池損耗的多少和電池使用頻率的高低成直接的關係。在連線外接電源的情況下,本本電池首先會被充電,待充滿後會自動處於不工作狀態。因此,有條件使用外接電源時,儘量使用外接電源,這樣可以減少電池的損耗。
損耗原因
電池損耗指的是電池在長時間使用後,實際容量變小,低於標稱容量。電池損耗通稱為記憶效應,但一般僅指筆記本電腦的記憶效應。電池損耗的原因很多,主要包括:
1、電池本身質量較差
2、使用劣質充電器
3、高溫或低溫環境長時間作業
4、使用電池是接高負荷外設,插拔不規範。
5、過度充放電(電池使用到剩餘電量低於3%)。電路都有保護,但是偶爾會發生。
6、長期在電磁強輻射地使用電池(會干擾電池內金屬的導電性)
7、長期在濕潤的條件下使用電池(潮濕的電池會性能降低)
Windows8及以上版本可以在命令提示符中輸入“powercfg /BatteryReport”查看電池使用和損耗,也可用硬體檢測軟體(如Everest、魯大師)看到,有時還會誤報。
容量恢復
對於一些用了較長時間的筆記本電池,電池損耗是不可避免的,而且損耗的比例會很高,高達30-40%以上。這樣直接影響到了電池的續航力能,以前可以續航3小時的,可能就只能支撐1.5-2小時,降低了筆記本戶外工作的能力。通過深度放電的方法可以讓損耗的電池容量恢復。方法如下:首先,啟動筆記本進入系統,把外接電源拔掉,用電池供電,直到電池耗儘自動關機。然後,插上電源充電並開機,直到充滿後,再次拔掉外接電源,直到電池耗儘自動關機。反覆3次以上操作,能起到電池修復作用,電池的容量能得到一定程度的恢復。
這個方法不建議新買筆記本的用戶使用,其實電池有10%以內的損耗,並不影響正常使用。對於電池已經使用較長時間,電池損耗較大,續航能力明顯變短的情況,可以使用這種深度放電的方法。
常見問題
筆記本鋰電池損耗有可能出現降低的情況嗎?
1. 電池損耗可能提升嗎?
(長期滿電使用可能會導致鋰離子失去活性,難道一到兩個月做一次完全循環充電可以激活部分?)
定期充放電,即使沒有記憶效應的鋰離子電池存在一定的惰性效應,長時間不使用會使鋰離子失去活性,需要重新激活。因此,如果長時間(3個星期或更長)不使用電腦或發現電池充放電時間變短,應使電池完全放電後再充電,一般每個月至少完整地充放電1次。
容量損失分析
由於鋰離子電池在充放電過程中過充電或過放電、電解液分解、SEI 膜的形成、活性物質的溶解及其他因素會導致電池容量損失。
一、鋰離子電池工作原理
鋰離子電池是指分別用兩種能可逆嵌入與脫嵌鋰離子的層間化合物作正負極活性物質而構成的二次電池,目前生產中普遍採用高嵌脫鋰電位的LiCoO2 類材料為正極,低嵌脫鋰電位的碳類材料為負極。鋰離子電池在最初的充電循環中,在碳負極材料會出現化學/電化學反應過程,分別對應有機電解液的分解和鋰離子的嵌入,伴隨形成SEI 膜。常用的有機溶劑有碳酸丙烯酯(PC)、碳酸乙烯酯(EC)、碳酸二乙酯(DEC)、碳酸二甲酯(DMC)和碳酸甲基乙基酯(EMC)等,電解質一般用鋰鹽有LiBF6、LiPF4、LiAsF6 和LiCIO4 等。隔膜用PP 微孔薄膜或PE 微孔薄膜。電極反應如下:
正極:LiCoO2充電→← 放電Li1 - xCoO2+xLi++xe-20
負極: 6C + xLi + + xe -充電→← 放電 LixC6
總的反應為: 6C + LiCoO2充電→← 放電 Li1-xCoO2+LixC6
充電時,鋰離子從LiCoO2 中立方緊密堆積氧層中八面體位置發生脫嵌,釋放一個電子給Co3+,其氧化為Co4+;放電時,鋰離子嵌入到八面體位置得到一個電子,Co4+還原為Co3+。負極中當鋰離子插入到石墨層中後石墨結構與此同時從外電路得到一個電子使得負極電荷平衡。與其它二次電池一樣,鋰離子經充放電循環後存在容量損失問題,導致這些問題的原因有很多,有材料方面也有製造工藝方面的因素。
二、容量損失原因分析
1.過充電
所謂過充電就是超過規定的充電終止電壓(一般為4.2V)而繼續充電的過程。在過充的情況下會造成電池容量的衰減,主要有如下因素:
① 石墨負極的過充反應;②正極過充反應;③電解液在過充時氧化反應。電池在過充時,鋰離子容易還原沉積在負極表面:Li++e→Li(s)
沉積的鋰包覆在負極表面,阻塞了鋰的嵌入。導致放電效率降低和容量損失,原因有:①可循環鋰量減少;②沉積的金屬鋰與溶劑或支持電解質反應形成Li2CO3,LiF 或其他產物;③金屬鋰通常形成於負極與隔膜之間,可能阻塞隔膜的孔隙增大電池內阻。快速充電,電流密度過大,負極嚴重極化,鋰的沉積會更明顯。正極過充導致容量損失主要是由於電化學惰性物質(如Co3O4,Mn2O3 等)的產生,破壞了電極間的容量平衡,其容量損失是不可逆的。
LiyCoO2→(1-y)/3[Co3O4+O2(g)]+yLiCoO2 y<0.4
同時正極材料在密封的鋰離子電池中分解產生的氧氣由於不存在再化合反應(如生成H2O)與電解液分解產生的可燃性氣體同時積累,後果將不堪構想。過充還會導致電解液的氧化反應,其氧化速率跟正極材料表面積大小、集電體材料以及所添加的導電劑(炭黑等)有很大關係,同時,炭黑的種類及表面積大小也是影響電解液氧化的一個重要因素,其表面積越大,溶劑更容易在表面氧化。當壓高於4.5V 時電解液就會氧化生成不溶物(如Li2Co3)和氣體,這些不溶物會堵塞在電極的微孔裡面阻礙鋰離子的遷移而造成循環過程中容量損失。
2.電解液分解
電解液由溶劑和支持電解質組成,在正極分解後通常形成不溶性產物Li2Co3 和LiF等,通過阻塞電極的孔隙而降低電池容量,電解液還原反應對電池的容量和循環壽命會產生不良影響,並且由於還原產生了氣體會使電池內壓升高,從而導致安全問題。電解液在石墨和其它嵌鋰碳負極上穩定性不高,容易反應產生不可逆容量。初次充放電時電解液分解會在電極表面形成鈍化膜,鈍化膜能將電解液與碳負極隔開阻止電解液的進一步分解。從而維持碳負極的結構穩定性。理想條件下電解液的還原限制在鈍化膜的形成階段,當循環穩定後該過程不再發生。電解質鹽的還原參與鈍化膜的形成,有利於鈍化膜的穩定化,但還原產生的不溶物對溶劑還原生成物產生不利影響,而且電解質鹽還原時電解液的濃度減小,導致電池容量損失(LiPF6 還原生成LiF、LixPF5-x、PF3O 和PF3),同時,鈍化膜的形成要消耗鋰離子,這會導致兩極間容量失衡而造成整個電池比容量降低。工藝中使用碳的類型、電解液成份以及電極或電解液中添加劑都是影響成膜容量損失的因素。電解液中常常會含有氧、水和二氧化碳等。微量水對石墨電極性能沒影響,但水含量過高生成LiOH(s)和Li2O 沉積層,不利鋰離子嵌入,造成不可逆容量損失:H2O+e→OH-+1/2H222
OH-+Li+→LiOH(s)
LiOH+Li++e→Li2O(s)+1/2H2
溶劑中的CO2 在負極上能還原生成CO 和LiCO3(s):
2CO2+2e+2Li+→Li2CO3+CO
CO 會使電池內壓升高,而Li2CO3(s)使電池內阻增大影響電池性能。
3.自放電
自放電是指電池在未使用狀態下,電容量自然損失的現象。鋰離子電池自放電導致容量損失分兩種情況:一是可逆容量損失;二是不可逆容量的損失。可逆容量損失是指損失的容量能在充電時恢復,而不可逆容量損失則相反,如鋰錳氧化物正極與溶劑會發生微電池作用產生自放電造成不可逆容量損失。自放電程度受正極材料、電池的製作工藝、電解液的性質、溫度和時等因素影響。如自放電速率主要因溶劑氧化速率控制,因此溶劑的穩定性影響著電池的貯存壽命,如果負極處於充足電的狀態而正極發生自放電,電池內容量平衡被破壞,將導致永久性容量損失。長時間或經常自放電時,鋰有可能沉積在碳上,增大兩級間容量不平衡程度。Pistoia等認為自放電的氧化產物堵塞電極材料上的微孔,使鋰的嵌入和脫出困難並且使內阻增大和放電效率降低,從而導致不可逆容量損失。
4.電極不穩定性
如上所述,正極活性物質在充電狀態下會氧化電解質分解而造成容量損失。另外,影響正極材料溶解的因素還有正極活性物質的結構缺陷,充電電勢過高以及正極材料中炭黑的含量。其中電極在充放電循環過程中結構的變化是最重要的因素
鋰鈷氧化物在完全充電狀態下為六方晶體,理論容量的50%放電後生成新相單斜晶體,鋰鎳氧化物在充放電循環過程中涉及斜方六面體及單斜晶體的變LiyNiO2 通常在0.3<y<0.9 範圍內循環。鋰錳氧化物在充放電過程中存在2 種不同的結構變化:一是化學計量不變的情況下發生的相變化;二是充放電過程中鋰嵌入和脫嵌量改變時發生的相變。LiCoO2 鋰離子電池充電電壓超過4.2V 時,容量損失與在負極檢測到鈷含量直接相關,而且充電截止電流電壓越高,鈷溶解的速率越大。另外,容量損失(或鈷溶解)與合成活性物質的熱處理溫度有關。
5.集流體
銅和鋁分別是負極和正極集流體常用的材料。其中鋁箔無論是在空氣種還是在電解液中都比較容易在表面形成氧化物膜,同時,集流體表面全面腐蝕和局部腐蝕(如點蝕)以及粘附性差等原因都會使得電極反應阻力增大,電池內阻增加,導致容量損失和放電效率降低。為了減少這些原因造成的影響,從市場上購得的集流體最好進行預處理(酸-鹼浸蝕、耐腐蝕包覆、導電包覆等),以提高耐腐蝕性與粘附性能。因為集流體表面粘附力太小,電極局部可能會與集流體分開,增加了極化作用,對容量有很大影響。銅集流體在使用過程中腐蝕生成一層絕緣腐蝕產物膜。致使電池內阻增大,循環過程中放電效率下降,造成容量損失。當過放電時,銅箔會發生如下反應:
Cu→Cu++e-所產生的Cu(I)
在充電時會以金屬銅的形式結晶沉積在負極表面上,形成銅枝晶,極易穿透隔膜造成短路甚至出現爆炸。特別注意的是在選擇負極極片時絕對不允許有掉料露銅的極片存在,否則在露銅處極片容易生成枝晶損壞電池。防止銅集流體溶解最好是放電電壓應不低於2.5V。
c關於記憶效應:
鋰離子電池很少有鎳鎘電池的記憶效應,記憶效應的原理是結晶化,在鋰電池中幾乎不會產生這種反應。但是,鋰離子電池在多次充放後容量仍然會下降,其原因是複雜而多樣的。主要是正負極材料本身的變化,從分子層面來看,正負極上容納鋰離子的空穴結構會逐漸塌陷、堵塞;從化學角度來看,是正負極材料活性鈍化,出現副反應生成穩定的其他化合物。物理上還會出現正極材料逐漸剝落等情況,總之最終降低了電池中可以自由在充放電過程中移動的鋰離子數目。
過度充電和過度放電,將對鋰離子電池的正負極造成永久的損壞,從分子層面看,可以直觀的理解,過度放電將導致負極碳過度釋出鋰離子而使得其片層結構出現塌陷,過度充電將把太多的鋰離子硬塞進負極碳結構里去,而使得其中一些鋰離子再也無法釋放出來。這也是鋰離子電池為什麼通常配有充放電的控制電路的原因。
概念:
A過放電(Over discharge): 超過電池放電截止電壓值, 若繼續放電則可能造成電池漏液或劣化.
B過充電(Over charge): 電池到達飽充狀態後, 再繼續充電的程度大小, 過度充電可能會使電池劣化.